Cho dung dịch CuCl vào cốc chứa 200ml dung dịch Na(OH) sau khi phản ứng kết thúc người ta thu được 9,8g 1 kết tủa màu xanh . Tính nồng độ dung dịch NaOH đã dùng biết phản ứng sảy ra hoàn toàn.

Những câu hỏi liên quan
X là dung dịch AlCl3, Y là dung dịch NaOH 2M. Cho 150ml dung dịch Y vào cốc chứa 100ml dung dịch X, khuấy đều tới phản ứng hoàn toàn thấy trong cốc có 7,8 gam kết tủa. Thêm tiếp vào cốc 100ml dung dịch Y, khuấy đều đến khi kết thúc phản ứng thấy trong cốc có 10,92 gam kết tủa. Nồng độ mol của dung dịch X là A. 3,2M B. 2,0M C. 1,6M D. 1,0M
Đọc tiếp
X là dung dịch AlCl3, Y là dung dịch NaOH 2M. Cho 150ml dung dịch Y vào cốc chứa 100ml dung dịch X, khuấy đều tới phản ứng hoàn toàn thấy trong cốc có 7,8 gam kết tủa. Thêm tiếp vào cốc 100ml dung dịch Y, khuấy đều đến khi kết thúc phản ứng thấy trong cốc có 10,92 gam kết tủa. Nồng độ mol của dung dịch X là
A. 3,2M
B. 2,0M
C. 1,6M
D. 1,0M
Do khối lượng kết tủa và số mol NaOH không tỉ lệ nên ở phần 2 đã có 1 phần kết tủa tan lại
Lần 2:
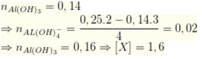
Đúng 0
Bình luận (0)
X là dung dịch AlCl3, Y là dung dịch NaOH 1M. Cho 240ml dung dịch Y vào cốc chứa 100ml dung dịch X, khuấy đều tới phản ứng hoàn toàn thấy trong cốc có 6,24 gam kết tủa. Thêm tiếp vào cốc 100ml dung dịch Y, khuấy đều đến khi kết thúc phản ứng thấy trong cốc có 4,68 gam kết tủa. Nồng độ mol của dung dịch X là A. 1,0M B. 1,2M C. 1,5M D. 1,6M
Đọc tiếp
X là dung dịch AlCl3, Y là dung dịch NaOH 1M. Cho 240ml dung dịch Y vào cốc chứa 100ml dung dịch X, khuấy đều tới phản ứng hoàn toàn thấy trong cốc có 6,24 gam kết tủa. Thêm tiếp vào cốc 100ml dung dịch Y, khuấy đều đến khi kết thúc phản ứng thấy trong cốc có 4,68 gam kết tủa. Nồng độ mol của dung dịch X là
A. 1,0M
B. 1,2M
C. 1,5M
D. 1,6M
Nhận thấy, ở lần 1 thì chưa có kết tủa tan còn lần 2 đã có kết tủa tan (nếu ở trường hợp cả 2 lần đều có kết tủa tan thì chênh lệch số mol kết tủa sẽ bằng chênh lệch số mol NaOH cho vào)
Lần 2:

Đúng 0
Bình luận (0)
Một hỗn hợp X gồm Al và Fe có khối lượng 8,3 gam. Cho X vào 1 lít dung dịch A chứa AgNO3 0,1M và Cu(NO3)2 0,2M. Sau khi phản ứng kết thúc được rắn B và dung dịch C đã mất màu hoàn toàn. B hoàn toàn không tan trong dung dịch HCl. Lấy 8,3 gam hỗn hợp X cho vào 1 lít dung dịch Y chứa AgNO3 và Cu(NO3)2 thu được chất rắn D có khối lượng là 23,6 gam và dung dịch E (màu xanh đã nhạt). Thêm NaOH dư vào dung dịch E được kết tủa. Đem kết tủa nung trong không khí đến khối lượng không đổi được 24 gam chất r...
Đọc tiếp
Một hỗn hợp X gồm Al và Fe có khối lượng 8,3 gam. Cho X vào 1 lít dung dịch A chứa AgNO3 0,1M và Cu(NO3)2 0,2M. Sau khi phản ứng kết thúc được rắn B và dung dịch C đã mất màu hoàn toàn. B hoàn toàn không tan trong dung dịch HCl. Lấy 8,3 gam hỗn hợp X cho vào 1 lít dung dịch Y chứa AgNO3 và Cu(NO3)2 thu được chất rắn D có khối lượng là 23,6 gam và dung dịch E (màu xanh đã nhạt). Thêm NaOH dư vào dung dịch E được kết tủa. Đem kết tủa nung trong không khí đến khối lượng không đổi được 24 gam chất rắn F. Các phản ứng đều xảy ra hoàn toàn. Nồng độ mol của AgNO3 và Cu(NO3)2 trong dung dịch Y là:
A. 0,1M; 0,2M
B. 0,4M; 0,1M
C. 0,2M; 0,1M
D. 0,1M; 0,4M
Đáp án D
Vì dung dịch C đã mất màu hoàn toàn nên cả Ag+ và Cu2+ đều phản ứng hết.
Mà B không tan trong HCl nên B chỉ chứa Ag và Cu. Do đó cả Al và Fe đều phản ứng hết.
Suy ra cho X vào A thì cả 4 chất đều phản ứng vừa đủ.
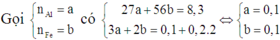
Vì dung dịch E đã nhạt màu nên Ag+ đã phản ứng hết và Cu2+ đã phản ứng một phần.
Do đó D chứa Ag và Cu.
Dung dịch E chứa Al3+, Fe2+ và Cu2+ dư. Khi đó E chứa Fe(OH)2 và Cu(OH)2
Suy ra F chứa Fe2O3 và CuO
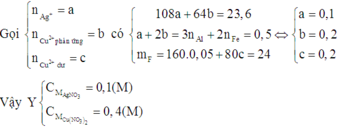
Đúng 0
Bình luận (0)
Thêm 150ml dung dịch NaOH 2M vào một cốc đựng 100ml dung dịch A1Cl3 nồng độ x mol/l, sau khi phản ứng hoàn toàn thấy trong cốc có 0,1 mol chất kết tủa. Thêm tiếp 100ml dung dịch NaOH 2M vào cốc, sau khi phản ứng hoàn toàn thấy trong cốc có 0,14 mol chất kết tủa. Tính X. A.1,6 B.1,8 C.3,2 D.3,6
Đọc tiếp
Thêm 150ml dung dịch NaOH 2M vào một cốc đựng 100ml dung dịch A1Cl3 nồng độ x mol/l, sau khi phản ứng hoàn toàn thấy trong cốc có 0,1 mol chất kết tủa. Thêm tiếp 100ml dung dịch NaOH 2M vào cốc, sau khi phản ứng hoàn toàn thấy trong cốc có 0,14 mol chất kết tủa. Tính X.
A.1,6
B.1,8
C.3,2
D.3,6
Cho Mg vào 200ml dung dịch A chứa CuSO4 0,5M và FeSO4 1M. Sau khi các phản ứng xảy ra hoàn toàn thu được 12 gam chất rắn X và dung dịch Y. Cho dung dịch Y tác dụng với dung dịch Ba(OH)2 lấy dư đến khi kết thúc các phản ứng thu được kết tủa E. Nung E trong không khí đến khối lượng không đổi thu được b gam chất rắn. Tính b.
Tính toán theo PTHH :
Mg + CuSO4 → Cu + MgSO4
Mg + FeSO4 → Fe + MgSO4
Ba(OH)2 + MgSO4 → BaSO4 + Mg(OH)2
Ba(OH)2 + FeSO4 → BaSO4 + Fe(OH)2
Mg(OH)2 → MgO + H2O
2 Fe(OH)2 + ½ O2 → Fe2O3 + 2 H2O
Giả sư dung dịch muối phản ứng hết
=> n Fe = n FeSO4 = 0,2 . 1= 0,2 mol => m Fe = 0,2 . 56 = 11,2 g
=> n Cu =n CuSO4 = 0,2 . 0,5 = 0,1 mol => m Cu = 0,1 . 64 = 6,4 g
=> m chất rắn = 11,2 + 6,4 = 17,6 g > 12 g > 6,4
=> kim loại Fe dư sau phản ứng Vì CuSO4 phản ứng trước sau đó mới đến FeSO4 phản ứng
CuSO4 đã hết và phản ứng với 1 phần FeSO4
12 g = m Cu + m Fe phản ứng = 6,4 g + m Fe phản ứng
=> m Fe = 5,6 g => n Fe = 0,1 mol => n FeSO4 dư = 0,2 – 0,1 = 0,1 mol
Theo PTHH : n Mg = 0,1 + 0,1 = 0,2 mol ( bắng số mol CuSO4 và FeSO4 phản ứng )
Theo PTHH : n Mg = n MgSO4 = n Mg(OH)2 = n MgO = 0,2 mol
n FeSO4 dư = n Fe(OH)2 = n Fe2O3 . 2 = 0,1 mol
=> n Fe2O3 = 0,1 mol
=> m chất rắn = m Fe2O3 + m MgO = 0,1 . 160 + 0,2 . 40 = 24 g
Đúng 0
Bình luận (0)
Cho từ từ đến hết 150ml dung dịch NaOH 2M vào một cốc đựng 100ml dung dịch AlCl3 nồng độ x mol/l, sau khi phản ứng hoàn toàn thấy trong cốc có 0,1 mol chất kết tủa. Thêm tiếp 100ml dung dịch NaOH 2M vào cốc, sau khi phản ứng hoàn toàn thấy trong cốc có 0,14 mol chất kết tủa. Giá trị của x là: A. 1,6 B. 1,0 C. 0,8 D. 2,0
Đọc tiếp
Cho từ từ đến hết 150ml dung dịch NaOH 2M vào một cốc đựng 100ml dung dịch AlCl3 nồng độ x mol/l, sau khi phản ứng hoàn toàn thấy trong cốc có 0,1 mol chất kết tủa. Thêm tiếp 100ml dung dịch NaOH 2M vào cốc, sau khi phản ứng hoàn toàn thấy trong cốc có 0,14 mol chất kết tủa. Giá trị của x là:
A. 1,6
B. 1,0
C. 0,8
D. 2,0
Ta thấy tỉ lệ số mol NaOH và số mol kết tủa không bằng nhau
Như vậy, phản ứng đầu chưa có kết tủa bị tan, ở phản ứng sau có kết tủa bị hòa tan
Phản ứng sau:
⇒
n
A
l
(
O
H
)
4
-
=
0
,
25
.
2
-
0
,
14
.
3
4
=
0
,
02
⇒
n
A
l
C
l
3
=
0
,
02
+
0
,
14
=
0
,
16
⇒
x
=
1
,
6
Đáp án A
Đúng 0
Bình luận (0)
Cho 300ml dung dịch NaOH 2M vào 200ml dung dịch chứa \(Fe_2\left(SO_4\right)_3\) 0,5M và \(H_2SO_4\) 0,5M đến khi phản ứng hoàn toàn, thu được m gam kết tủa và dung dịch X. Tính m và nồng độ mol các ion trong X
\(\left\{{}\begin{matrix}n_{NaOH}=0,3.2=0,6\left(mol\right)\\n_{Fe_2\left(SO_4\right)_3}=0,2.0,5=0,1\left(mol\right)\\n_{H_2SO_4}=0,2.0,5=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\left\{{}\begin{matrix}n_{Na^+}=0,6\left(mol\right)\\n_{Fe^{3+}}=0,1.2=0,2\left(mol\right)\\n_{H^+}=0,1.2=0,2\left(mol\right)\end{matrix}\right.\\\left\{{}\begin{matrix}n_{SO_4^{2-}}=0,1.3+0,1=0,4\left(mol\right)\\n_{OH^-}=0,6\left(mol\right)\end{matrix}\right.\end{matrix}\right.\)
PT ion rút gọn:
\(H^++OH^-\rightarrow H_2O\)
0,2-->0,2
\(Fe^{3+}+3OH^-\rightarrow Fe\left(OH\right)_3\downarrow\)
\(\dfrac{2}{15}\)<----0,4--------->\(\dfrac{2}{15}\)
\(\Rightarrow m=\dfrac{2}{15}.107=\dfrac{214}{15}\left(g\right)\)
dd sau phản ứng có: \(\left\{{}\begin{matrix}n_{Na^+}=0,6\left(mol\right)\\n_{Fe^{3+}\left(d\text{ư}\right)}=0,2-\dfrac{2}{15}=\dfrac{1}{15}\left(mol\right)\\n_{SO_4^{2-}}=0,4\left(mol\right)\end{matrix}\right.\)
\(V_{\text{dd}}=0,3+0,2=0,5\left(l\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C_{Na^+}=\dfrac{0,6}{0,5}=1,2M\\C_{Fe^{3+}}=\dfrac{\dfrac{1}{15}}{0,5}=\dfrac{2}{15}M\\C_{SO_4^{2-}}=\dfrac{0,4}{0,5}=0,8M\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Có 4 lít dung dịch X chứa:
CO
3
-
,
Ba
2
+
,
Na
+
và
0
,
0...
Đọc tiếp
Có 4 lít dung dịch X chứa: CO 3 - , Ba 2 + , Na + và 0 , 03 mol Cl - Cho 2 lít dung dịch X tác dụng với dung dịch NaOH dư, kết thúc các phản ứng thu được 9,85 gam kết tủa. Mặt khác, cho lượng dư dung dịch NaHSO4 vào 2 lít dung dịch X còn lại, sau phản ứng hoàn toàn thu được 17.457 g kết tủa. Nếu đun nóng toàn bộ lượng X trên tới phản ứng hoàn toàn, lọc bỏ kết tủa rồi cô cạn nước lọc thì thu được bao nhiêu gam muối khan
A. 26.65
B. 39.60
C. 26.68
D. 26.60
X là dung dịch AlCl3, Y là dung dịch NaOH 2M. Cho 150 ml dung dịch Y vào cốc chứa 100 ml dung dịch X, khuấy đều tới phản ứng hoàn toàn thấy trong cốc có 7,8 gam kết tủa. Thêm tiếp vào cốc 100 ml dung dịch Y, khuấy đều đến khi kết tủa phản ứng thấy trong cốc có 10,92 gam kết tủa. Nồng độ mol của dung dịch X là A. 3,2M. B. 2,0M. C. 1,6M. D. 1,0M.
Đọc tiếp
X là dung dịch AlCl3, Y là dung dịch NaOH 2M. Cho 150 ml dung dịch Y vào cốc chứa 100 ml dung dịch X, khuấy đều tới phản ứng hoàn toàn thấy trong cốc có 7,8 gam kết tủa. Thêm tiếp vào cốc 100 ml dung dịch Y, khuấy đều đến khi kết tủa phản ứng thấy trong cốc có 10,92 gam kết tủa. Nồng độ mol của dung dịch X là
A. 3,2M.
B. 2,0M.
C. 1,6M.
D. 1,0M.
Đáp án C.
TN1: 150 ml dd Y (NaOH 2M) vào 100 ml dd X (AlCl3) à 7,8 gam kết tủa Al(OH)3
TN2: Thêm tiếp vào cốc trên 100 ml dd Y à 10,92 gam kết tủa Al(OH)3
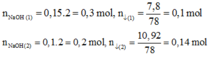


Đúng 0
Bình luận (0)







