đun nòn 0,11 mol hh khí T gồm CH4, C2H4, H2 (xúc tác Ni)sau 1 thời gian thu được 0,1 mol hh khí Q có tỉ khối so với H2 bằng 7,7
Cho Q lội qua dd Br2 dư thì có 4,8g Br2 tham gia pứ
Tính % thể tích H2 trong hh Q
Hh khí X gồm 0,3 mol H2 và 0,1 mol Viny1axeti1en. Nung X một thời gian với xúc tác Ni thu được hh khí Y có tỉ khối so với không khí là 1. Nếu cho toàn bộ Y sục từ từ vào dd brom (dư) thì có m gam brom tham gia pư. Giá trị của m là
A. 16,0
B. 3,2
C. 8,0
D. 32,0
Hỗn hợp khí X gồm 0,1 mol C 2 H 2 ; 0,2 mol C 2 H 4 và 0,3 mol H 2 . Đun nóng X với xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y có tỉ khối so với H 2 bằng 11. Hỗn hợp Y phản ứng tối đa với a mol B r 2 trong dung dịch. Giá trị của a là
A. 0,1
B. 0,2
C. 0,4
D. 0,3
Hỗn hợp khí X gồm 0,1 mol C2H2; 0,2 mol C2H4; 0,3 mol H2. Đun nóng X với xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 11. Hỗn hợp Y phản ứng tối đa với a mol Br2 trong dung dịch. Giá trị của a là
A. 0,3
B. 0,2
C. 0,4
D. 0,1
Áp dụng định luật bảo toàn khối lượng ta có:
mđầu = msau ⇒ nđầu.Mđầu = nsau.Msau
→ n s a u n đ ầ u = M đ ầ u M s a u h a y n 2 n 1 = M 2 M 1
Ta có công thức rất quan trọng là
n đ ầ u - n s a u = n 1 - n 2 = n H 2 p h ả n ứ n g - n π phản ứng
Vậy mục tiêu của ta bây giờ là đi tính n2.
Ta lần lượt có n1 = 0,1 + 0,2 + 0,3 = 0,6 mol.
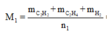
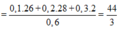
Mà M2 = 11. M H 2 = 11.2 = 22 nên từ:
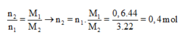
![]()
Phải hiểu rằng n2 = 0,2 mol nghĩa là số mol H2 đã phản ứng là 0,2 mol hay cũng chính là số mol π đã phản ứng là 0,2.
Do đó để tính a là số mol tối đa hỗn hợp Y phản ứng với Br2 trong dung dịch thì ta chỉ cần lấy số mol π ban đầu trừ đi số mol π ban đầu đã phản ứng, hay ta có
a = nπ (đầu) – nπ (đã phản ứng) = 0,1.2 + 0,2.1 –(0,6 – 0,4) = 0,2 mol
Đáp án B
Hỗn hợp khí X gồm 0,1 mol C2H2 ; 0,2 mol C2H4 và 0,3 mol H2. Đun nóng X với xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 11. Hỗn hợp Y phản ứng tối đa với a mol Br2 trong dung dịch. Giá trị của a là
A.0,1
B. 0,2
C. 0,4
D. 0,3
Đáp án B
BTKL: Þ mY = mX = 0,1.26. + 0,2.28 + 0,3.2 = 8,8 (gam)
Þ MY = 11.2 = 22 Þ nY = 0,4 mol
Số mol H2 tham gia phản ứng là: nX – nY = (0,1 + 0,2 + 0,3) – 0,4 = 0,2 mol
![]()
![]()
Hỗn hợp khí X gồm 0,1 mol C2H2; 0,2 mol C2H4 và 0,3 mol H2. Đun nóng X với xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 11. Hỗn hợp Y phản ứng tối đa với a mol Br2 trong dung dịch. Giá trị của a là
A. 0,3
B. 0,2
C. 0,4
D. 0,1
Hỗn hợp khí X gồm 0,1 mol CH2=CH–C–CH, 0,2 mol CH2=CH–CHO, 0,3 mol C2H4 và 0,4 mol H2. Đun nóng X với xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 16. Hỗn hợp Y phản ứng tối đa với a mol Br2 trong dung dịch. Giá trị của a là
A. 0,8
B. 1,0
C. 0,4
D. 0,6
Đáp án A
BTKL: mX = mY → nY = mX : MY = (0,1. 52 + 0,2. 56 + 0,3. 28 + 0,4. 2) : 32 = 0,8
→ n(khí giảm) = n(X) – n(Y) = n(pi p.ư) = 0,1 + 0,2 + 0,3 + 0,4 – 0,8 = 0,2
→ n(Pi trong Y) = n(Pi trong X) – n(Pi p.ư) = (0,1. 3 + 0,2. 2 + 0,3. 1) – 0,2 = 0,8 → a = 0,8
Hỗn hợp khí X gồm 0,1 mol CH2=CH–C–CH, 0,2 mol CH2=CH–CHO, 0,3 mol C2H4 và 0,4 mol H2. Đun nóng X với xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 16. Hỗn hợp Y phản ứng tối đa với a mol Br2 trong dung dịch. Giá trị của a là
A. 0,8
B. 1,0
C. 0,4
D. 0,6
Đáp án A
BTKL: mX = mY → nY = mX : MY = (0,1. 52 + 0,2. 56 + 0,3. 28 + 0,4. 2) : 32 = 0,8
→ n(khí giảm) = n(X) – n(Y) = n(pi p.ư) = 0,1 + 0,2 + 0,3 + 0,4 – 0,8 = 0,2
→ n(Pi trong Y) = n(Pi trong X) – n(Pi p.ư) = (0,1. 3 + 0,2. 2 + 0,3. 1) – 0,2 = 0,8 → a = 0,8
→ Các mệnh đề đúng là a, b, d.
X, Y là hợp chất đơn chức, Z là hợp chất tạp chức
Bài 1: Hỗn hợp X gồm 0,2 mol axetilen và 0,35 mol H2 vào bình kín có xúc tác Ni nung nóng. Sau một thời gian thu được hỗn hợp Y gồm 4 khí. Khi cho Y lội qua dung dịch Br2 dư thấy có 4,48 lít (đktc) khí Z bay ra. Tỉ khối của Z so với H2 là 4,5. Tính độ tăng khối lượng của bình brom
Bài 2: Hỗn hợp X gồm 0,2 mol C2H2 và 0,4 mol H2 được chứa trong bình jins có sẵn bột Ni (thể tích không đáng kể). Đun nóng bình một thời gian thu được hỗn hợp khí Y (tỉ khối của Y so với H2 là 6). Cho Y đi chậm qua dung dịch Br2/CCl4 dư thấy có m gam brom phản ứng. Tính m
Lúc đầu khổi lượng của hỗn hợp khí là: 0.2 x 26 + 0.35.2 = 5,9 ((g),
Khối lượng khí Z bay ra là: \(\dfrac{4.48}{22.4}\) x 4.5 x 2 =1,8 (g)
Áp dụng định luật bảo toàn khối lượng:
Độ tăng khối lượng của bình brom là: 5,9 - 1,8 = 4,1 (g)
Hỗn hợp khí X gồm 0,3 mol C2H4; 0,15 mol C2H2 và 0,5 mol H2. Đun nóng X với xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 13,3. Hỗn hợp Y phản ứng tối đa với x mol Br2 trong dung dịch. Giá trị của x là
A. 0,1
B. 0,15
C. 0,25
D. 0,3