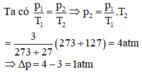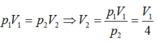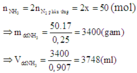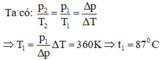một lượng chất khí được nhốt trong bình kín thể tích ko đổi ban đầu chất khí có nhiệt độ là 27°c sau đó được nung nóng đến 127°c áp suất ban đầu là 3 atm thì áp suất lúc sau là

Những câu hỏi liên quan
Xét một lượng khí không đổi chứa trong một bình kín, ban đầu khí trong bình có nhiệt độ 27 độ C và áp suất 2.10^ 5 Pa, sau đó người ta nung nóng khi đến nhiệt độ 627 độ C . Tìm áp suất của khí trong bình lúc này và vẽ đồ thị biểu diễn quá trình trên trong hệ tọa độ (p, T) ?
Trạng thái 1: \(\left\{{}\begin{matrix}p_1=2\cdot10^5Pa\\T_1=27^oC=300K\end{matrix}\right.\)
Trạng thái 2: \(\left\{{}\begin{matrix}p_2=???\\T_2=627^oC=900K\end{matrix}\right.\)
Quá trình đẳng tích:
\(\dfrac{p_1}{T_1}=\dfrac{p_2}{T_2}\Rightarrow\dfrac{2\cdot10^5}{300}=\dfrac{p_2}{900}\)
\(\Rightarrow p_2=6\cdot10^5Pa\)
Đúng 2
Bình luận (0)
Trong điều kiện thể tích không đổi, chất khí có nhiệt độ thay đổi là 27 ° C đến 127 ° C , áp suất lúc đầu 3atm thì độ biến thiên áp suất:
A. Giảm 3 atm
B. Giảm 1 atm
C. Tăng 1 atm
D. Tăng 3 atm
Một khối khí lí tưởng xác định có áp suất 1 atm được làm tăng áp suất đến 4atm ở nhiệt độ không đổi thì thể tích biến đổi một lượng 3 lít. Thể tích ban đầu của khối khí đó là : A. 4 lít B. 8 lít C. 12 lít D. 16 lít
Đọc tiếp
Một khối khí lí tưởng xác định có áp suất 1 atm được làm tăng áp suất đến 4atm ở nhiệt độ không đổi thì thể tích biến đổi một lượng 3 lít. Thể tích ban đầu của khối khí đó là :
A. 4 lít
B. 8 lít
C. 12 lít
D. 16 lít
Nung hỗn hợp gồm FeCO3 và FeS2 với tỉ lệ mol là 1:1 trong một bình kín chứa không khí dư với áp suất p1 atm. Sau khi các phản ứng xảy ra hoàn toàn đưa bình về nhiệt độ ban đầu thu được chất rắn duy nhất là Fe2O3 và áp suất khí trong bình lúc này là p2 atm. (thể tích các chất rắn không đáng kể và sau phản ứng lưu huỳnh ở mức oxi hóa +4). Mối liên hệ giữa p1 và p2 là: A. p1 p2 B. p1 2p2 C. 2p1 p2 D. p1 3p2
Đọc tiếp
Nung hỗn hợp gồm FeCO3 và FeS2 với tỉ lệ mol là 1:1 trong một bình kín chứa không khí dư với áp suất p1 atm. Sau khi các phản ứng xảy ra hoàn toàn đưa bình về nhiệt độ ban đầu thu được chất rắn duy nhất là Fe2O3 và áp suất khí trong bình lúc này là p2 atm. (thể tích các chất rắn không đáng kể và sau phản ứng lưu huỳnh ở mức oxi hóa +4). Mối liên hệ giữa p1 và p2 là:
A. p1 = p2
B. p1 = 2p2
C. 2p1 = p2
D. p1 = 3p2
Đáp án A
2FeCO3 + 1/2O2 → Fe2O3 + 2CO2
x x/4 x
4FeS2 + 11O2 → 2Fe2O3 + 8SO2
x 11x/4 2x
Số mol oxi mất đi = số mol CO2 và SO2 sinh ra nên p1 = p2
Đúng 0
Bình luận (0)
Có hỗn hợp A gồm 3 muối NH4HCO3, NaHCO3 và Ca(HCO3)2. Khi nung 48,8 gam hỗn hợp đó đến khối lượng không đổi thu được 16,2 bã rắn và hỗn hợp khí X. Nung X ở nhiệt độ 180 - 200°C, dưới áp suất khoảng 200 atm. Sau một thời gian đưa về nhiệt độ ban đầu ta thu được một chất rắn duy nhất và còn lại một chất khí Z có áp suất bằng áp suất của X. Xác định thành phần phần trăm khối lượng của Ca(HCO3)2 trong hỗn hợp ban đầu: A. 33,197% B. 25,62% C. 66,39% D. 46,2%
Đọc tiếp
Có hỗn hợp A gồm 3 muối NH4HCO3, NaHCO3 và Ca(HCO3)2. Khi nung 48,8 gam hỗn hợp đó đến khối lượng không đổi thu được 16,2 bã rắn và hỗn hợp khí X. Nung X ở nhiệt độ 180 - 200°C, dưới áp suất khoảng 200 atm. Sau một thời gian đưa về nhiệt độ ban đầu ta thu được một chất rắn duy nhất và còn lại một chất khí Z có áp suất bằng áp suất của X. Xác định thành phần phần trăm khối lượng của Ca(HCO3)2 trong hỗn hợp ban đầu:
A. 33,197%
B. 25,62%
C. 66,39%
D. 46,2%
Tóm tắt: 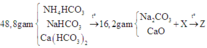
Gọi a; b; c lần lượt là số mol của NH4HCO3, NaHCO3 và Ca(HCO3)2
Ta có: 89a + 84b + 162c =48,8 (l)
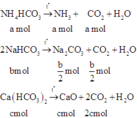
Khối lượng của hỗn hợp rắn là: 53b + 56c = 16,2 (2)
Hỗn hợp khí X gồm NH3 (a mol) và CO2 (a + b 2 + 2c)
⇒ n x = (2a + b 2 + 2c)
Khi X ở nhiệt độ 180 – 200°C, dưới áp suất khoảng 200 atm thì đây chính là phản ứng điều chế đạm urê nên ta có phản ứng:
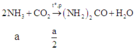
NH3 phản ứng với CO2 theo tỉ lệ 1:2 lượng khí Z còn lại chính là CO2 ⇒ n z = a 2 + b 2 . 2 c
Do sau phản ứng đưa về nhiệt độ ban đầu nên ta có:
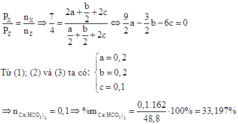
Đáp án A.
Đúng 0
Bình luận (0)
Trong một bình kín dung tích 56 lít (không đổi) chứa N2 và H2 theo tỷ lệ thể tích là 1:4. Ở 00C, áp suất 200 atm (xt Fe3O4). Nung nóng bình một thời gian sau đó đưa bình về nhiệt độ 00C thấy áp suất trong bình giảm 10% so với áp suất ban đầu. Lấy toàn bộ lượng NH3 trên thì có thể điều chế được bao nhiêu lít dd NH3 nồng độ 25% (d 0,907 g/ml) A. 0,1376 lít B. 2,838 lít C. 3,784 lít D. 3,4056 lít
Đọc tiếp
Trong một bình kín dung tích 56 lít (không đổi) chứa N2 và H2 theo tỷ lệ thể tích là 1:4. Ở 00C, áp suất 200 atm (xt Fe3O4). Nung nóng bình một thời gian sau đó đưa bình về nhiệt độ 00C thấy áp suất trong bình giảm 10% so với áp suất ban đầu.
Lấy toàn bộ lượng NH3 trên thì có thể điều chế được bao nhiêu lít dd NH3 nồng độ 25% (d = 0,907 g/ml)
A. 0,1376 lít
B. 2,838 lít
C. 3,784 lít
D. 3,4056 lít
Một lượng khí đựng trong một xilanh có pit tông chuyển động được. Lúc đầu, khí có thể tích 15 lít, nhiệt độ 27
°
C
và áp suất 2 atm. Khi pit tông nén khí đến thể tích 12 lít thì áp suất khí tăng lên tới 3,5 atm. Nhiệt độ của khí trong pit tông lúc này là A. 37,8
°
C
B. 147
°
C
C. 147 K D. 47,5
°
C
Đọc tiếp
Một lượng khí đựng trong một xilanh có pit tông chuyển động được. Lúc đầu, khí có thể tích 15 lít, nhiệt độ 27 ° C và áp suất 2 atm. Khi pit tông nén khí đến thể tích 12 lít thì áp suất khí tăng lên tới 3,5 atm. Nhiệt độ của khí trong pit tông lúc này là
A. 37,8 ° C
B. 147 ° C
C. 147 K
D. 47,5 ° C
Đáp án B.
Ta có: Trạng thái đầu: V 1 = 15 lít; p 1 = 2 atm; T 1 = 27 + 273 = 300 K.
Trạng thái sau: V 2 = 12 lít; p 2 = 3,5 atm; T 2 = ?
Áp dụng phương trình trang thái ta được:
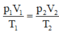
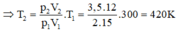
Suy ra t 2 = 420 – 273 = 147 ° C
Đúng 1
Bình luận (0)
Cho một chiết bình kín có thể tích không đổi. Khi đun nóng khí trong bình kín thêm
1
°
C thì áp suất khí tăng thêm 1/360 áp suất ban đầu. Xác định nhiệt độ ban đầu của khí? A.
87
°
C B.
360
°
C C. 17K D. 87K
Đọc tiếp
Cho một chiết bình kín có thể tích không đổi. Khi đun nóng khí trong bình kín thêm 1 ° C thì áp suất khí tăng thêm 1/360 áp suất ban đầu. Xác định nhiệt độ ban đầu của khí?
A. 87 ° C
B. 360 ° C
C. 17K
D. 87K
Cho một chiết bình kín có thể tích không đổi. Khi đun nóng khí trong bình kín thêm 1 ° C thì áp suất khí tăng thêm 1/360 áp suất ban đầu. Xác định nhiệt độ ban đầu của khí ?
A. 87 ° C
B. 360 ° C
C. 17 K
D. 87 K