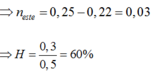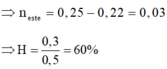Chia một lượng hỗn hợp hai ancol no, đơn chức thành hai phần bằng nhau:
- Phần 1 đem đốt cháy hoàn toàn thu được 2,24l CO2 (đktc).
- Phần 2 đem tách nước hoàn toàn thu được hỗn hợp hai anken.
Đốt cháy hoàn toàn hai anken thu được bao nhiêu gam nước?
A. 1,2 g
B. 1,8 g
C. 2,4 g
D. 3,6 g