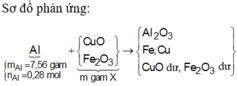
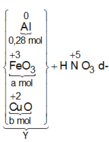
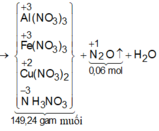
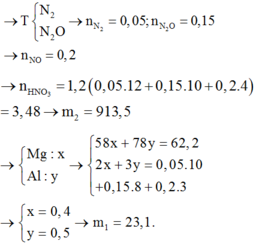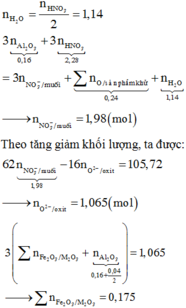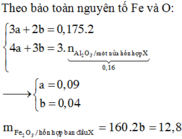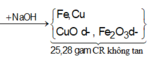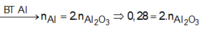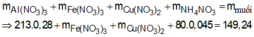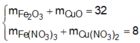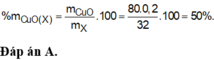Cho một luồng khí O2đi qua 24 gam Mg thu được 36,8 gam hỗn hợp rắn X. Cho X tác dụng hết với HNO3(vừa đủ ) thấy thoát ra 0,224 lít khí N2O(đktc). Khối lượng muối thu được sau phản ứng là m1 gam. Khối lượng HNO3đã dùng là m2gam. Tổng giá trị của m1+m2 là
A. 283,5
B. 285,3
C. 238,5
D. 253,8