Nhiệt phân hoàn toàn một lượng M(NO3)2 trong chân không (với M là kim loại) thu được 8 gam một oxit kim loại và 5,04 lít hỗn hợp khi X gồm NO2 và O2 (đo ở đktc). Khối lượng của hỗn hợp X là 10 gam. Kim loại M là
A. Mg.
B. Cu.
C. Fe.
D. Zn.
Nhiệt phân hoàn toàn R(NO3)2 (với R là kim loại) thu được 8 gam một oxit kim loại và 5,04 lít hỗn hợp khí X gồm NO2 và O2 (đo ở đktc). Khối lượng của hỗn hợp khí X là 10 gam. Muối R(NO3)2 là?
A.Mg(NO3)2.
B.Cu (NO3)2 .
C.Fe(NO3)2.
D. Zn(NO3)2.
Đáp ánC
Đặt ![]()
Ta có hệ 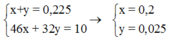
Bảo toàn nguyên tố N ta có
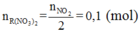
Bảo toàn khối lượng ta lại có:
![]()
Nhiệt phân hoàn toàn A(NO3)2 (với R là kim loại) trong chân không thu được 9,6 gam một oxit kim loại và 6,048 lít hỗn hợp khí X gồm NO2 và O2 (đo ở đktc). Khối lượng của hỗn hợp khí X là 12 gam. Xác định công thức của muối A(NO3)2
A. Mg(NO3)2.
B.Zn(NO3)2.
C.Cu(NO3)2
D.Fe(NO3)2.
n X = 6 , 048 22 , 4 = 0 , 27 m o l .
Đặt
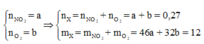
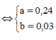

Cách 1: Áp dụng định luật bảo toàn khối lượng, không xét đến trong quá trình nhiệt phân A có thay đổi số oxi hóa hay không.Áp dụng định luật bảo toàn khối lượng ta có:
![]()
Bảo toàn nguyên tố N:
![]()

![]()
Vậy đáp án đúng là D.
Cách 2: Xét tỉ lệ mol giữa NO2 và O2 để tìm dạng phản ứng nhiệt phân của A(NO3)2 . Có
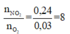
Khi đó trong quá trình nhiệt phân, A có sự thay đổi số oxi hóa từ +2 lên +3:
![]()
Quan sát 4 đáp án nhận thấy chỉ có Fe(NO3 )2 thỏa mãn.
Đáp án D.
Nhiệt phân hoàn toàn R N O 3 2 , thu được 8 gam oxit kim loại và 5,04 lít hỗn hợp khí X N O 2 v à O 2 . Khối lượng của hỗn hợp khí X là 10 gam. Khối lượng mol của muối R N O 3 2 là
A. 148.
B. 180.
C. 188.
D. 189.
Nhiệt phân hoàn toàn R(NO3)2 thu được 8 gam oxit kim loại và 5,04 lít hỗn hợp khí X. Khối lượng của hỗn hợp khí X là 10 gam. Công thức của muối nitrat đem nhiệt phân là:
A. Fe(NO3)2
B. Mg(NO3)2
C. Cu(NO3)2
D. Zn(NO3)2
Đáp án A
Vì nhiệt phân R(NO3)2 thu được oxit kim loại nên hỗn hợp khí X thu được gồm NO2 và O2.
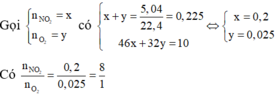
Do đó hóa trị của R trong muối và trong oxit là khác nhau. Căn cứ vào 4 đáp án ta được Fe(NO3)2.
Để tác dụng vừa đủ với m gam hỗn hợp X gồm Cr và kim loại M có hóa trị không đổi cần vừa đúng 2,24 lít hỗn hợp khí Y (đktc) gồm O2 và Cl2 có tỷ khối đối với H2 là 27,7 thu được 11,91 gam hỗn hợp Z gồm các oxit và muối clorua. Mặt khác, cho m gam hỗn hợp X tác dụng với một lượng dư dung dịch HNO3 đặc, nguội thu được 2,24 lít khí NO2 (đktc) là sản phẩm khử duy nhất. Các phản ứng xảy ra hoàn toàn. Kim loại M là:
A. Ca
B. Cu
C. Mg
D. Zn
Đáp án D
Có

m g X + HNO3 đặc nguội → 0,1 mol NO2
→ BTe a . n M = 0 , 1 m o l ( 2 )
Từ (1) và (2) suy ra:
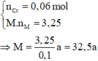
=> a = 2, M = 65 (M là Zn).
nung 37,6 gam một muối của kim loại X sau phản ứng kết thúc thu được m gam chất rắn Y là oxit bazơ của kim loại X. (trong Oxit X chiếm 80% về khối lượng) và 11,2 lít hỗn hợp khí Z gồm NO2 và O2 ở ĐKTC có tỉ khối so với H2 là 21,6.
a. Tính m
b. Xác định CTHH của X và Y
Hòa tan hoàn toàn m gam hỗn hợp E gồm Sn và một kim loại R (có hóa trị không đổi) trong lượng dư dung dịch HCl, thu được 5,04 lít khí H2 (đktc) và dung dịch chứa 36,27 gam muối. Mặt khác, để đốt cháy cũng m gam hỗn hợp E cần vừa đủ 3,696 lít O2 (đktc). Kim loại R là
A. Al
B. Zn
C. Ca
C. Ca
Gọi hóa trị của R là n và số mol Sn và R lần lượt là a và b mol
+/ Khi phản ứng với HCl :
Sn + HCl → SnCl2 + H2
R + nHCl → RCln + 0,5nH2
+/ Khi đốt trong oxi :
Sn + O2 → SnO2
2R + 0,5nO2 → R2On
=> Ta có : nH2 = a + 0,5nb = 0,225 mol
Và nO2 = a + 0,25nb = 0,165 mol
=> a = 0,105 mol ; nb = 0,24 mol
Có mmuối = 0,105.190 + 0,24/n . (R + 35,5n) = 36,27
=>R = 32,5n
=>Cặp n =2 ; R =65 (Zn) thỏa mãn
=>B
Một oxit kim loại có công thức MxOy chứa 27,59% oxi về khối lượng. Khử hoàn toàn oxit kim loại này bằng CO thu được 1,68 gam M. Hòa tan hết M trong một lượng dung dịch HNO3 đặc nóng, thu được 1,6128 lít hỗn hợp G gồm NO2 và N2O4 ở 1 atm; 54,6°C, có tỉ khối so với H2 là 34,5 và một dung dịch A chỉ chứa M(NO3)2. Hòa tan G vào dung dịch KOH dư trong điều kiện có không khí thu được dung dịch B, cho 24,05 gam Zn vào dung dịch B thu được hỗn hợp khí D. Thể tích hỗn hợp D (đktc) là:
A. 2,24 lít
B. 3,36 lít
C. 4,48 lít
D. 5,6 lít
Nung m gam hỗn hợp A gồm Mg, FeCO3, FeS, Cu(NO3)2 (trong A % khối lượng oxi là 47,818%) một thời gian (muối nitrat bị nhiệt phân hoàn toàn) thì thu được chất rắn B và 11,144 lít hỗn hợp khí gồm CO2, NO2, O2, SO2. B phản ứng hoàn toàn với HNO3 đặc nóng dư (thấy có 0,67 mol HNO3 phản ứng) thu được dung dịch C và 3,136 lít hỗn hợp X gồm NO2 và CO2 ( d x H 2 = 321 14 ). C tác dụng hoàn toàn với BaCl2 dư thấy xuất hiện 2,33 gam kết tủa. Biết các khí đo ở đktc. Giá trị gần nhất của m là?
A. 48
B. 33
C. 40
D. 42
Đáp án : D
Xét X : có nX = 0,14 mol ; MX = 321/7g
Áp dụng qui tắc đường chéo => nCO2 = 0,01 mol ; nNO2 = 0,13 mol
Kết tủa 2,33g chính là BaSO4 => nBaSO4 = nSO2 = 0,01 mol
Khi khí B + HNO3 :
4NO2 + O2 + 2H2O -> 4HNO3
,x -> 0,25x
=> nB = nSO2 + nCO2 + nNO2 + nO2
=> 0,495 = 0,01 + 0,01 + 0,13 + x + 0,25x
=> x = 0,276 mol
Bảo toàn nguyên tố :
,nFeCO3 = nCO2 = 0,01 ; nCu(NO3)2 = ½nNO2 = 0,203 mol
=> nO(X) = 3nFeCO3 + 6nCu(NO3)2 = 1,248 mol
Vì %mO = 47,818% => m = 41,76g