Cho 2,16 gam kim loại (hóa trị không đổi) vào cốc đựng 250 gam dung dịch Cu(NO3)2 3,76% màu xanh đến khi các phản ứng hoàn toàn, lọc bỏ phần không tan thu được dung dịch không màu có khối lượng 247,152 gam. Kim loại R là:
A. Mg
B. Ca
C. Al
D. Na
Cho 2,16 gam kim loại (hóa trị không đổi) vào cốc đựng 250 gam dung dịch Cu(NO3)2 3,76% màu xanh đến khi các phản ứng hoàn toàn, lọc bỏ phần không tan thu được dung dịch không màu có khối lượng 247,152 gam. Kim loại R là:
A. Mg.
B. Ca.
C. Al.
D. Na.


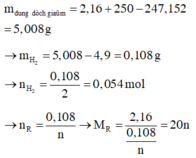
| n |
1 |
2 |
3 |
| M |
20 (Loại) |
40 (Ca) |
60 (Loại) |
Kim loại R là Ca.
Cho 2,16 gam kim loại R (hóa trị không đổi) vào cốc đựng 250 gam dung dịch Cu(NO3)2 3,76% màu xanh đến khi các phản ứng xảy ra hoàn toàn, lọc bỏ phần không tan thu được dung dịch không màu có khối lượng 247,152 gam. Kim loại R là
A. Ca.
B. Al.
C. Na.
D. Mg.
Đáp án A
Giả sử KL đó tác dụng được với nước.
nCu(OH)2 = nCu2+ = 0,05 mol
BTKL: mR + m dd Cu(NO3)2 = m Cu(OH)2 + m dd sau pư + mH2 => mH2 = 2,16+250-247,152-0,05.98 = 0,108 gam
=> nH2 = 0,054 mol
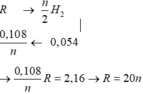
=> n = 2, R = 40 (Ca)
HS xét tiếp trường hợp R không phản ứng với H2O.
Cho 2,16 gam kim loại R (hóa trị không đổi) vào cốc đựng 250 gam dung dịch Cu(NO3)2 3,76% màu xanh đến khi các phản ứng xảy ra hoàn toàn, lọc bỏ phần không tan thu được dung dịch không màu có khối lượng 247,152 gam. Kim loại R là
A. Mg
B. Ca
C. Al
D. Na
Đáp án : B
Giả sử kim loại R có hóa trị không đổi x
+) TH1: R không phản ứng với H2O
2R à xCu
Do màu xanh dung dịch mất đi => Cu2+ hết
nCu2+ = 0,05mol => mR pứ = 64.0,05 – 2,848 = 0,353g = R. 0 , 1 x => R = 3,52x (Loai)
+) TH2 : R là kim loại kiềm hoặc kiềm thổ
R + xH2O à R(OH)x + ½ xH2
2R(OH)x + xCu2+ à xCu(OH)2 + 2Rx+
=> BTKL : mR + mdd muối đồng = mdd sau + mH2 + mCu(OH)2
(xnR = 2nH2) => x.nR = x. 2 , 16 R = 0,108 => R = 20x => x = 2 và R là Ca (M = 40)
giúp mình vs ạ
cho 2,16 g kim loại R (hóa trị không đổi) vào cốc đựng 250g dung dịch Cu(NO3)2 3,76% màu xanh đến khi các phản ứng xảy ra hoàn toàn ,lọc bỏ phần không tan thu được dung dịch không màu có khối lượng 247,152g.kim loại R là?
Đối với bài này ta chỉ cần tìm số mol của hidro là xong. BTKl ta đc mchấtkotan=2,16+250-247,125=5,008g nCu(NO3)2=0,05mol=nCu(OH)2 mchấtkotan=mCu(OH)2+mH2 suyra mH2=5,008-0,005*98=0,108g suyra nh2=0,054 biện luận nếu R hóa trị 2 thì nh2=nR=0,054 suy ra MR=2,16/0,05=40 suy ra là Canxi,các hóa trị khác biện luận tương tự bằng pp bảo toàn e
cho 2,16g kim loại loại R(hóa trị không đổi) vào cooc đựng 250g dd Cu(NO3)2 3,76% màu xanh đến khi các phản ứng xảy ra hoàn toàn, lọc bỏ phần không thu được dd không màu có khối lượng 247,152g, Tìm R
Hòa tan hoàn toàn 37,44 gam kim loại M (có hóa trị không đổi) vào dung dịch X chứa 84,6 gam Cu(NO3)2. Sau phản ứng hoàn toàn, lọc bỏ chất rắn, thu được dung dịch không màu có khối lượng giảm so với khối lượng của X là 7,62 gam. Kim loại M là:
A. Mg.
B. Ca.
C. K.
D. Be.
Hòa tan hoàn toàn 11,6 gam hỗn hợp A gồm Fe và Cu vào 87,5 gam dung dịch HNO3 50,4%, sau khi kim loại tan hết thu được dung dịch X và hỗn hợp khí B. Cho 500ml dung dịch KOH 1M vào dung dịch X thu được kết tủa Y và dung dịch Z. Lọc lấy Y rồi nung trong không khí đến khối lượng không đổi thu được 16,0 gam chất rắn. Cô cạn dung dịch Z được chất rắn T. Nung T đến khối lượng không đổi thu được 41,05 gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. Nồng độ phần trăm của Cu(NO3)2 trong dung dịch X gần nhất với giá trị nào sau đây?
A. 13,6%.
B. 11,8%.
C. 10,6%.
D. 20,2%.
Chọn đáp án C
Giả sử KOH tác dụng với X thì KOH hết ⇒ n KNO 3 = n KOH = 0 , 5 mol.
⇒ m KNO 3 = 0 , 5 x 101 = 50 , 5 gam gam > 41,05 gam ⇒ vô lí ⇒ KOH dư.
Đặt n KOH dư = x mol; n KNO 3 = y mol
![]()
Phản ứng:
![]()
Giải hệ có: x = 0,05 mol; y = 0,45 mol
![]()
Đặt n Fe = a mol; n Cu = b mol ⇒ m A = 56 a + 64 b = 11 , 6 gam.
Do KOH dư ⇒ kết tủa hết ion kim loại ⇒ nung T thì rắn gồm Fe2O3 và CuO.
⇒ mrắn = 41,05 = 0,5a × 160 + 80b. Giải hệ có: a = 0,15 mol; b = 0,05 mol.
Quy hỗn hợp B về N và O. Bảo toàn nguyên tố nitơ có nN spk = 0,7 – 0,45 = 0,25 mol.
![]()
⇒ dung dịch chứa ion Fe2+, Fe3+ và H+ hết.!
Bảo toàn nguyên tố hidro có n H 2 O = 0 , 7 ÷ 2 = 0 , 35 mol.
⇒ bảo toàn nguyên tố oxi có nO sk = 0,7 × 3 – 0,45 × 3 – 0,35 = 0,4 mol.
⇒ BTKL mdung dịch sau phản ứng = 11,6 + 87,5 – 0,25 × 14 – 0,4 × 16 = 89,2 gam.
![]()
Hòa tan hoàn toàn 11,6 gam hỗn hợp A gồm Fe và Cu vào 87,5 gam dung dịch HNO3 50,4%, sau khi kim loại tan hết thu được dung dịch X và hỗn hợp khí B. Cho 500ml dung dịch KOH 1M vào dung dịch X thu được kết tủa Y và dung dịch Z. Lọc lấy Y rồi nung trong không khí đến khối lượng không đổi thu được 16,0 gam chất rắn. Cô cạn dung dịch Z được chất rắn T. Nung T đến khối lượng không đổi thu được 41,05 gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. Nồng độ phần trăm của Cu(NO3)2 trong dung dịch X gần nhất với giá trị nào sau đây?
A. 13,6%.
B. 11,8%.
C. 10,6%.
D. 20,2%.

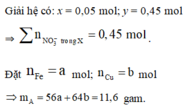
Do KOH dư ⇒ kết tủa hết ion kim loại ⇒ nung T thì rắn gồm Fe2O3 và CuO.
⇒ mrắn = 41,05 = 0,5a × 160 + 80b. Giải hệ có: a = 0,15 mol; b = 0,05 mol.
Quy hỗn hợp B về N và O. Bảo toàn nguyên tố nitơ có nN spk = 0,7 – 0,45 = 0,25 mol.

⇒ bảo toàn nguyên tố oxi có nO sk = 0,7 × 3 – 0,45 × 3 – 0,35 = 0,4 mol.
⇒ BTKL mdung dịch sau phản ứng = 11,6 + 87,5 – 0,25 × 14 – 0,4 × 16 = 89,2 gam.
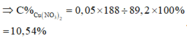
Đáp án C
Cho 4,58 gam hỗn hợp A gồm Zn, Fe và Cu vào cốc đựng 85 ml dung dịch C u S O 4 1M. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch B và kết tủa C. Nung C trong không khí đến khối lượng không đổi được 6 gam chất rắn D. Thêm dung dịch NaOH dư vào dung dịch B, lọc kết tủa thu được, rửa sạch rồi nung ở nhiệt độ cao đến khối lượng không đổi thu được 5,2 gam chất rắn E. Các phản ứng xảy ra hoàn toàn. % khối lượng mỗi kim loại trong hỗn hợp A (theo thứ tự Zn, Fe, Cu) là
A. 28,38%; 36,68% và 34,94%
B. 14,19%; 24,45% và 61,36%
C. 28,38%; 24,45% và 47,17%
D. 42,58%; 36,68% và 20,74%