Cấu hình electron lớp ngoài cùng của một ion là : 3s23p6. Số hiệu của nguyên tử có thể có của nguyên tố tạo nên ion đó là
A. 15, 16 hoặc 17.
B. 18, 19 hoặc 20.
C. 15, 16, 17, 19 hoặc 20.
D. 15, 16, 17, 18, 19 hoặc 20.
Cấu hình electron lớp ngoài cùng của một ion là : 3 s 2 3 p 6 . Số hiệu của nguyên tử có thể có của nguyên tố tạo nên ion đó là
A. 15,16 hoặc 17
B. 18,19 hoặc 20
C. 15,16,17,19 hoặc 20
D. 15,16,17,18,19 hoặc 20
Cho nguyên tử của các nguyên tố: X (Z = 11); Y (Z = 12); L (Z = 17); E (Z = 16); G (Z = 8); Q (Z = 9); T (Z = 18); M (Z = 19). Trường hợp nào sau đây chỉ gồm các nguyên tử và ion có cùng cấu hình electron?
A. X+ , Y2+ , G2- , L-
B. L- , E2+ , T , M+
C. X+ , Y2+ , G2- ,Q
D. Q-, E2+ , T , M+
Chọn đáp án B.
Dễ dàng nhìn thấy L- , E2- , T, M+ đều có cùng cấu hình electron của khí hiếm Ar.
Nguyên tử của nguyên tố X khi mất 2 electron lớp ngoài cùng thì tạo thành ion X2+ có cấu hình electron lớp ngoài cùng là 3p6. Số hiệu nguyên tử X là
A. 18
B. 20
C. 38
D. 40
Đáp án B
Hướng dẫn Cấu hình e của X: 1s22s22p63s23p64s2 => có 20e => Z=20
Nguyên tử của nguyên tố X khi mất 2 electron lớp ngoài cùng thì tạo thành ion X 2 + có cấu hình electron lớp ngoài cùng là 3 p 6 . Số hiệu nguyên tử X là
A. 18
B. 20
C. 38
D. 40
Cho các nguyên tố Q, T, Y, Z có số hiệu nguyên tử lần lượt là 13, 16, 19, 25. Ion nào sau đây không có cấu hình electron của khí hiếm
A. Q 3 +
B. T 2 -
C. Y +
D. Z 2 +
Viết cấu hình electron của các nguyên tử có số hiệu nguyên tử là: 7, 8, 10, 12, 13, 16, 17, 18, 19, 23, 24, 26, 29, 30, 35. Trong số các nguyên tử trên nguyên tử nào thuộc nguyên tố s, p, d, f? Nguyên tử nào là kim loại, phi kim, khí hiếm?
) Để giá trị của phân số không đổi thì ta phải xóa những số ở mẫu mà tổng của nó gấp 6 lần tổng của những số xóa đi ở tử. Khi đó tổng các số còn lại ở mẫu cũng gấp 6 lần tổng các số còn lại ở tử. Vì vậy đổi vai trò các số bị xóa với các số còn lại ở tử và mẫu thì ta sẽ có thêm phương án xóa. Có nhiều cách xóa, xin giới thiệu một số cách (số các số bị xóa ở mẫu tăng dần và tổng chia hết cho 6): mẫu xóa 12 thì tử xóa 2; mẫu xóa 18 thì tử xóa 3 hoặc xóa 1, 2; mẫu xóa 24 hoặc xóa 11, 13 thì tử xóa 4 hoặc xóa 1, 3; mẫu xóa 12, 18 hoặc 13, 17 hoặc 14, 16 thì tử xóa 5 hoặc 2, 3 hoặc 1, 4; mẫu xóa 12, 24 hoặc 11, 25 hoặc 13, 23 hoặc 14, 22 hoặc 15, 21 hoặc 16, 20 hoặc 17, 19 thì tử xóa 6 hoặc 1, 5 hoặc 2, 4 hoặc 1, 2, 3; mẫu xóa 18, 24 hoặc 17, 25 hoặc 19, 23 hoặc 20, 22 hoặc 11, 13, 18 hoặc 12, 13, 17 hoặc 11, 14, 17 hoặc 11, 15, 16 hoặc 12, 14, 16 hoặc 13, 14, 15 thì tử xóa 7 hoặc 1, 6 hoặc 2, 5 hoặc 3, 4 hoặc 1, 2, 4; ...
Các bạn hãy kể tiếp thử xem được bao nhiêu cách nữa?
Cấu hình electron của ion được thiết lập bằng cách thêm hoặc bớt electron, bắt đầu từ phân lớp ngoài cùng của cấu hình electron nguyên tử tương ứng. a. Viết cấu hình electron của Na+ và Cl-. b. Nguyên tử Cl nhận 1 electron để trở thành ion Cl-, electron này xếp vào AO thuộc phân lớp nào của Cl? AO đó là AO trống, chứa 1 hay 2 electron?
Cấu hình electron của ion được thiết lập bằng cách thêm hoặc bớt electron, bắt đầu từ phân lớp ngoài cùng của cấu hình electron nguyên tử tương ứng.
a) Viết cấu hình electron của Na+ và Cl-.
b) Nguyên tử Cl nhận 1 electron để trở thành ion Cl-, electron này xếp vào AO thuộc phân lớp nào của Cl? AO đó là AO trống, chứa 1 hay 2 electron?
a) Na (Z = 11) 1s22s22p63s1 ⇒ Na+: 1s22s22p6.
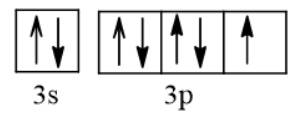
Cl (Z = 17) 1s22s22p63s23p5 ⇒ Cl-: 1s22s22p63s23p6.
b) Nguyên tử Cl nhận 1 electron để trở thành ion Cl-, electron này xếp vào AO thuộc phân lớp p của Cl. AO đó là AO chứa 1 electron.