Hòa tan hoàn toàn 13,00 gam Zn trong dung dịch HNO3 loãng dư thu được dung dịch X và 0,448 lít khí N2 (đktc). Khối lượng muối trong dung dịch X là:
A. 18,90 gam
B. 37,80 gam
C. 39,80 gam
D. 28,35 gam
Hòa tan hoàn toàn 13,00 gam Zn trong dung dịch HNO3 loãng dư thu được dung dịch X và 0,448 lít khí N2 (đktc). Khối lượng muối trong dung dịch X là:
A. 18,90 gam
B. 37,80 gam
C. 39,80 gam
D. 28,35 gam
Đáp án C
Ta có:
![]()
ne nhường = 2.nZn = 0,4 mol > ne nhận = 10.nN2 = 0,2 mol → phản ứng tạo thành NH4NO3.
![]()
(vì khi tạo thành NH4NO3: N + 8e → N)
Khối lượng muối trong dung dịch X là = 180.0,2 + 80.0,025 = 39,80 gam
Lưu ý: Đề bài không nói thu được khí X duy nhất nên có thể có muối NH4NO3 tạo thành.
Hòa tan hoàn toàn 13,00 gam Zn trong dung dịch HNO3 loãng dư thu được dung dịch X và 0,448 lít khí N2 (đktc). Khối lượng muối trong dung dịch X là:
A. 18,90 gam
B. 37,80 gam
C. 39,80 gam
D. 28,35 gam
Hỗn hợp X gồm Fe3O4 và CuO. Cho 29,2 gam X phản ứng với CO nung nóng, sau một thời gian thu được hỗn hợp rắn Y và hỗn hợp khí Z. Cho Z tác dụng với dung dịch Ba(OH)2 dư thu được 9,85 gam kết tủa. Hòa tan hết Y trong 150 gam dung dịch HNO3 63% đun nóng thu được dung dịch T và 4,48 lít NO2 (đktc) (sản phẩm khử duy nhất). Cho V (lít) dung dịch NaOH 1M vào dung dịch T, phản ứng hoàn toàn tạo ra kết tủa với khối lượng lớn nhất. Phần trăm khối lượng Fe3O4 và giá trị V là
A. 79,45% và 0,525 lít
B. 20,54% và 1,300 lít
C. 79,45% và 1,300 lít
D. 20,54% và 0,525 lít.
Cho hỗn hợp gồm 6,72 gam Mg và 0,8 gam MgO tác dụng hết với lượng dư dung dịch HNO3. Sau khi các phản ứng xảy ra hoàn toàn, thu được 0,896 lít một khí X (đktc) và dung dịch Y. Làm bay hơi dung dịch Y thu được 46 gam muối khan. Khí X là
A. NO2
B. N2O
C. N2
D. NO.
Hòa tan m(g) hỗn hợp Fe và Cu, trong đó Fe chiếm 40% khối lượng bằng dung dịch HNO3 thu được dung dịch X; 0,448 lít NO duy nhất (đktc) và còn lại 0,65m (g) kim loại. Khối lượng muối trong dung dịch X là:
A. 5,4g
B. 6,4g
C. 11,2g
D. 4,8g
Đáp án A
Ta có: mFe = 40%.m = 0,4m (g) → mCu = m - 0,4m = 0,6m (g)
Sau phản ứng còn 0,65m (g) kim loại > mCu = 0,6m (g)
Khối lượng Fe còn dư: 0,65m - 0,6m = 0,05m (g)
Vậy: mFe phản ứng = 0,4m - 0,05m = 0,35m (g)
Do Fe còn dư sau phản ứng nên tạo thành muối Fe2+
Quá trình nhường electron:
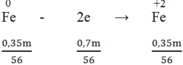
Quá trình nhận electron:
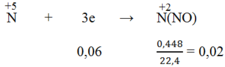
Áp dụng định luật bảo toàn electron, ta có:
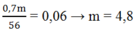
Ta có:
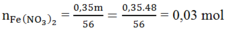
![]()
Hòa tan hoàn toàn 20,88 gam một oxit sắt bằng dung dịch H2SO4 đặc, nóng thu được dung dịch X và 3,248 lít khí SO2 (sản phầm khử duy nhất, ở đktc). Cô cạn dung dịch X, thu được m gam muối sunfat khan. Giá trị của m là:
A. 52,2
B. 48,4
C. 54,0
D. 58,0
Đáp án D
Ta có: = 0,145 mol
Quy đổi 20,88 g oxit sắt FexOy thành 20,88 g Fe và O
Gọi nFe = x mol; nO = y mol
Quá trình nhường electron:
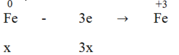
Quá trình nhận electron:
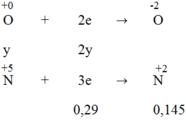
Áp dụng định luật bảo toàn electron, ta có:
3x = 2y + 0,29 → 3x - 2y = 0,29 (1)
Mặt khác: 56x + 16y = 20,88 (2)
Từ (1) và (2) → x = 0,29 và y = 0,29
Muối sinh ra là muối Fe2(SO4)3. Áp dụng ĐL bảo toàn nguyên tố ta có:
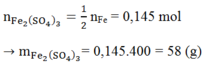
Hòa tan hoàn toàn 7.5 gam hỗn hợp gồm Mg và Al bằng lượng vừa đủ V lít dung dịch HNO3 1M. Sau khi các phản ứng kết thúc, thu được 0,672 lít N2 (đktc) duy nhất và dung dịch chứa 54,9 gam muối. Giá trị của V là?
nN2 = 0,03
m muối - mkim loại = mNO3
=> mNO3 = 54,9-7,5 = 47,4(g)
=> nN(trong muối) = nNO3 = \(\frac{47,4}{62}=0,764mol\)
BT nguyên tố N => nHNO3 = nN(trong muối) +nN2 = 0,764 + 0,03.2 = 0,824 mol
=> V = 0,824 (l)
Hòa tan hoàn toàn 7.5 gam hỗn hợp gồm Mg và Al bằng lượng vừa đủ V lít dung dịch HNO3 1M. Sau khi các phản ứng kết thúc, thu được 0,672 lít N2 (đktc) duy nhất và dung dịch chứa 54,9 gam muối. Giá trị của V là?
Hòa tan hoàn toàn 7.5 gam hỗn hợp gồm Mg và Al bằng lượng vừa đủ V lít dung dịch HNO3 1M. Sau khi các phản ứng kết thúc, thu được 0,672 lít N2 (đktc) duy nhất và dung dịch chứa 54,9 gam muối. Giá trị của V là?