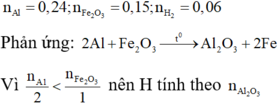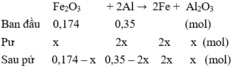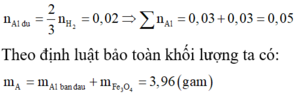Trộn 6,48 gam Al với 16 gam Fe2O3. Thực hiện phản ứng nhiệt nhôm được chất rắn A. Khi cho A tác dụng với dung dịch NaOH dư, có 1,344 lít H2 (đktc) thoát ra. Tính hiệu suất phản ứng nhiệt nhôm (hiệu suất được tính đối với chất thiếu).
A. 100%
B. 85%
C. 80%
D. 75%