So sánh tính chất hoá học của: Ankan với ankylbenzen
Cho ví dụ minh hoạ
So sánh tính chất hoá học của: Anken với ankin
Cho ví dụ minh hoạ
∗ So sánh tính chất hóa học anken và ankin:
- Giống nhau :
+ Cộng hiđro.
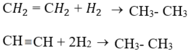
+ Cộng brom (dung dịch).
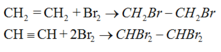
+ Cộng HX theo quy tắc Mac-côp-nhi-côp.
+ Làm mất màu dung dịch KMnO4.
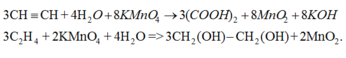
- Khác nhau :
+ Anken : Không có phản ứng thế bằng ion kim loại.
+ Ankin : Ank-1-in có phản ứng thế bằng ion kim loại.
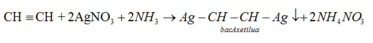
Câu 3.
a) Hãy lấy ví dụ minh hoạ các tính chất hoá học của đơn chất oxi. So sánh với tính chất hoá học của đơn chất hiđro? b) Hãy nêu phương pháp phân biệt các chất lỏng không mẫu sau: Dung dịch axit clohiđric, dung dịch nước vôi trong, dung dịch rượu cồn, dung dịch muối ăn.So sánh tính chất hóa học của:
a. anken và ankin
b.ankan và ankylbenzen
Cho ví dụ minh họa
Lời giải:
* So sánh tính chất hóa học anken và ankin:
- Giống nhau :
+ Cộng hiđro.
+ Cộng brom (dung dịch).
+ Cộng HX theo quy tắc Mac-côp-nhi-côp.
+ Làm mất màu dung dịch KMnO4.
- Khác nhau :
+ Anken : Không có phản ứng thế bằng ion kim loại.
+ Ankin : Ank-1-in có phản ứng thế bằng ion kim loại.
* So sánh tính chất hóa học ankan với ankylbenzen:
- Giống nhau :
+ Phản ứng thế (halogen).
+ Phản ứng oxi hóa .
- Khác nhau :
+ Ankan : Phản ứng tách .
+ Ankylbenzen : Phản ứng cộng.
So sánh tính chất hoá học của CO và CO 2 . Cho các thí dụ minh hoạ.
Giống nhau : CO và CO 2 là oxit.
Khác nhau : CO 2 là oxit axit : CO 2 + Ca OH 2 → CaCO 3 + H 2
CO là oxit trung tính.
CO 2 là chất oxi hoá : C + CO 2 → 2CO.
CO là chất khử: 2CO + O 2 → 2 CO 2
Viết phương trình hoá học minh hoạ cho tính chất hoá học của oxide base và oxide acid. Lấy magnesium oxide và sulfur dioxide làm ví dụ.
- Tính chất hoá học của oxide base:
+ Tác dụng với oxide acid: MgO + CO2 -> MgCO3
+ Tác dụng với dung dịch acid: MgO + 2HCl -> MgCl2 + H2O
+ Tác dụng với nước tạo dung dịch base: MgO là oxide base không tan nên không có phản ứng với nước.
- Tính chất hoá học của oxide acid:
+ Tác dụng với oxide base: SO2 + K2O -> K2SO3
+ Tác dụng với dung dịch base: SO2 + 2 KOH -> K2SO3 + H2O
+ Tác dụng với nước tạo dung dịch acid: \(SO_2+H_2O⇌H_2SO_3\)
So sánh tính chất hoá học của etylbenzen với stiren, viết phương trình hoá học của phản ứng để minh hoạ.
a. Giống nhau: đều phản ứng thế
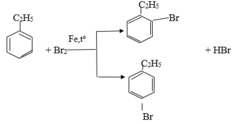
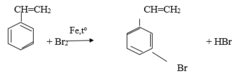
b. Khác nhau:
Etylbenzen có tính chất giống ankan
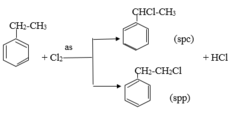
Stiren có tính chất giống anken
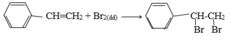
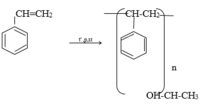
So sánh anken với ankan về đặc điểm cấu tạo và tính chất hóa học. Cho thí dụ minh họa.
- Về đặc điểm cấu tạo: Khác với ankan là phân tử chỉ chứa liên kết σ, phân tử anken còn có chứa 1 liên kết π kém bền, dễ gẫy.
- Do đó về tính chất hóa học cũng không giống với ankan là cho phản ứng thế là phản ứng đặc trưng, anken cho phản ứng cộng là phản ứng đặc trưng
Ví dụ:
C2H4 + H2→C2H6 (xúc tác : Ni)
C2H4 + Br2→C2H4Br2
C2H4 + HBr→C2H5Br
Ngoài ra anken còn cho phản ứng trùng hợp phản ứng làm mất màu dung dịch thuốc tím.
Ví dụ :
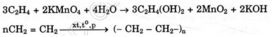
So sánh tính chất hoá học của hai dạng thù hình. Dẫn ra PTHH để minh hoạ.
So sánh tính chất hoá học của oxi và ozon
| Oxi | Ozon |
a. Tác dụng với kim loại Tác dụng với hầu hết kim loại (trừ Ag, Au và Pt) → oxit. Các phản ứng thường xảy ra ở nhiệt độ cao. 2Mg + O 2 → 2MgO 3Fe + O 2 → Fe 3 O 4 b. Tác dụng với phi kim - Oxi phản ứng với hầu hết các phi kim (trừ halogen) tạo thành oxit axit hoặc oxit không tạo muối. - Các phản ứng thường xảy ra ở nhiệt độ cao. S + O 2 → S O 2 C + O 2 → C O 2 2C + O 2 → 2CO N2 + O 2 c. Tác dụng với hợp chất có tính khử 2CO + O 2 → 2C O 2 4Fe S 2 + 11 O 2 → 2 Fe 2 O 3 + 8S O 2 |
Có tính oxi hóa mạnh hơn Oxi: O 3 + 2KI + H 2 O → 2KOH + I 2 + O 2 2Ag + O 3 → Ag 2 O + O 2 (phản ứng xảy ra ngay ở nhiệt độ thường). |
Làm thế nào để so sánh độ hoạt động hoá học mạnh hay yếu của phi kim ? Cho thí dụ minh hoạ.
Mức độ hoạt động hoá học mạnh, yếu của phi kim thường được xem xét qua khả năng phản ứng với hiđro hoặc với kim loại. Thí dụ :
H 2 + F 2 → bóng tối 2HF
H 2 + Cl 2 → t ° 2HCl
F hoạt động hóa học mạnh hơn Cl.