Điện phân dung dịch muối MCln bằng dòng điện 5A, điện cực trơ, sau 21 phút 27 giây ngừng điện phân, thấy trên catot sinh ra 2,1335 gam kim loại M. Xác định tên kim loại M
A. Cu
B. Fe
C. Mg
D. Zn
Điện phân (điện cực trơ) dung dịch muối sunfua của một kim loại hóa trị II với dòng điện cường độ 3A. Sau khi 1930 giây điện phân thấy khối lượng catot tăng 1,92 gam. Xác định tên kim loại.
Theo định luật Faraday ta có khối lượng chất thoát ra ở điện cực là :
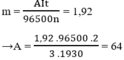
Trong đó A là nguyên tử khối
A = 64 ⇒ A là Cu
điện phân dung dịch muối clorua của kim loại hoá trị 2 với dòng điện cường độ 5A sau 1800 giây, thấy khối lượng catot tăng 3,03 gam . a) xác định kim loại đó b) viết sơ đồ điện phân dung dịch muối trên
a) Gọi CTHH của muối đó là XCl2
X+2 + 2e --> X
Có \(m=\dfrac{AIt}{nF}=\dfrac{M_X.5.1800}{2.96500}\)
=> \(M_X=65\left(Zn\right)\)
b)
Ở catot: Zn2+ + 2e --> Zn
Ở anot: 2Cl- --> Cl2 + 2e
\(ZnCl_2\underrightarrow{đpdd}Zn+Cl_2\)
Điện phân (điện cực trơ) dung dịch muối sunfat của một kim loại hoá trị II với cường độ dòng điện 3A, sau 1930 giây thấy khối lượng catot tăng 1,68 gam. Tên kim loại là
A. Fe
B. Cu
C. Al
D. Ni
Điện phân dung dịch CuCl2, điện cực trơ bằng dòng điện 5A trong 45 phút 20 giây. Khối lượng kim loại sinh ra trên catot và thể tích khí sinh ra ở anot (ở đktc) lần lượt bằng:
A. 4,512 g và 3,1584 lít
B. 4,512 g và 1,5792 lít
C. 2,256 g và 3,1584 lít
D. 2,256 g và 1,5792 lít
Đáp án B.
PT điện phân: CuCl2 → đ p d u n g d ị c h Cu + Cl2↑
Áp dụng công thức có:
mCu = 64 x 5 x 2720 2 x 96500 = 4,512 g → n Cl 2 = nCu = 4 , 512 64 = 0,0705 mol
V Cl 2 = 0,0705 × 22,4 = 1,5792 lít
Điện phân 100 gam dung dịch MSO4 32,2% (M là kim loại có hóa trị không đổi) bằng dòng điện một chiều có cường độ 5A (điện cực trơ, hiệu suất điện phân 100%, các khí sinh ra không tan trong dung dịch). Sau thời gian t giây, nước chưa bị điện phân đồng thời ở hai điện cực và tại catot thu được 10,4 gam kim loại M. Sau thời gian 2t giây, tổng thể tích khí thoát ra ở cả hai điện cực là 6,272 lít (đktc). Giá trị của t là
A. 6948.
B. 5790.
C. 6176.
D. 7720.
Điện phân dung dịch CuCl2, điện cực trơ bằng dòng điện 5A trong 45 phút 20 giây. Tính khối lượng kim loại sinh ra ở Catot và V lít (đktc) khí sinh ra ở Anot.
A. 4,512g
B. 4,5g
C. 4,6g
D. 4,679g
Điện phân với điện cực trơ, cường độ dòng điện không đổi dung dịch muối nitrat của một kim loại M (có hóa trị không đổi). Sau thời gian t giây thấy khối lượng dung dịch giảm 6,96 gam và tại catot chỉ thu được a gam kim loại M. Sau thời gian 2t giây khối lượng dung dịch giảm 11,78 gam và tại catot thoát ra 0,224 lít khí (đktc). Giá trị của a là:
A. 8,64
B. 6,40
C. 6,48
D. 5,60
Điện phân dung dịch hỗn hợp gồm CuCl2, CuSO4 và KCl (điện cực trơ, màng ngăn xốp), cường độ dòng điện không đổi. Trong thời gian t giây đầu tiên, thu được a mol khí ở anot và m gam kim loại ở catot. Điện phân thêm t giây tiếp sau đó thì ngừng điện phân, thu được thêm 0,225 mol khí ở cả hai điện cực và 0,8m gam kim loại ở catot. Dung dịch sau điện phân hòa tan tối đa 8 gam CuO. Giá trị của m là
A. 17,6
B. 16,0
C. 19,2
D. 12,8
Điện phân dung dịch muối MCl n với điện cực trơ. .Khi ở catot thu được 16 gam kim loại M thì ở anot thu được 5,6 lít (đktc). Kim loại M là
A. Mg
B. Cu
C. Ca
D. Zn