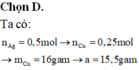Cho a gam hỗn hợp bột gồm Ni và Cu vào dung dịch AgNO3 (dư). Sau khi kết thúc phản ứng thu được 54g chất rắn. Mặt khác cũng cho a gam hỗn hợp trên vào dung dịch CuSO4 (dư). Sau khi kết thúc phản ứng thu được chất rắn có khối lượng (a + 0,5) gam. Giá trị của a là:
A.15,5.
B. 42,5g.
C.33,7g.
D. 53,5g.