Có các nguyên tố hóa học: Cr (Z = 24), Fe (Z = 26), P (Z = 15), Al (Z =13). Nguyên tố mà nguyên tử của nó có số electron độc thân lớn nhất ở trạng thái cơ bản là
A. P
B. Al
C. Cr
D. Fe
Có các nguyên tố hóa học: Cr (Z = 24), Fe (Z = 26), P (Z = 15), Al (Z = 13). Nguyên tố mà nguyên tử của nó có số electron lớp ngoài cùng lớn nhất ở trạng thái cơ bản là
A. Al.
B. Fe.
C. Cr.
D. P.
Câu 1: Một nguyên tử X có tổng số electron ở các phân lớp s là 6 và tổng số electron ở lớp ngoài cùng cũng là 6, cho biết X là nguyên tố hóa học nào sau đây?
A. O (Z = 8). B. S (Z = 16). C. Fe (Z = 26). D. Cr (Z = 24).
Cho số hiệu nguyên tử của: Al (Z = 13); Be (Z = 4); Ca (Z = 20); Cr (Z = 24); Fe (Z = 26); Cu (Z = 29). Số nguyên tố kim loại nhóm B (kim loại chuyển tiếp) trong dãy trên là
A. 6.
B. 5.
C. 4.
D. 3.
Cho số hiệu nguyên tử của: Al (Z = 13); Be (Z = 4); Ca (Z = 20); Cr (Z = 24); Fe (Z = 26); Cu (Z = 29). Số nguyên tố kim loại nhóm B (kim loại chuyển tiếp) trong dãy trên là
A. 6.
B. 5.
C. 4.
D. 3.
Đáp án D
+ Kim loại chuyển tiếp là kim loại có electron cuối cùng điền vào phân lớp d, f.
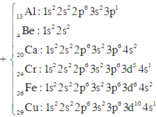
=> có 3 kim loại chuyển tiếp là Cr, Fe, Cu.
Cho số hiệu nguyên tử của: Al (Z = 13); Be (Z = 4); Ca (Z = 20); Cr (Z = 24); Fe (Z = 26); Cu (Z = 29). Số nguyên tố kim loại nhóm B (kim loại chuyển tiếp) trong dãy trên là
A. 6.
B. 5.
C. 4.
D. 3.
Đáp án D.
3.
Cr (Z = 24); Fe (Z = 26); Cu (Z = 29).
Ở trạng thái cơ bản:
- Phân lớp electron ngoài cùng của nguyên tử nguyên tố X là np2n+1.
- Tổng số electron trên các phân lớp p của nguyên tử nguyên tố Y là 7.
- Số hạt mang điện trong nguyên tử nguyên tố Z nhiều hơn số hạt mang điện trong nguyên tử nguyên tố X là 20 hạt. Nhận xét nào sau đây là sai? ( biết Z = 7 là F; Z = 17 là Cl; Z - 11 là Na; Z = 12 là Mg; Z = 13 là Al; Z = 19 là K)
A. Số oxi hóa cao nhất của X trong hợp chất là +7
B. Oxit và hiđroxit của Y có tính lưỡng tính
C. Độ âm điện giảm dần theo thứ tự X, Y, Z
D. Nguyên tố X và Y thuộc 2 chu kì kế tiếp
Chọn A.
- Y có cấu hình e là : 1s22s22p63s23p1. Y là Al.
- Với X, do ep= 2n+1 ≤ 6 và 2≤ n (n=2 trở lên mới có phân lớp p)nên n=2
→ X có cấu hình e là : 1s22s22p5. X là F. Số oxi hóa cao nhất của F trong hợp chất là -1.
Cho các nguyên tử: Al (Z = 13); S (Z = 16); O (Z =8); Fe (Z = 26); Cu (Z = 29); Zn (Z = 30); Cl (Z =
17); K (Z = 19); Br (Z = 35), Ne (Z = 10).
a. Viết cấu hình electron của các nguyên tử trên.
b. Cho biết nguyên tố nào thuộc nguyên tố s , p , d , f ? Vì sao?
c. Xác định kim loại, phi kim, khí hiếm?
Al : 1s22s22p63s23p1 ( kim loại vì lớp e ngoài cùng có 3e)
S : 1s22s22p63s23p4 ( phi kim vì lớp e ngoài cùng có 6e )
O : 1s22s22p4 ( phi kim vì lớp e ngoài cùng có 6e )
Fe : 1s22s22p63s23p63d64s2 ( kim loại vì lớp e ngoài cùng có 2e )
Cu : 1s22s22p63s23p63d104s1 ( kim loại vì lớp e ngoài cùng có 1e )
Zn : 1s22s22p63s23p63d104s2 ( kim loại vì lớp e ngoài cùng có 2e )
Cl : 1s22s22p63s23p5 ( kim loại vì lớp e ngoài cùng có 7e )
K : 1s22s22p63s23p64s1 ( kim loại vì lớp e ngoài cùng có 1e )
Br : 1s22s22p63s23p63d104s24p5 (kim loại vì lớp e ngoài cùng có 7e )
Ne : 1s22s22p6 ( khí hiếm vì lớp e ngoài cùng có 8e )
- Nguyên tố s : K ( e cuối cùng điền vào phân lớp s )
- Nguyên tố p : O, Ne, S, Cl, Br, Al ( e cuối cùng điền vào phân lớp p )
- Nguyên tố d : Fe, Cu, Zn ( e cuối cùng điền vào phân lớp d )
Nguyên tố Cl (Z = 17) có số electron độc thân ở trạng thái cơ bản là
A. 7
B. 5
C. 1
D. 3
Đáp án : C
Cấu hình e : 1s22s22p63s23p5 có 1 e độc thân
hãy xác định vị trí trong hệ thống tuần hoàn (số thứ tự, chu kỳ, nhóm)cho các nguyên tố sau
a. Be(Z=4); Al(Z=13); Fe(Z=26)
b. nguên tố Y có tổng số e của các phân lớp p là 11
c.Nguyên tử của nguyên tố R có 3e ở phân lớp 3d
Na(Z=11) 1s2 2s2 2p6 3s1 thuộc ô thứ 11, chu kì 3, nhóm IA
Al(Z=13) 1s2 2s2 2p6 3s2 3p1 thuộc ô thứ 13, chu kì 3, nhóm IIIA
S(Z=16) 1s2 2s2 2p6 3s2 3p4 thuộc ô thứ 16, chu kì 3
Nhóm VIA
Cl(Z=17) 1s2 2s2 2p6 3s2 3p5 thuộc ô thứ 17, chu kì 3,
Nhóm VIIA