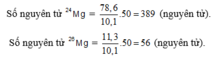Agon có ba đồng vị có số khối lần lượt là 36, 38 và A. Thành phần phần tram số nguyên tử của các đồng vị tương ứng bằng: 0,34% ; 0,06% ; 99,60%. Nguyên tử khối trung bình của agon là 39,98. Giá trị của A là
A. 40
B. 37
C. 35
D. 41
Biết rằng nguyên tố agon có ba đồng vị khác nhau, ứng với số khối 36; 38 và A. Phần trăm các đồng vị tương ứng lần lượt bằng : 0,34% ; 0,06% và 99,6%. Số khối của đồng vị A của nguyên tố agon là ? biết rằng nguyên tử khối trung bình của agon bằng 39,98
A. 37
B. 39
C. 40
D. 41
Câu 6. Biết rằng nguyên tố agon có ba đồng vị khác nhau, ứng với số khối 36; 38 và A. Phần trăm các đồng vị tương ứng lần lượt bằng : 0,34% ; 0,06% và 99,6%.
a) Tính số khối của đồng vị A của nguyên tố agon, biết rằng nguyên tử khối trung bình của agon bằng 39,98
b) Tính thể tích của 12 gam aggron (đktc)
Nguyên tố Agon có ba đồng vị khác nhau ứng với số khối 36, 38 và A3. % các đồng vị tương ứng lần lượt bằng 0,34%; 0,06% và 99,6%. Biết rằng nguyên tử khối trung bình của Agon bằng 39,985. Số khối A3 của nguyên tố Agon là?
A. 41
B. 39
C. 40
D. 42
Nguyên tố Argon có 3 loại đồng vị có số khối bằng 36; 38 và A. Phần trăm số nguyên tử tương ứng của 3 đồng vị lần lượt bằng 0,34%; 0,06% và 99,6%. Biết 125 nguyên tử Ar có khối lượng 4997,5 đvc. Số khối A của đồng vị thứ 3 là:
A. 40
B. 40,5
C. 39
D. 39,8
Đáp án A.
Nguyên tử khối trung bình của Ar: 4997,5:125=39.98(u)
Ta có phương trình:
A = 0 , 34 . 36 + 0 , 06 . 38 + 99 , 6 . A 100 = 39 , 98 ⇒ A = 40 ( u )
Biết rằng nguyên tố agon có ba đồng vị khác nhau, ứng với số khối 36 ,38 và A . Phần trăm các đồng vị tương ứng lần lượt bằng : 0,34 %, 0,06%, và 99,6% .
Tính khối lượng đồng vị A của nguyên tố agon , biết rằng nguyên tử khối trung bình của agon bằng 38,98
Gọi số khối của đồng vị A của nguyên tố agon là X
Ta có \(\overset{-}{A}\)Ar = 36 . \(\dfrac{0,34}{100}\) + 38 . \(\dfrac{0,06}{100}\) + X . \(\dfrac{99,6}{100}\) = 38,98
=> X = 40
Nguyên tử Mg có ba đồng vị ứng với thành phần phần trăm về số nguyên tử như sau

Giả sử trong hỗn hợp nói trên có 50 nguyên tử M 25 g , thì số nguyên tử tương ứng của hai đồng vị M 24 g và M 26 g lần lượt là
A. 389 và 56
B. 56 và 389
C. 495 và 56
D. 56 và 495
A
Giả sử trong hỗn hợp nói trên có 50 nguyên tử M 25 g , thì số nguyên tử tương ứng của 2 đồng vị còn lại là :
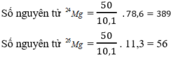
Các đồng vị của hiđro tồn tại trong tự nhiên chủ yếu là H 1 2 H 1 1
Đồng vị thứ ba H 1 3 có thành phần không đáng kể. Coi các đồng vị trên có nguyên tử khối tương ứng là 1 và 2 ; nguyên tử khối trung bình của hiđro tự nhiên là 1,008. Hãy tính thành phần phần trăm số nguyên tử của hai đồng vị H 1 2 H 1 1
Gọi x là thành phần phần trăm của H 1 thành phần phần trăm của H 1 2 sẽ là 100 –x
![]()
Giải ra ta được: x = 99,2.
Kết quả:thành phần : H 1 1 là 99,2%
H 1 2 là 0.8%
Trong tự nhiên Fe có 2 đồng vị là 55Fe và 56Fe. Nguyên tử khối trung bình của sắt bằng 55,85. Thành phần phần trăm tương ứng của 2 đồng vị lần lượt là:
A. 85 và 15
B. 42,5 và 57,5
C. 15 và 85
D. 57,5 và 42,5
Đáp án C
Gọi phần trăm khối lượng của đồng vị 55Fe, 56Fe lần lượt là x, y
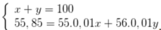
=>
Nguyên tử Mg có ba đồng vị ứng với thành phần phần trăm về số nguyên tử như sau:

Giả sử trong hỗn hợp nói trên có 50 nguyên tử 25Mg, thì số nguyên tử tương ứng của hai đồng vị 24, 26 lần lượt là bao nhiêu?
A. 48 và 52
B. 56 và 389
C. 389 và 56
D. 52 và 48
Đáp án C.
Ta có:
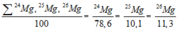
Giả sử trong hỗn hợp nói trên có 50 nguyên tử 25Mg, thì số nguyên tử tương ứng của 2 đồng vị còn lại là: