Cho phản ứng: N2+ 3 H2 ⇌ 2 NH3
Sau một thời gian, nồng độ các chất như sau: [N2]= 2,5 mol/l; [H2]= 1,5 mol/l; [NH3]= 2 mol/l. Nồng độ ban đầu của N2 và H2 lần lượt là:
A. 2,5M và 4,5 M
B. 3,5 M và 2,5M
C. 1,5M và 3,5M
D. 3,5M và 4,5M
Người ta cho N 2 và H 2 vào trong bình kín dung tích không đổi và thực hiện phản ứng:
N 2 + 3 H 2 ⇄ 2 N H 3
Sau một thời gian, nồng độ các chất trong bình như sau: N 2 = 2 M ; H 2 = 3 M ; N H 3 = 2 M . Nồng độ mol/l của N 2 và H 2 ban đầu lần lượt là
A. 3 và 6.
B. 2 và 3.
C. 4 và 8.
D. 2 và 4.
Thực hiện phản ứng tổng hợp amoniac N 2 + 3 H 2 ⇄ x t , t ° 2 N H 3 . Nồng độ mol ban đầu của các chất như sau : N 2 = 1 m o l / l ; H 2 = 1 , 2 m o l / l . Khi phản ứng đạt cân bằng nồng độ mol của N H 3 = 0 , 2 m o l / l . Hiệu suất của phản ứng là
A. 43%
B. 10%
C. 30%
D. 25%
Thực hiện phản ứng tổng hợp amoniac: N2 + 3H2 -> 2NH3 . ∆rH0298 <0
Nồng độ mol ban đầu của các chất như sau: [N2] = 0,5 mol/l; [H2] = 0,6 mol/l. Khi phản ứng đạt cân bằng nồng độ mol của [NH3] = 0,1 mol/l.
a/ Tính hằng số cân bằng của phản ứng ?
b/ Nêu các biện pháp tác động lên hệ cân bằng để tăng hiệu suất tổng hợp NH3 ?a)Tại tđ cân bằng:
\(\left[N_2\right]=0,5-\dfrac{1}{2}.0,1=0,5-0,05=0,45\left(M\right)\)
\(\left[H_2\right]=0,6-\dfrac{3}{2}.0,1=0,6-0,15=0,45\left(M\right)\)
\(\Rightarrow k_c=\dfrac{\left[NH_3\right]^2}{\left[N_2\right].\left[H_2\right]^3}=\dfrac{0,1^2}{0,45.0,45^3}\approx0,244\)
b) Để tăng H tổng hợp \(NH_3\), chúng ta có thể:
- Tăng P bằng cách giảm V (chọn P phù hợp)
- Giảm nhiệt độ của hệ ( chọn nhiệt độ phù hợp)
- Thêm \(N_2;H_2\)
Ở một nhiệt độ nhất định, phản ứng thuận nghịch N 2 ( k ) + 3 H 2 ( k ) ⇔ 2 NH 3 ( k ) đạt trạng thái cân bằng khi nồng độ của các chất như sau.[H2] = 2,0 mol/lít.[N2]=0,01 mol/lít. [NH3] = 0,4 mol/lít. Nồng độ ban đầu của H2 là.
A. 2,6 M.
B. 1,3 M.
C. 3,6 M
D. 5,6 M.
Thực hiện phản ứng tổng hợp amoniac :
N 2 + 3 H 2 ↔ 2 NH 3
Nồng độ mol ban đầu của các chất như sau :
[ N 2 ] = 1 mol/l ; [ H 2 ] = 1,2 mol/l
Khi phản ứng đạt cân bằng nồng độ mol của [ NH 3 ] = 0,2 mol/1. Tính hiệu suất của phản ứng tổng hợp amoniac.
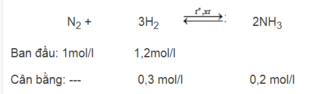
Theo PTHH thì 1 mol N 2 cần 3 mol H 2 . Ở đây chỉ có 1,2 mol H 2 , vì H 2 thiếu nên tác dụng hết. Hiệu suất phải tính theo lượng chất tác dụng hết. Số mol H 2 đã tác dụng là 0,3 mol.
Vậy h = (0,3 : 1,2). 100 = 25
Đáp số : h = 25%.
Ở một nhiệt độ nhất định, phản ứng thuận nghịch N 2 ( k ) + 3 H 2 ( k ) ⇔ 2 NH 3 ( k ) đạt trạng thái cân bằng khi nồng độ của các chất như sau.[H2] = 2,0 mol/lít.[N2]=0,01 mol/lít. [NH3] = 0,4 mol/lít. Hằng số cân bằng ở nhiệt độ đó là?
A. 2.
B. 3
C. 5
D. 7
Ammonia (NH3) được điều chế bằng phản ứng: N2(g)+3H2(g) 2NH3(g) .Ở t độ C: nồng độ mol ban đầu của [N2] =1 M, [H2] = 1, 2M khi ở trạng thái cân bằng là: [NH3] = 0, 2 M. Hiệu suất của phản ứng là
A. 25%
B. 43%.
C. 30%
D. 10%.
`1>{1,2}/3->H` tính theo `H_2.`
Tại TTCB: `[H_2]=3/{2}[NH_3]=0,3M`
`->C_{H_2\ pu}=1,2-0,3=0,9M`
`->H={0,9}/{1,2}.100\%=75\%`
Không có đáp án đúng.
Khi phản ứng .N2 (k) + 3H2 (k) ⇄ 2NH3 (k) đạt đến trạng thái cân bằng thì hỗn hợp khí thu được có thành phần. 1,5
mol NH3, 2 mol N2 và 3 mol H2. Vậy số mol ban đầu của H2 là.
A. 3 mol
B. 4 mol
C. 5,25 mol
D. 4,5 mol
Đáp án C.
N2 (k) + 3H2 (k) ⇄ t o , x t , p 2NH3 (k)
Cân bằng: 2 3 1,5 (mol)
phản ứng : 0,75 2,25 1,5
ban đầu: 2,75 5,25 0
Nén 2 mol N2 và 8 mol H2 vào bình kín có thể tích 2 lít (chứa sẵn chất xúc tác với thể tích không đáng kể) và giữ cho nhiệt độ không đổi. Khi phản ứng trong bình đạt tới trạng thái cân bằng, áp suất các khí trong bình bằng 0,8 lần áp suất lúc đầu (khi mới cho vào bình, chưa xảy ra phản ứng).
Nồng độ của khí NH3 tại thời điểm cân bằng là giá trị nào trong số các giá trị sau?
A. 0,5M
B. 1M
C. 2M
D. 4M