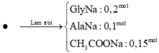
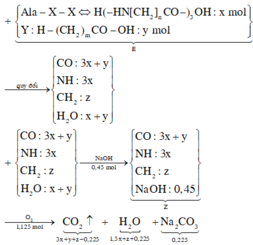
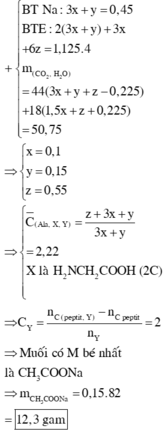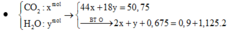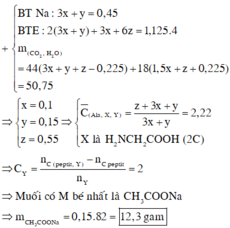X là amino axit có công thức , Y là axit cacboxylic no, đơn chức, mạch hở. Cho hỗn hợp E gồm peptit Ala-X-X và Y tác dụng vừa đủ với 450 ml dung dịch NaOH 1M, thu được m gam muối Z. Đốt cháy hoàn toàn Z cần 25,2 lít khí O 2 (đktc), thu được N 2 , N a 2 C O 3 và 50,75 gam hỗn hợp gồm C O 2 v à H 2 O . Khối lượng của muối có phân tử khối nhỏ nhất trong Z là
A. 29,10 gam.
B. 14,55 gam.
C. 12,30 gam.
D. 26,10 gam.