Điều chế NH3 từ hỗn hợp gồm N2 và H (tỉ lệ mol 1:3). Tỉ khối hỗn hợp trước so với hỗn hợp sau phản ứng là 0,6. Hiệu suất phản ứng là
Điều chế NH3 từ hỗn hợp gồm N2 và H2 (tỉ lệ mol 1:3). Tỉ khối hỗn hợp trước so với hỗn hợp sau phản ứng là 0,9. Hiệu suất phản ứng là:
A. 20%
B. 30%
C. 40%
D. 50%
Đáp án A

Tỉ khối hỗn hợp trước so với hỗn hợp sau phản ứng là 0,9.
→Khối lượng mol của hỗn hợp khí sau phản ứng là 8,5 : 0,9=85/9 (g/mol)

Điều chế NH3 từ hỗn hợp gồm N2 và H2 (tỉ lệ mol tương ứng là 1 : 3). Tỉ khối của hỗn hợp trước so với hỗn hợp sau phản ứng là 0,9. Hiệu suất phản ứng là
A. 25%.
B. 60%.
C. 70%.
D. 20%.
Đáp án D
+ B ả n c h ấ t p h ả n ứ n g : N 2 ( k h í ) + 3 H 2 ( k h í ) ⇆ p, xt, t o 2 N H 3 ( k h í ) ⇒ S a u p h ả n ứ n g n k h í g i ả m = 0 , 5 n k h í t h a m g i a s a u p h ả n ứ n g . + C h ọ n n H 2 = 3 ; n N 2 = 1 n H 2 p ư = 3 x ; n N 2 p ư = x ⇒ n 1 = n t p ¨ o = 4 n 2 = n s p ư = n 1 + n k h í g i ả m = 4 - 2 x + B T K L : m 1 = m 2 ⇒ n 1 M ¯ 1 = n 2 M ¯ 2 ⇒ n 2 n 1 = M ¯ 1 M ¯ 2 ⇒ 4 - 2 x 4 = 0 , 9 ⇒ x = 0 , 2 . ⇒ H = 20 %
Điều chế N H 3 từ hỗn hợp hồm N 2 v à H 2 (tỉ lệ 1 : 3) . Tỉ khối hỗn hợp trước so với hỗn hợp sau phản ứng là 0,9. Hiệu suất phản ứng là
A. 25%.
B. 40%.
C. 10%.
D. 20%.
Chọn D
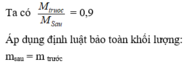
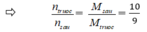
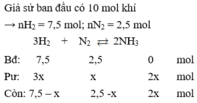
(Do ban đầu số mol N2 : H2 = 1 : 3 → hiệu suất tính theo H2 hoặc N2)
Sau phản ứng n = nH2 + nN2 + nNH3 = 7,5 - 3x + 2,5 – x + 2x = 10 – 2x = 9
→ x = 0,5 ⇒ H% = (0,5/2,5). 100% = 20%
Điều chế NH 3 từ hỗn hợp hồm N 2 và H 2 (tỉ lệ 1 : 3) . Tỉ khối hỗn hợp trước so với hỗn hợp sau phản ứng là 0,9. Hiệu suất phản ứng là
A. 25%.
B. 40%.
C. 10%.
D. 20%.
Một hỗn hợp A gồm hai khí N2 và H2 theo tỉ lệ 1:3. Tạo phản ứng giữa H2 với N2 cho ra NH3. Sau phản ứng thu được hỗn hợp khí B có tỉ khối: dA/B = 0,6. Tính hiệu suất phản ứng tổng hợp NH3.
A. 80%
B. 50%
C. 20%
D. 75%
Hỗn hợp khí A gồm N2 và H2 có tỉ lệ 1:3 về thể tích. Sau phản ứng thu được hỗn hợp B. Tỉ khối của A so với B là 0,6. Hiệu suất tổng hợp NH3 là bao nhiều?
Gọi N2 ban đầu là a thì H2 ban đầu là 3a,
gọi số mol N2 p/ứ là b:.
\(N_2+3H_2\rightarrow2NH_3\)
\(b\) \(3b\) \(2b\)
Ta có :
\(\frac{2b+\left(a-b\right)+\left(3a-3b\right)}{a}=0,6\)
Từ đó : \(\Rightarrow\frac{b}{a}=0,8\) hay \(H=80\%\)
Hỗn hợp khí A gồm N2 và H2 có tỉ lệ 1:3 về thể tích. Sau phản ứng thu được hỗn hợp B. Tỉ khối của A so với B là 0,6. Hiệu suất tổng hợp NH3 là bao nhiêu?
Mình cảm ơn nhiều.
Hỗn hợp A gồm N2 và H2 theo tỷ lệ thể tích 1:3, tạo phản ứng giữa N2 và H2 sinh ra NH3. Sau phản ứng được hỗn hợp khí B có tỉ khối so với khí A là 10/6. Hiệu suất phản ứng là
A. 80%
B. 50%
C. 70%
D. 85%
Hỗn hợp A gồm N2 và H2 theo tỷ lệ thể tích 1:3, tạo phản ứng giữa N2 và H2 sinh ra NH3. Sau phản ứng được hỗn hợp khí B có tỉ khối so với khí A là 10/6. Hiệu suất phản ứng là
A. 80%
B. 50%
C. 70%
D. 85%