Làm thế nào để phân biệt oxi hóa mạnh oxi hóa yếu và không oxi hóa
Chọn câu đúng khi nói về flo, clo, brom, iot:
A. Flo có tính oxi hóa rất mạnh, oxi hóa mãnh liệt nước.
B. Clo có tính oxi hóa mạnh, oxi hóa được nước.
C. Brom có tính oxi hóa mạnh, nhưng yếu hơn flo và clo, nó cũng oxi hóa được nước.
D. Iot có tính oxi hóa yếu hơn flo, clo, brom nhưng cũng oxi hóa được nước.
Cho các ion riêng biệt trong dung dịch là Ni2+, Zn2+, Ag+, Sn2+, Fe3+, Pb2+. Ion có tính oxi hóa mạnh nhất và ion có tính oxi hóa yếu nhất lần lượt là
A. Fe3+ và Zn2+.
B. Ag+ và Zn2+.
C. Ni2+ và Sn2+
D. Pb2+ và Ni2+.
Cho các ion riêng biệt trong dung dịch là Ni2+, Zn2+, Ag+, Sn2+, Au3+, Pb2+. Ion có tính oxi hóa mạnh nhất và ion có tính oxi hóa yếu nhất lần lượt là
A. Au3+ và Zn2+.
B. Ag+ và Zn2+
C. Ni2+ và Sn2+
D. Pb2+ và Ni2+.
Đáp án : A
Kim loại có tính khử mạnh thì ion của nó có tính oxi hóa yếu và ngược lại
Có các ion riêng biệt trong dung dịch là Ni 2 + , Zn 2 + , Ag + , Sn 2 + , Au 3 + , Pb 2 + . Ion có tính oxi hóa mạnh nhất và ion có tính oxi hóa yếu nhất lần lượt là
A. Pb 2 + và Ni 2 + .
B. Ag + và Zn 2 +
C. Au 3 + và Zn 2 + .
D. Ni 2 + và Sn 2 + .
Cho các ion riêng biệt trong dung dịch là Ni 2 + , Zn 2 + , Ag + , Sn 2 + , Fe 3 + , Pb 2 + . Ion có tính oxi hóa mạnh nhất và ion có tính oxi hóa yếu nhất lần lượt là
A. Fe 3 + và Zn 2 +
B. Ag + và Zn 2 +
C. Ni 2 + và Sn 2 +
D. Pb 2 + và Ni 2 +
Phân biệt chất oxi hóa và sự oxi hóa, chất khử và sự khử. Lấy thí dụ để minh họa.
Chất oxi hóa là chất nhận electron.
Sự oxi hóa một chất là làm cho chất đó nhường electron.
Chất khử là chất nhường electron.
Sự khử một chất là sự làm cho chất đó thu electron.
Thí dụ: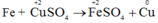
- Nguyên tử Fe nhường electron, là chất khử. Sự nhường electron của Fe được gọi là sự oxi hóa nguyên tử sắt.
- Ion đồng nhận electron, là chất oxi hóa. Sự nhận electron của ion đồng được gọi là sự khử ion đồng.
Nhận xét nào sau đây về tính chất hóa học của cacbon là đúng?
A. Cacbon không thể hiện tính oxi hóa và tính khử.
B. Cacbon thể hiện tính oxi hóa và tính khử với mức độ ngang nhau.
C. Cacbon thể hiện tính oxi hóa và tính khử nhưng tính oxi là tính chất chủ yếu.
D. Cacbon thể hiện tính oxi hóa và tính khử nhưng tính khử là tính chất chủ yếu.
Cho các nhận xét:
(1) Dung dịch H2SO4 đặc nóng có tính axit mạnh và tính oxi hóa mạnh,dung dịch HCl có tính axit mạnh và tính khử mạnh.
(2) Phân tử SO2 có khả năng làm mất màu nước brom.
(3) Hiđro sunfua khi tác dụng với dung dịch NaOH có thể tạo hai muối.
(4) Hiđropeooxit (H2O2) là chất vừa có tính oxi hóa vừa có tính khử.
(5) O2 và O3 đều cóa tính oxi hóa mạnh,nhưng tính oxi hóa của O3 mạnh hơn O2.
Số nhận xét đúng:
A.2
B.3
C.4
D.5
Chọn đáp án C
(1) (Sai vì tính axit là tính khử khi tính oxi hóa mạnh thì tính khử yếu)
(2) Đ
(3) Đ
(4) Đ
(5) Đ
Cho các phát biểu sau:
(1) Điều chế oxi trong phòng thí nghiệm bằng các nhiệt phân KMnO4 (rắn), KClO3 (rắn), …
(2) Chưng cất phân đoạn không khí lỏng là phương pháp duy nhất điều chế oxi trong công nghiệp
(3) Khí ozon không màu, không mùi, tan nhiều trong nước
(4) Ozon có tính oxi hóa rất mạnh và mạnh hơn cả oxi
(5) Ozon oxi hóa hầu hết các kim loại kể cả Au, Pt
(6) Ở điều kiện bình thường, oxi và ozon có thể oxi hóa bạc thành bạc oxit
Số phát biểu đúng là:
A.2
B.1
C.3
D.4
(1) Điều chế oxi trong phòng thí nghiệm bằng các nhiệt phân KMnO4 (rắn), KClO3 (rắn),
(4) Ozon có tính oxi hóa rất mạnh và mạnh hơn cả oxi
ĐÁP ÁN A
hãy dẫn ra những phản ứng hóa học để chứng minh rằng : a) oxi và ozon đều có tính oxi hóa ; b) ozon có tính oxi hóa mạnh hơn oxi .
a) Oxi và ozon đều có tính oxi hóa.
(1) Tác dụng với kim loại, oxi tác dụng với hầu hết các kim loại trừ Pt, Au, Ag... còn ozon tác dụng với hầu hết các kim loại trừ Au và Pt.
3Fe + 2O2 Fe3O4
2Ag + O3 -> Ag2O + O2
(2) Tác dụng với phi kim.
4P + 5O2 -> 2P2O5
2C + 2O3 -> 2CO2 + O2
(3) Tác dụng với nhiều hợp chất vô cơ, hữu cơ :
C2H5OH + 3O2 -> 2CO2 + 3H2O
2H2S + 3O2 -> 2SO2 + 2H2O
b) Ozon có tính oxi hóa mạnh hơn oxi.
- Oxi không tác dụng được với Ag, nhưng Ozon tác dụng được :
2Ag + O3 -> Ag2O + O2
O2 không oxi hóa được I- nhưng O3 oxi hóa được thành I2 :
2KI + O3 + H2O -> I2 + 2KOH + O2
-So với phân tử O2, phân tử O3 kém bền , dễ bị phân hủy .
O3 -> O2 + O ; 2O -> O2
Oxi dạng nguyên tử hoạt động mạnh hơn oxi dạng phân tử nên ozon hoạt động mạnh hơn oxi.