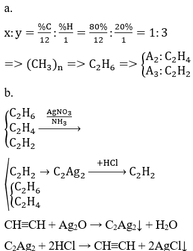Đốt cháy hoàn toàn một hợp chất có CTHH CxHy. Sau đó ấp thụ toàn bộ sản phẩm vào dd Ca(OH)2 dư thì thấy có 30g kết tủa và khối lượng dd giảm xuống 6g. Xác định CTHH của CxHy, biết CTHH này trùng với CT đơn giản nhất.

Những câu hỏi liên quan
Đốt cháy hoàn toàn một hợp chất có CTHH CxHy. Sau đó ấp thụ toàn bộ sản phẩm vào dd Ca(OH)2 dư thì thấy có 30g kết tủa và khối lượng dd giảm xuống 6g. Xác định CTHH của CxHy, biết CTHH này trùng với CT đơn giản nhất.
Đốt cháy hoàn toàn hợp chất CxHy. Sau đó dẫn toàn bộ sản phẩm cháy vào 400ml dd Ba(OH)2 1M. Thấy có 29,55(g) kết tủa và thấy khối lượng dd giảm 17,15g. Xác định Công thức của CxHy biết M(CxHy)= 28(g/mol)
Ta có: \(n_{Ba\left(OH\right)_2}=0,4.1=0,4\left(mol\right)\)
\(n_{BaCO_3}=\dfrac{29,55}{197}=0,15\left(mol\right)\)
TH1: Ba(OH)2 dư.
BTNT C, có: nCO2 = nBaCO3 = 0,15 (mol) = nC
Có: m dd giảm = mBaCO3 - mCO2 - mH2O ⇒ mH2O = 5,8 (g)
\(\Rightarrow n_{H_2O}=\dfrac{5,8}{18}=\dfrac{29}{90}\left(mol\right)\Rightarrow n_H=\dfrac{29}{45}\left(mol\right)\)
\(\Rightarrow x:y=0,15:\dfrac{29}{45}\approx23:100\) → vô lý
TH2: Ba(OH)2 hết.
BTNT Ba, có: nBa(HCO3)2 = 0,4 - 0,15 = 0,25 (mol)
BTNT C, có: nCO2 = 0,25.2 + 0,15 = 0,65 (mol)
Có: m dd giảm = mBaCO3 - mCO2 - mH2O ⇒ mH2O = -16,2 → vô lý
Bạn xem lại đề nhé.
Đúng 2
Bình luận (2)
Đốt cháy hiđrocacbon X, rồi hấp thụ hoàn toàn sản phẩm cháy vào dd Ba(OH)2 dư, thấy có 49,25 gam kết tủa xuất hiện và khối lượng dd sau phản ứng giảm đi 32,85 gam. CTPT của X là: A. C5H12 B. C2H6 C. C3H8 D. C4H10
Đọc tiếp
Đốt cháy hiđrocacbon X, rồi hấp thụ hoàn toàn sản phẩm cháy vào dd Ba(OH)2 dư, thấy có 49,25 gam kết tủa xuất hiện và khối lượng dd sau phản ứng giảm đi 32,85 gam. CTPT của X là:
A. C5H12
B. C2H6
C. C3H8
D. C4H10
Đáp án A
nCO2 = nBaCO3 = 49,25/197 = 0,25 mol ; mCO2 + mH2O = 49,25 – 32,85 = 16,4
mH2O = 16,4 – 0,25.44 = 5,4 ; nH2O = 5,4/18 = 0,3 mol ; nH2O > nCO2 => X là ankan ;
CTPT của X là : CnH2n+2 ; n = 0,25/0,05 = 5=> X : C5H12
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 4,3g hidrocacbon X cần dùng vừa đủ V lít O2 (đktc). Sản phẩm cháy cho hấp thụ hết vào bình đựng dd Ca(OH)2. Sau khi các pứ xảy ra hoàn toàn thu đc 20g kết tủa và 1 dd có khối lượng giảm 0.5g.
Xem chi tiết
a. Xác định CTPT của X
b. Tính V
c. Xác định công thức cấu tạo của X. Biết khi mono clo hóa X thu được tối đa 4 sản phẩm thế
\(n_{CaCO_3}=\dfrac{20}{100}=0,2\left(mol\right)\)
Đặt CTHH của X là \(C_xH_y\)
\(C_xH_y+\left(x+\dfrac{y}{4}\right)O_2\underrightarrow{t^o}xCO_2+\dfrac{y}{2}H_2O\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
\(2CO_2+Ca\left(OH\right)_2\rightarrow Ca\left(HCO_3\right)_2\)
\(m_{dd.giảm}=m_{kt}-\left(m_{CO_2}+m_{H_2O}\right)\\ \Leftrightarrow0,5=20-\left(m_{CO_2}+m_{H_2O}\right)\\ \Rightarrow m_{CO_2}+m_{H_2O}=20-0,5=19,5\left(g\right)\left(I\right)\)
Mặt khác:
\(m_{O_2}=m_{CO_2}+m_{H_2O}-m_X=19,5-4,3=15,2\left(g\right)\\ \Rightarrow n_{CO_2}+0,5n_{H_2O}=\dfrac{15,2}{32}=0,475\left(mol\right)\left(II\right)\)
Từ (I), (II) suy ra: \(\left\{{}\begin{matrix}n_{CO_2}=0,3\\n_{H_2O}=0,35\end{matrix}\right.\)
Vì \(n_{H_2O}>n_{CO_2}\Rightarrow X:ankan\) \(\left(C_nH_{2n+2}\right)\)
\(n=\dfrac{n_{CO_2}}{n_{H_2O}-n_{CO_2}}=\dfrac{0,3}{0,35-0,3}=6\)
a
CTPT của X: \(C_6H_{14}\)
b
\(V_{O_2}=0,475.22,4=10,64\left(l\right)\)
c
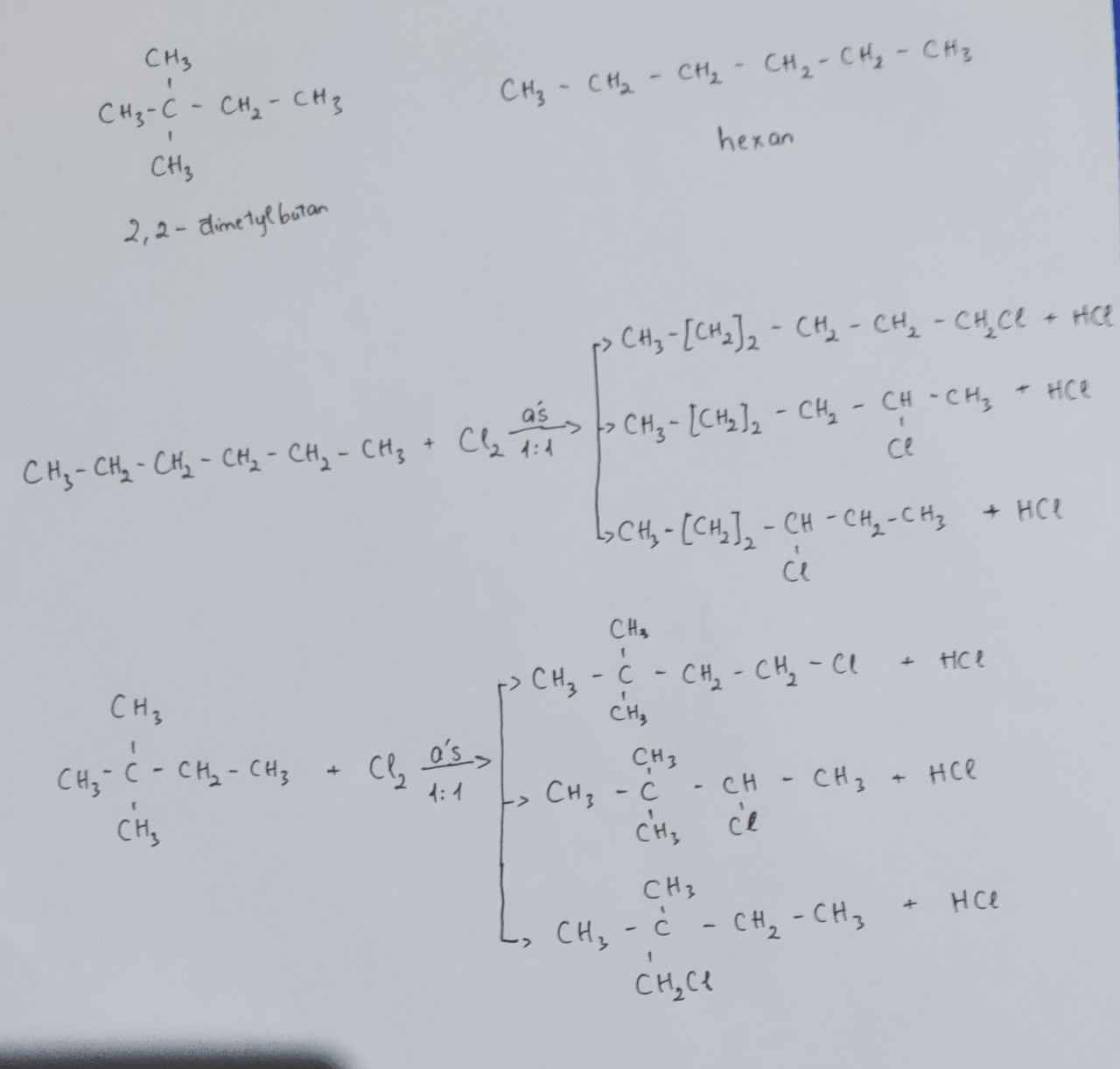
Đúng 3
Bình luận (1)
Cho hỗn hợp A gồm 3 hiđrocacbon A1, A2, A3 có công thức phân tử lần lượt là: CxHy, CxHy–2, CxHy–4. Trong đó, A1 có chứa 20% H về khối lượng. a. Xác định công thức phân tử và viết công thức cấu tạo của A1, A2, A3. b. Trình bày phương pháp tách riêng A3 từ hỗn hợp A. c. Đốt cháy hoàn toàn V lít hỗn hợp A (đktc) rồi cho toàn bộ sản phẩm cháy sục vào bình chứa nước vôi trong dư thấy xuất hiện 4 gam kết tủa, đồng thời khối lượng dung dịch trong bình nước vôi giảm a gam. Tính V và tìm khoảng giới hạn...
Đọc tiếp
Cho hỗn hợp A gồm 3 hiđrocacbon A1, A2, A3 có công thức phân tử lần lượt là: CxHy, CxHy–2, CxHy–4. Trong đó, A1 có chứa 20% H về khối lượng.
a. Xác định công thức phân tử và viết công thức cấu tạo của A1, A2, A3.
b. Trình bày phương pháp tách riêng A3 từ hỗn hợp A.
c. Đốt cháy hoàn toàn V lít hỗn hợp A (đktc) rồi cho toàn bộ sản phẩm cháy sục vào bình chứa nước vôi trong dư thấy xuất hiện 4 gam kết tủa, đồng thời khối lượng dung dịch trong bình nước vôi giảm a gam. Tính V và tìm khoảng giới hạn của a.
Đốt cháy hoàn toàn một hidrocacbon X. Hấp thụ toàn bộ sản phâm cháy vào dung dịch Ba(OH)2 dư tạo ra 29,55 gam kết tủa, dung dịch sau phản ứng có khối lượng giảm 19,35 gam so ới dd Ba(OH)2 ban đầu. Xác định CTPT cua X
Ta có: \(n_{CO_2}=n_{BaCO_3}=\dfrac{29,55}{197}=0,15\left(mol\right)\)
m giảm = m kết tủa - mCO2 - mH2O
⇒ mH2O = 29,55 - 0,15.44 - 19,35 = 3,6 (g)
\(\Rightarrow n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
Vì: Đốt cháy hiđrocacbon X thu được nH2O > nCO2 nên X là ankan.
⇒ nX = 0,2 - 0,15 = 0,05 (mol)
Gọi CTPT của X là CnH2n+2 (n ≥ 1)
\(\Rightarrow n=\dfrac{0,15}{0,05}=3\left(tm\right)\)
Vậy: X là C3H8.
Bạn tham khảo nhé!
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 4,08 gam hỗn hợp các hidrocacbon trong oxi vừa đủ thu được sản phẩm khử (chỉ chứa CO2 và H2O. Hấp thụ toàn bộ lượng sản phẩm này vào dung dịch Ca(OH)2 dư thấy khối lượng bình tăng 17,52 gam và xuất hiện m gam kết tủa. Xác định giá trị của m
Ta có: m bình tăng = mCO2 + mH2O
⇒ 17,52 = 44nCO2 + 18nH2O (1)
BTNT C, có: nC = nCO2
BTNT H, có: nH = 2nH2O
⇒ mC + mH = 4,08 ⇒ 12nCO2 + 2nH2O = 4,08 (2)
Từ (1) và (2) ⇒ nCO2 = 0,3 (mol), nH2O = 0,24 (mol)
⇒ nCaCO3 = nCO2 = 0,3 (mol)
⇒ m = m kết tủa = 0,3.100 = 30 (g)
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 6,8 gam một este A no đơn chức chứa vòng benzen thu được CO2 và H2O . Hấp thụ toàn bộ sản phẩm này vào bình đựng dung dịch Ca(OH)2 lấy dư thấy khối lượng bình tăng 21,2 gam đồng thời có 40 gam kết tủa. Xác định CTPT, CTCT có thể có của A A. 2 B. 3 C. 6 D. 5
Đọc tiếp
Đốt cháy hoàn toàn 6,8 gam một este A no đơn chức chứa vòng benzen thu được CO2 và H2O . Hấp thụ toàn bộ sản phẩm này vào bình đựng dung dịch Ca(OH)2 lấy dư thấy khối lượng bình tăng 21,2 gam đồng thời có 40 gam kết tủa. Xác định CTPT, CTCT có thể có của A
A. 2
B. 3
C. 6
D. 5
Đáp án : C
Ta có: mCaCO3 = 40 => nCO2 = 0,4 mol.
m bình tăng = mCO2 + mH2O => mH2O = 3,6
=> nH2O = 0,2 mol.
=> mO (trong este) = 6,8 – 0,4.12 – 0,2.2 = 1,6
=> nO = 0,1
Ta có: C: H: O = 0,4 : 0,4 : 0,1 = 4 : 4 : 1 = 8 : 8 : 2
=> Este là C8H8O2.
Các đồng phân:
HCOO – CH2 – C6H5
CH3-COO – C6H5
C6H5 – COO – CH3.
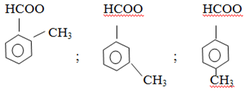
=>Có 6 đồng phân
Đúng 0
Bình luận (0)
1.Hỗn hợp X ( gồm CH4 và C2H6) có tỉ khối so với không khí bằng 0,6. Đốt cháy hoàn toàn 3,36 lít X(đktc) rồi hấp thụ hết toàn bộ sản phẩm bằng dd Ca(OH)2 dư thu đc m gam kết tủa. Tính khối lượng kết tủa thu đc?
Xem chi tiết
Ta có: \(\left\{{}\begin{matrix}\overline{M}_{hhkhí}=0,6\cdot29=17,4\\n_{hhkhí}=\dfrac{3,36}{22.4}=0,15\left(mol\right)\end{matrix}\right.\)
Theo phương pháp đường chéo: \(\dfrac{n_{CH_4}}{n_{C_2H_4}}=\dfrac{53}{7}\) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,1325\left(mol\right)\\n_{C_2H_4}=0,0175\left(mol\right)\end{matrix}\right.\)
Bảo toàn nguyên tố: \(\Sigma n_{CaCO_3}=n_{CH_4}+2n_{C_2H_4}=0,1675\left(mol\right)\)
\(\Rightarrow m_{CaCO_3}=0,1675\cdot100=16,75\left(g\right)\)
Đúng 1
Bình luận (2)