Cho dd Y chứa 0,25 mol Cu2+, x mol Al3+, 0,1 mol Cl- và y mol SO4 2- . Cô cạn dd Y thu được 72,95 gam chất rắn. Tìm x và y

Những câu hỏi liên quan
Dung dịch X chứa các ion: Fe2+ (0,1 mol); Al3+ (0,2 mol), Cl- (x mol), SO42- (y mol). Cô cạn dung dịch X thu được 46,9 gam muối rắn. Giá trị của x và y lần lượt là: A. 0,1 và 0,35 B. 0,3 và 0,2 C. 0,2 và 0,3 D. 0,4 và 0,2
Đọc tiếp
Dung dịch X chứa các ion: Fe2+ (0,1 mol); Al3+ (0,2 mol), Cl- (x mol), SO42- (y mol). Cô cạn dung dịch X thu được 46,9 gam muối rắn. Giá trị của x và y lần lượt là:
A. 0,1 và 0,35
B. 0,3 và 0,2
C. 0,2 và 0,3
D. 0,4 và 0,2
Đáp án C
Định luật bảo toàn điện tích: 0,1.2+ 0,2.3= x.1+ y.2
Định luật bảo toàn khối lượng: 0,1.56+ 0,2.27+ 35,5.x+ 96.y= 46,9
Suy ra x= 0,2; y=0,3
Đúng 0
Bình luận (0)
Một dd X chứa 0,15 mol So4 2-, 0,2 mol NO3-, 0,1 mol Zn 2+,15 mol H+, và Cu 2+. Cô cạn X thu được chất rắn Y, nung đến khối lượng k đổi được chất rắn Z. m Z=?
Áp dụng bảo toàn điện tích ta có:
\(n_{Cu^{2+}}=0,15.2+0,2-0,1.2-0,15=0,15\left(mol\right)\)\(\rightarrow m_Z=0,15.96+0,2.62+0,1.65+0,15.1+0,15.64\)\(=43,05\left(g\right)\)
Đúng 0
Bình luận (0)
KHẨN CẦU MỌI NGƯỜI GIẢI NHANH GIÚP EM VỚI Ạ!!! :câu 1:Dung dịch X chứa các ion: Fe2+ (0,1 mol), Al3+ (0,2 mol), Cl- (x mol), SO42- (y mol). Cô cạn dung dịch X thu được 44,4 gam muối rắn. Tìm giá trị x và y?Câu 2 : Cho 5,1 gam hỗn hợp Al và Mg tác dụng với dung dịch HNO3 loãng dư, thu được dung dịch X và 1,12 lít khí N2 (đktc, sản phẩm khử duy nhất). Khối lượng muối thu được trong X là?Câu 3 : Trộn 200ml dung dịch gồm HCl 0,01M và H2SO4 0,02M với 300ml dung dịch KOH 0,03M. Tính pH dung dịch thu đ...
Đọc tiếp
KHẨN CẦU MỌI NGƯỜI GIẢI NHANH GIÚP EM VỚI Ạ!!! :<<<<
câu 1:Dung dịch X chứa các ion: Fe2+ (0,1 mol), Al3+ (0,2 mol), Cl- (x mol), SO42- (y mol). Cô cạn dung dịch X thu được 44,4 gam muối rắn. Tìm giá trị x và y?
Câu 2 : Cho 5,1 gam hỗn hợp Al và Mg tác dụng với dung dịch HNO3 loãng dư, thu được dung dịch X và 1,12 lít khí N2 (đktc, sản phẩm khử duy nhất). Khối lượng muối thu được trong X là?
Câu 3 : Trộn 200ml dung dịch gồm HCl 0,01M và H2SO4 0,02M với 300ml dung dịch KOH 0,03M. Tính pH dung dịch thu được?
(Cho biết Fe=56; Al=27; Cl=35,5; S=32; O=16; H=1; N=14)
Câu 1:
Theo ĐLBT ĐT, có: x + 2y = 0,1.2 + 0,2.3 (1)
Theo ĐLBT KL, có: 35,5x + 96y = 44,4 - 0,1.56 - 0,2.27 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,4\left(mol\right)\\y=0,2\left(mol\right)\end{matrix}\right.\)
Câu 2:
Gọi: \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Mg}=y\left(mol\right)\end{matrix}\right.\)
⇒ 27x + 24y = 5,1 (1)
Có: \(n_{N_2}=0,05\left(mol\right)\)
Theo ĐLBT e, có: 3x + 2y = 0,05.10 (2)
Từ (1) và (2) \(\Rightarrow x=y=0,1\left(mol\right)\)
BTNT Al và Mg, có: \(n_{Al\left(NO_3\right)_3}=n_{Mg\left(NO_3\right)_2}=0,1\left(mol\right)\)
⇒ m muối = 0,1.213 + 0,1.148 = 36,1 (g)
Câu 3:
Có: \(n_{H^+}=0,2.0,01+0,2.0,02.2=0,01\left(mol\right)\)
\(n_{OH^-}=0,3.0,03=0,009\left(mol\right)\)
PT: \(H^++OH^-\rightarrow H_2O\)
__0,01___0,009 (mol)
⇒ H+ dư và nH+ (dư) = 0,001 (mol)
\(\Rightarrow\left[H^+\right]=\dfrac{0,001}{0,2+0,3}=0,002\left(M\right)\)
\(\Rightarrow pH=-log0,002\approx2,7\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
Cho 0,1 mol chất X (CH6O3N2) tác dụng với dd chứa 0,2 mol NaOH đun nóng thu được chất khí làm xanh giấy quì tím ẩm và dd Y. Cô cạn dd Y thu được m gam rắn khan. Giá trị của m là: A. 8,5. B. 12,5. C. 15. D. 21,8.
Đọc tiếp
Cho 0,1 mol chất X (CH6O3N2) tác dụng với dd chứa 0,2 mol NaOH đun nóng thu được chất khí làm xanh giấy quì tím ẩm và dd Y. Cô cạn dd Y thu được m gam rắn khan. Giá trị của m là:
A. 8,5.
B. 12,5.
C. 15.
D. 21,8.
Đáp án B
X có công thứ CH6O3N2 tác dụng NaOH sinh ra chất khí làm xanh giấy quỳ → X có cấu tạo CH3NH3NO3
CH3NH3NO3 +NaOH → CH3NH2 + NaNO3 + H2O
Thấy nX < nNaOH → NaOH còn dư : 0,1 mol
mchất rắn = mNaNO3 + mNaOH dư = 0,1. 85 + 0,1. 40 = 12,5 gam
Đáp án B.
Đúng 0
Bình luận (0)
Cho 0,1 mol chất X có công thức là
C
2
H
12
O
4
N
2
S
tác dụng với dd chứa 0,35 mol NaOH đun nóng thu được chất khí làm xanh giấy quỳ ẩm và dd Y. Cô cạn dd Y thu được m gam chất rắn khan. Giá trị của m là ? A. 26,4 gam B. 15 gam C. 14,2 gam D. 20,2 gam
Đọc tiếp
Cho 0,1 mol chất X có công thức là C 2 H 12 O 4 N 2 S tác dụng với dd chứa 0,35 mol NaOH đun nóng thu được chất khí làm xanh giấy quỳ ẩm và dd Y. Cô cạn dd Y thu được m gam chất rắn khan. Giá trị của m là ?
A. 26,4 gam
B. 15 gam
C. 14,2 gam
D. 20,2 gam
Cô cạn dung dịch X chứa 0,1 mol Al3+; 0,1 mol Cu2+; 0,2 mol SO42- và 1 lượng ion Cl- thì thu được bao nhiêu gam muối khan? A. 28,3 B. 31,85 C. 34,5 D. 42,7
Đọc tiếp
Cô cạn dung dịch X chứa 0,1 mol Al3+; 0,1 mol Cu2+; 0,2 mol SO42- và 1 lượng ion Cl- thì thu được bao nhiêu gam muối khan?
A. 28,3
B. 31,85
C. 34,5
D. 42,7
Đáp án B
0,1.3 + 0,1.2 = 0,2.2 +![]() = 0,1
= 0,1
Bảo toàn khối lượng mmuối = 0,1.27 + 0,1.64 + 0,2.96 + 0,1.35,5 = 31,85g
Đúng 0
Bình luận (0)
Cô cạn dung dịch X chứa 0,1 mol Al3+; 0,1 mol Cu2+; 0,2 mol SO42- và 1 lượng ion Cl- thì thu được bao nhiêu gam muối khan?
A. 28,3.
B. 31,85.
C. 34,5.
D. 42,7.
0,1.3 + 0,1.2 = 0,2.2 + n Cl - → n Cl - = 0,1
Bảo toàn khối lượng → mmuối = 0,1.27 + 0,1.64 + 0,2.96 + 0,1.35,5 = 31,85g
Đáp án B
Đúng 0
Bình luận (0)
Cô cạn dung dịch X chứa 0,1 mol
Al
3
+
; 0,1 mol
Cu
2
+
; 0,2 mol
SO
4
2
-
và 1 lượng ion
Cl
-
thì thu được bao nhiêu gam muối khan? A. 28,3 B. 31,85 C. 34,5 D. 42,7
Đọc tiếp
Cô cạn dung dịch X chứa 0,1 mol Al 3 + ; 0,1 mol Cu 2 + ; 0,2 mol SO 4 2 - và 1 lượng ion Cl - thì thu được bao nhiêu gam muối khan?
A. 28,3
B. 31,85
C. 34,5
D. 42,7
Chọn B
Bảo toàn điện tích có:
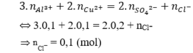
Bảo toàn khối lượng có:
mmuối = ∑mion = 0,1.27 + 0,1.64 + 0,2.96 + 0,1.35.5 = 31,85 (gam).
Đúng 0
Bình luận (0)
Một dung dịch chứa 2 cation: 0,02 mol Al3+, 0,03 mol Fe2+ và 2 anion: x mol Cl-, y mol SO42-. Khi cô cạn dung dịch thu được 7,23 gam chất rắn khan. Dung dịch chứa 2 muối là: A. Al2(SO4)3, FeCl2 B. Al2(SO4)3, FeCl3 C. AlCl3, FeSO4 D. AlCl3, Fe2(SO4)3
Đọc tiếp
Một dung dịch chứa 2 cation: 0,02 mol Al3+, 0,03 mol Fe2+ và 2 anion: x mol Cl-, y mol SO42-. Khi cô cạn dung dịch thu được 7,23 gam chất rắn khan. Dung dịch chứa 2 muối là:
A. Al2(SO4)3, FeCl2
B. Al2(SO4)3, FeCl3
C. AlCl3, FeSO4
D. AlCl3, Fe2(SO4)3
Theo định luật bảo toàn điện tích: 0,02.3+ 0,03.2=x + 2y
mmuối= 0,02.27+ 0,03.56 + 35,5.x+ 96.y=7,23
Suy ra x=0,06; y=0,03
Ta có: 2 cation: 0,02 mol Al3+, 0,03 mol Fe2+ và 2 anion: 0,06 mol Cl-, 0,03 mol SO42-
Suy ra 2 muối là FeCl2 và Al2(SO4)3
Đúng 0
Bình luận (0)









