Viết cấu hình electron của các nguyên tử, ion sau:Al(Z=13); Al3+;Cl (Z=17);Cl-?

Những câu hỏi liên quan
Cho biết nguyên tử Clo có Z17, cấu hình electron của ion Cl- là: A. 1s2 2s2 2p6 3s2 3p5 B. 1s2 2s2 2p6 3s2 3p6 C. 1s2 2s2 2p6 3s2 3p4 D. 1s2 2s2 2p6 3s2 3p6 4s1
Đọc tiếp
Cho biết nguyên tử Clo có Z=17, cấu hình electron của ion Cl- là:
A. 1s2 2s2 2p6 3s2 3p5
B. 1s2 2s2 2p6 3s2 3p6
C. 1s2 2s2 2p6 3s2 3p4
D. 1s2 2s2 2p6 3s2 3p6 4s1
Đáp án B
Theo quy tắc bát tử, Clo có xu hướng nhận thêm 1e
Đúng 0
Bình luận (0)
Cho các nguyên tử: Al (Z = 13); S (Z = 16); O (Z =8); Fe (Z = 26); Cu (Z = 29); Zn (Z = 30); Cl (Z =
17); K (Z = 19); Br (Z = 35), Ne (Z = 10).
a. Viết cấu hình electron của các nguyên tử trên.
b. Cho biết nguyên tố nào thuộc nguyên tố s , p , d , f ? Vì sao?
c. Xác định kim loại, phi kim, khí hiếm?
Al : 1s22s22p63s23p1 ( kim loại vì lớp e ngoài cùng có 3e)
S : 1s22s22p63s23p4 ( phi kim vì lớp e ngoài cùng có 6e )
O : 1s22s22p4 ( phi kim vì lớp e ngoài cùng có 6e )
Fe : 1s22s22p63s23p63d64s2 ( kim loại vì lớp e ngoài cùng có 2e )
Cu : 1s22s22p63s23p63d104s1 ( kim loại vì lớp e ngoài cùng có 1e )
Zn : 1s22s22p63s23p63d104s2 ( kim loại vì lớp e ngoài cùng có 2e )
Cl : 1s22s22p63s23p5 ( kim loại vì lớp e ngoài cùng có 7e )
K : 1s22s22p63s23p64s1 ( kim loại vì lớp e ngoài cùng có 1e )
Br : 1s22s22p63s23p63d104s24p5 (kim loại vì lớp e ngoài cùng có 7e )
Ne : 1s22s22p6 ( khí hiếm vì lớp e ngoài cùng có 8e )
- Nguyên tố s : K ( e cuối cùng điền vào phân lớp s )
- Nguyên tố p : O, Ne, S, Cl, Br, Al ( e cuối cùng điền vào phân lớp p )
- Nguyên tố d : Fe, Cu, Zn ( e cuối cùng điền vào phân lớp d )
Đúng 1
Bình luận (0)
Cấu hình electron của ion được thiết lập bằng cách thêm hoặc bớt electron, bắt đầu từ phân lớp ngoài cùng của cấu hình electron nguyên tử tương ứng. a. Viết cấu hình electron của Na+ và Cl-. b. Nguyên tử Cl nhận 1 electron để trở thành ion Cl-, electron này xếp vào AO thuộc phân lớp nào của Cl? AO đó là AO trống, chứa 1 hay 2 electron?
Cấu hình electron của ion được thiết lập bằng cách thêm hoặc bớt electron, bắt đầu từ phân lớp ngoài cùng của cấu hình electron nguyên tử tương ứng.
a) Viết cấu hình electron của Na+ và Cl-.
b) Nguyên tử Cl nhận 1 electron để trở thành ion Cl-, electron này xếp vào AO thuộc phân lớp nào của Cl? AO đó là AO trống, chứa 1 hay 2 electron?
a) Na (Z = 11) 1s22s22p63s1 ⇒ Na+: 1s22s22p6.
Cl (Z = 17) 1s22s22p63s23p5 ⇒ Cl-: 1s22s22p63s23p6.
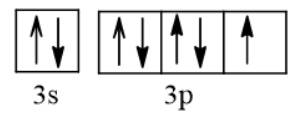
b) Nguyên tử Cl nhận 1 electron để trở thành ion Cl-, electron này xếp vào AO thuộc phân lớp p của Cl. AO đó là AO chứa 1 electron.
Đúng 0
Bình luận (0)
Câu 7: Hãy viết cấu hình electron của các ion sau : (1) Na^ + ( (Na / Z = 11) (2) Cl * (Cl / Z - 17) (3) Ca^ 2+ (Ca / Z = 20) (4) Ni^ 2+ (Ni:Z=28) (5) Fc^ 2+ , Fc3+(Fc:Z-26) (6) Cu^ + ,Cu^ 2+ (Cu:Z=29) (7) S^ 2- (S:Z=16) (8) Al^ 3+ (Al:Z-13)
Viết cấu hình e của Ca(Z=20), Fe(Z=26), Cl(Z=17), S(Z=16) từ đó suy ra cấu hình e
của các ion: Ca2+,Fe2+, Fe3+, Cl-, S2-
Cho 2 nguyên tố Cl (Z = 17); Al( Z=13) a. Viết cấu hình electron b. Cho biết chúng là kim loại, phi kim hay khí hiếm? vì sao? Các bạn hãy giúp mình với :))
Cho ngtử K(Z=19) a) viết cấu hình electron nguyên tử và biểu diễn cấu hình theo ô orbital của nguyên tử Cl b)hãy cho biết Cl là nguyên tố s,p hay d?giải thích
Viết cấu hình electron của cc ion Cu2+,N3-,Fe3+,Cl-,Al3+. Biết số thứ tự của các nguyên tố làn lượt là Cu(Z=29),N(Z=14),Fe(Z=26),Cl(Z=17),Al(Z=13)
\(Cu^{2+}:1s^22s^22p^63s^23p^63d^74s^2\)
\(N^{3-}:1s^22s^22p^63s^23p^5\)
\(Fe^{3+}:1s^22s^22p^63s^23p^63d^34s^2\)
\(Cl^-:1s^22s^22p^63s^23p^6\)
\(Al^{3+}:1s^22s^22p^6\)