có 2 thùng nước ở nhiệt độ t1 và t2. phải pha trộn chúng theo tỉ lệ nào để được 1 hỗn hợp có nhiệt độ t = 1/4 ( t1+t2). nếu t2/t1 = 3,4 thì tỉ lệ đó là bao nhiêu? bỏ qua hao phí nhiệt
Dựa vào nội dung sau đây để trả lời các câu hỏi 25.13 và 25.14.
Đổ một chất lỏng có khối lượng m1, nhiệt dung c1 và nhiệt độ t1 vào một chất lỏng có khối lượng m2 = 2.m1, nhiệt dung riêng c2 = 1/2 .c1 và nhiệt độ t2 > t1
Nếu bỏ qua sự trao đổi nhiệt giữa hai lỏng và môi trường (cốc đựng, không khí…) thì có cân bằng nhiệt, nhiệt độ t của hai chất lỏng trên có giá trị là
A . t = t 2 - t 1 2 B . t = t 2 + t 1 2 C . t < t 1 < t 2 D . t > t 1 > t 2
Chọn B
Nhiệt lượng do chất lỏng 2 tỏa ra là:
Q2 = m2.c2.(t2 - t) = 2.m1. 1/2 .c1.(t2 - t) = m1.c1.(t2 - t)
Nhiệt lượng do chất lỏng 1 thu vào là:
Q1 = m1.c1.(t - t1)
Áp dụng phương trình cân bằng nhiệt ta có: Q1 = Q2 ⇔ t2 – t = t – t1
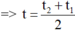
Có ba thùng đựng nước A,B,C có nhiệt độ lần lượt là t1,t2,t3.Nếu múc ở mỗi bình một ca nước pha lẫn với nhau thì hỗn hợp có nhiệt độ 60°C.Nếu pha 3 ca nước ở bình A với 1 ca nước của bình B thì hỗn hợp có nhiêt độ 90°C .Nếu pha 3 ca nước của bình B với 2 ca nước của bình C thì nhiệt độ của hỗn hợp là 44°C.Hỏi cần pha bao nhiêu ca nước ở bình A và bình B để có nước ở nhiệt độ 30°C ? Cho rằng chỉ có trao đổi nhiệt giữa nước với nước.
Hai vật 1 và 2 trao đổi nhiệt với nhau. Khi có cân bằng nhiệt thì nhiệt độ vật 1 giảm bớt △ t 1 , nhiệt độ vật 2 tăng thêm △ t 2 . Hỏi △ t 1 = △ t 2 trong trường hợp nào dưới đây?
A. Khi m 1 = m 2 ; c 1 = c 2 ; t 1 = t 2
B. Khi m 1 = 3 2 m 2 ; c 1 = 2 3 c 2 ; t 1 > t 2
C. Khi m 1 = m 2 ; c 1 = c 2 ; t 1 < t 2
D. Khi m 1 = 3 2 m 2 ; c 1 = 2 3 c 2 ; t 1 < t 2
Chọn B.
Hai vật 1 và 2 trao đổi nhiệt với nhau. Khi có cân bằng nhiệt thì nhiệt độ vật 1 giảm bớt Δt1 tức là vật 1 tỏa nhiệt, nhiệt độ vật 2 tăng thêm Δt2 tức là vật 2 thu nhiệt. Do đó ban đầu t1 > t2.
Khi nhiệt độ cân bằng ta có phương trình cân bằng nhiệt:
Q1 = Q2 ⇔ m1.c1.Δt1 = m2.c2.Δt2
Để Δt1 = Δt2 thì m1.c1 = m2.c2
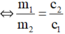
Ta thấy đáp án B là thỏa mãn hệ thức trên và điều kiện t1 > t2.
Trong một bình kín có cân bằng hóa học sau :
2 N O 2 k ⇆ N 2 O 4 k
Tỉ khối hơi của hỗn hợp khí trong bình so với H2 ở nhiệt độ T1 bằng 27,6 và ở nhiệt độ T2 bằng 34,5. Biết T1> T2. Phát biểu nào sau đây về cân bằng trên là đúng?
A. Phản ứng thuận là phản ứng tỏa nhiệt
B. Khi tăng nhiệt độ, áp suất chung của hệ cân bằng giảm
C. Khi giảm nhiệt độ, áp suất chung của hệ cân bằng tăng
D. Phản ứng nghịch là phản ứng tỏa nhiệt
Chọn A
Tỉ khối hơi của hỗn hợp khí trong bình so với H2 ở nhiệt độ T1 bằng 27,6 và ở nhiệt độ T2 bằng 34,5. Biết T1> T2. Suy ra khi giảm nhiệt độ thì số mol khí giảm, tức là cân bằng chuyển dịch theo chiều tạo ra N2O4 khi giảm nhiệt độ.
Vậy phát biểu đúng là “Phản ứng thuận là phản ứng tỏa nhiệt”.
Các phát biểu còn lại đều sai.
Trong một bình kín có cân bằng hóa học sau:
2 N O 2 k ⇄ N 2 O 4 k
Tỉ khối hơi của hỗn hợp khí trong bình so với H2 ở nhiệt độ T1 bằng 27,6 và ở nhiệt độ T2 bằng 34,5. Biết T1 > T2. Phát biểu nào sau đây về cân bằng trên là đúng?
A. Phản ứng thuận là phản ứng tỏa nhiệt
B. Khi tăng nhiệt độ, áp suất chung của hệ cân bằng giảm
C. Khi giảm nhiệt độ, áp suất chung của hệ cân bằng tăng
D. Phản ứng nghịch là phản ứng tỏa nhiệt
- Theo phương trình, số mol hỗn hợp khí sau nhỏ hơn số mol hỗn hợp khí trước, nên tỉ khối của hỗn hợp khí sau so với H2 sẽ lớn hơn tỉ khối của hỗn hợp khí trước so với H2.
- Khi giảm nhiệt độ, tỉ khối tăng chứng tỏ cân bằng chuyển dịch theo chiều thuận → Chiều thuận là chiều toả nhiệt → Chiều nghịch là chiều thu nhiệt.
Chọn đáp án A
Xét phản ứng : 2 N O 2 ( k ) ⇄ N 2 O 4 ( k ) . Tỉ khối hơi của hỗn hợp khí thu được so với H 2 ở nhiệt độ t 1 là 27,6 ; ở nhiệt độ t 2 là 34,5 t 1 > t 2 . Có 3 ống nghiệm đựng khí N O 2 (có nút kín). Sau đó : Ngâm ống thứ nhất vào cốc nước đá ; ngâm ống thứ hai vào cốc nước sôi ; ống thứ ba để ở điều kiện thường. Một thời gian sau, ta thấy
A. ống thứ nhất có màu đậm nhất, ống thứ hai có màu nhạt nhất
B. ống thứ nhất có màu nhạt nhất, ống thứ hai có màu đậm nhất
C. ống thứ nhất có màu đậm nhất, ống thứ ba có màu nhạt nhất
D. ống thứ nhất có màu đậm nhất, ống thứ hai và ống thứ ba đều có màu nhạt hơn
Chọn B
Ở nhiệt độ t 2 hỗn hợp khí có tỉ khối hơi so với H 2 lớn hơn nhiệt độ t 1 → ở nhiệt độ t 2 có lượng N 2 O 4 lớn hơn ở nhiệt độ t 1 .
Mà t 1 > t 2 → khi giảm nhiệt độ cân bằng chuyển dịch theo chiều thuận (tạo thành N 2 O 4 không màu); khi tăng nhiệt độ cân bằng chuyển dịch theo chiều nghịch (tạo thành N O 2 màu nâu).
Xét phản ứng : 2 N O 2 k ⇄ N 2 O 4 k . Tỉ khối hơi của hỗn hợp khí thu được so với H2 ở nhiệt độ t1 là 27,6; ở nhiệt độ t2 là 34,5 (t1 > t2). Có 3 ống nghiệm đựng khí NO2 (có nút kín). Sau đó: Ngâm ống thứ nhất vào cốc nước đá; ngâm ống thứ hai vào cốc nước sôi; ống thứ ba để ở điều kiện thường. Một thời gian sau, ta thấy
A. ống thứ nhất có màu đậm nhất, ống thứ hai có màu nhạt nhất
B. ống thứ nhất có màu nhạt nhất, ống thứ hai có màu đậm nhất
C. ống thứ nhất có màu đậm nhất, ống thứ ba có màu nhạt nhất
D. ống thứ nhất có màu đậm nhất, ống thứ hai và ống thứ ba đều có màu nhạt hơn
- Khi tăng nhiệt độ từ nhiệt độ t1 lên nhiệt độ t1 thì tỉ khối hơi của hỗn hợp khí tăng từ 27,6 lên 34,5 → Số mol phân tử khí giảm → Cân bằng dịch chuyển theo chiều thuận.
- Nhận xét: Khi tăng nhiệt độ mà cân bằng dịch chuyển theo chiều thuận → Phản ứng theo chiều thuận là phản ứng thu nhiệt → Phản ứng theo chiều nghịch là phản ứng tỏa nhiệt.
- Khi ngâm ống nghiệm thứ hai vào cốc nước sôi (tăng nhiệt độ) → Cân bằng dịch chuyển theo chiều giảm nhiệt độ tức là chiều thu nhiệt → Chiều thuận → Màu nâu nhạt dần.
- Khi ngâm ống nghiệm thứ nhất vào cốc nước đá (giảm nhiệt độ) → Cân bằng dịch chuyển theo chiều tăng nhiệt độ tức là chiều tỏa nhiệt → Chiều nghịch → Màu nâu đậm dần.
- Khi để ống nghiệm thứ ba ở điều kiện thường → Cân bằng dịch chuyển theo chiều tăng nhiệt độ tức là chiều tỏa nhiệt → Chiều nghịch → Mâu nâu đậm dần nhưng nhạt hơn ống thứ nhất.
Chọn đáp án D
Trong một bình kín có cân bằng hóa học sau: 2 N O 2 ( K ) ⇔ N 2 O 4 ( K )
Tỉ khối hơi của hỗn hợp khí trong bình so với H2 ở nhiệt độ T1 bằng 27,6 và ở nhiệt độ T2 bằng 34,5. Biết T1>T2. Phát biểu nào sau đây về cân bằng trên là đúng
A. Khi tăng nhiệt độ, áp suất chung của hệ cân bằng giảm
B. Phản ứng thuận là phản ứng tỏa nhiệt
C. Phản ứng ngịch là phản ứng tỏa nhiệt
D. Khi giảm nhiệt độ, áp suất chung của hệ cân bằng tăng
Chọn đáp án B
Khi giảm nhiệt độ M tăng nên số mol khí phải giảm → cân bằng dịch phải .Vậy phản ứng thuận là tỏa nhiệt
Trong một bình kín có cân bằng hóa học sau:
2 N O 2 ( k ) ⇌ N 2 O 4 (k)
Tỉ khối hơi của hỗn hợp khí trong bình so với H 2 ở nhiệt độ T 1 bằng 27,6 và ở nhiệt độ T 2 bằng 34,5. Biết T 1 > T 2 .
Phát biểu nào sau đây về cân bằng trên là đúng?
A. Phản ứng thuận là phản ứng tỏa nhiệt
B. Khi tăng nhiệt độ, áp suất chung của hệ cân bằng giảm
C. Khi giảm nhiệt độ, áp suất chung của hệ cân bằng tăng
D. Phản ứng nghịch là phản ứng tỏa nhiệt
Chọn A
Theo bài ra giảm nhiệt độ cân bằng chuyển dịch theo chiều thuận → phản ứng thuận là phản ứng tỏa nhiệt.