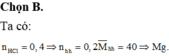để hòa tan 6.4 gam hỗn hợp gồm kim loại R(chỉ có hóa trị 2) và oxit của nó cần vừ đủ 400ml dung dich HCl 1M. tìm kim loại R

Những câu hỏi liên quan
Để hòa tan hoàn toàn 6,4 gam hỗn hợp kim loại R (chỉ có hóa trị II) và oxit của nó cần vừa đủ 400ml dung dịch HCl 1M. Tìm kim loại R
A. Ca
B. Mg
C. Ba
D. Be
Đáp án B
R + HCl → RCl2 + H2
RO + 2HCl → RCl2 + H2O
Ta có: nHCl =0,4.1 = 0,4 mol → ![]() = 0,2 mol →
= 0,2 mol → ![]() = 32
= 32
Theo tính chất của ![]() ta có: M < 32 < M + 16 → 16 < M < 32
ta có: M < 32 < M + 16 → 16 < M < 32
→ M = 24 (Mg) là nghiệm hợp lí
Đúng 0
Bình luận (0)
Để hoà tan hoàn toàn 6,4 gam hỗn hợp gồm kim loại R (chỉ có hoá trị II) và oxit của nó cần vừa đủ 400 ml dung dịch HCl 1M. Kim loại R là
A. Ba
B. Ca
C. Be
D. Mg
Để hoà tan hoàn toàn 6,4 gam hỗn hợp gồm kim loại R (chỉ có hoá trị II) và oxit của nó cần vừa đủ 400 ml dung dịch HCl 1M. Kim loại R là: A. Be B. Ca C. Ba D. Mg
Đọc tiếp
Để hoà tan hoàn toàn 6,4 gam hỗn hợp gồm kim loại R (chỉ có hoá trị II) và oxit của nó cần vừa đủ 400 ml dung dịch HCl 1M. Kim loại R là:
A. Be
B. Ca
C. Ba
D. Mg
Ta có nR = x, nRO = y.
R(x+y)+16y=6,4.
x+y=0,2.
=> 16<R<32.
=> R là magie
=> Đáp án D
Đúng 0
Bình luận (0)
Để hoà tan hoàn toàn 8,4 gam hỗn hợp gồm kim loại R (chỉ có hoá trị II) và oxit của nó cần vừa đủ 100 ml dung dịch HCl 5M. Kim loại R là
A. Ba
B. Ca
C. Be
D. Mg
Hòa tan 8,0 gam hỗn hợp gồm Ca và oxit RO (R có hóa trị không đổi) cần dùng 200 ml dung dịch HCl 2M. Kim loại R là:
A. Cu
B. Mg
C. Ba
D. Be
Hòa tan 8,0 gam hỗn hợp gồm Ca và oxit RO (R có hóa trị không đổi) cần dùng 200 ml dung dịch HCl 2M. Kim loại R là A. Cu B. Mg C. Ba D. Be.
Đọc tiếp
Hòa tan 8,0 gam hỗn hợp gồm Ca và oxit RO (R có hóa trị không đổi) cần dùng 200 ml dung dịch HCl 2M. Kim loại R là
A. Cu
B. Mg
C. Ba
D. Be.
Cho 11,6 gam hỗn hợp gồm oxit và muối cacbonat của kim loại kiềm R. Hòa tan hết hỗn hợp trên cần vừa đủ 0,2 mol HCl. Kim loại R là A. Na. B. Li. C. Cs. D. K.
Đọc tiếp
Cho 11,6 gam hỗn hợp gồm oxit và muối cacbonat của kim loại kiềm R. Hòa tan hết hỗn hợp trên cần vừa đủ 0,2 mol HCl. Kim loại R là
A. Na.
B. Li.
C. Cs.
D. K.
Chọn đáp án D
R 2 O + 2HCl → 2RCl + H 2 O
x 2x mol
R 2 C O 3 + 2HCl → 2RCl + C O 2 + H 2 O
y 2y mol
Theo bài ra: n H C l = 2x + 2y = 0,2 → x + y = nhh = 0,1 mol
M h h = 11 , 6 0 , 1 (g/mol)
→ 2 M R + 16 < 116 < 2 M R + 60 → 28 < M R < 50. Vậy R là K.
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn m gam hỗn hợp E gồm Sn và một kim loại R (có hóa trị không đổi) trong lượng dư dung dịch HCl, thu được 5,04 lít khí H2 (đktc) và dung dịch chứa 36,27 gam muối. Mặt khác, để đốt cháy cũng m gam hỗn hợp E cần vừa đủ 3,696 lít O2 (đktc). Kim loại R là A. Al B. Zn C. Ca C. Ca
Đọc tiếp
Hòa tan hoàn toàn m gam hỗn hợp E gồm Sn và một kim loại R (có hóa trị không đổi) trong lượng dư dung dịch HCl, thu được 5,04 lít khí H2 (đktc) và dung dịch chứa 36,27 gam muối. Mặt khác, để đốt cháy cũng m gam hỗn hợp E cần vừa đủ 3,696 lít O2 (đktc). Kim loại R là
A. Al
B. Zn
C. Ca
C. Ca
Gọi hóa trị của R là n và số mol Sn và R lần lượt là a và b mol
+/ Khi phản ứng với HCl :
Sn + HCl → SnCl2 + H2
R + nHCl → RCln + 0,5nH2
+/ Khi đốt trong oxi :
Sn + O2 → SnO2
2R + 0,5nO2 → R2On
=> Ta có : nH2 = a + 0,5nb = 0,225 mol
Và nO2 = a + 0,25nb = 0,165 mol
=> a = 0,105 mol ; nb = 0,24 mol
Có mmuối = 0,105.190 + 0,24/n . (R + 35,5n) = 36,27
=>R = 32,5n
=>Cặp n =2 ; R =65 (Zn) thỏa mãn
=>B
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 1g oxit của kim loại R cần dùng 25ml dung dịch gồm hỗn hợp H2SO4 và axit HCl 1M . Tính công thức hóa học của oxit trên