Thả 2 miếng Al kim loại vào 3 cốc đựng 3 dung dịch
a, Dung dịch HNO3
b, dung dịch NaOH
c, dung dịch FeCl2 có mặt HCl dư
Thực hiện các thí nghiệm sau:
(1) Cho kim loại K vào dung dịch HCl.
(2) Đốt bột Al trong khí Cl2.
(3) Cho Na2CO3 vào dung dịch AlCl3.
(4) Cho NaOH vào dung dịch Mg(NO3)2.
(5) Điện phân Al2O3 nóng chảy, có mặt Na3AlF6.
(6) Cho FeCl2 tác dụng với dung dịch AgNO3 dư.
Số thí nghiệm có phản ứng oxi hoá – khử xảy ra là
A. 5.
B. 2
C. 4
D. 3
Đáp án C.
(1) 2K + 2HCl ® 2KCl + H2.
(2) 2Al + 3Cl2 ® 2AlCl3
(3) 3Na2CO3 + 2AlCl3 + 3H2O ® 2Al(OH)3 + 3CO2 + 6NaCl.
(4) 2NaOH + Mg(NO3)2 ® Mg(OH)2 + NaNO3.
(5) 2Al2O3 → 4Al + 3O2.
(6) FeCl2 + 3AgNO3 ® Fe(NO3)3 + 2AgCl + Ag.
Thực hiện các thí nghiệm sau:
(1) Cho kim loại K vào dung dịch HCl.
(2) Đốt bột Al trong khí Cl2.
(3) Cho Na2CO3 vào dung dịch AlCl3.
(4) Cho NaOH vào dung dịch Mg(NO3)2.
(5) Điện phân Al2O3 nóng chảy, có mặt Na3AlF6.
(6) Cho FeCl2 tác dụng với dung dịch AgNO3 dư.
Số thí nghiệm có phản ứng oxi hoá – khử xảy ra là
A. 5
B. 2
C. 4
D. 3
Chọn C.
(1) 2K + 2HCl ® 2KCl + H2.
(2) 2Al + 3Cl2 ® 2AlCl3
(3) 3Na2CO3 + 2AlCl3 + 3H2O ® 2Al(OH)3 + 3CO2 + 6NaCl.
(4) 2NaOH + Mg(NO3)2 ® Mg(OH)2 + NaNO3.
![]()
(6) FeCl2 + 3AgNO3 ® Fe(NO3)3 + 2AgCl + Ag.
Phân biệt các chất 1) Dung dịch: HCl, HNO3, K2SO4, NaOH 2) Các kim loại: Fe, Al, Cu 3) Dung dịch: KOH, Ba(OH)2, HCl, HNO3 4) Dung dịch: HCl, NaOH, NaCl, H2SO4
1. - Trích mẫu thử.
- Nhỏ từng mẫu thử vào giấy quỳ tím.
+ Quỳ hóa đỏ: HCl, HNO3 (1)
+ Quỳ hóa xanh: NaOH
+ Quỳ không đổi màu: K2SO4
- Cho mẫu thử nhóm (1) pư với dd AgNO3.
+ Có tủa trắng: HCl
PT: \(HCl+AgNO_3\rightarrow HNO_3+AgCl\)
+ Không hiện tượng: HNO3
- Dán nhãn.
2. - Trích mẫu thử.
- Cho từng mẫu thử pư với dd HCl.
+ Tan, có khí thoát ra: Fe, Al (1)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
+ Không hiện tượng: Cu
- Cho mẫu thử nhóm (1) pư với dd NaOH.
+ Tan, có khí thoát ra: Al
PT: \(2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2\)
+ Không tan: Fe.
- Dán nhãn.
3. - Trích mẫu thử.
- Nhỏ vài giọt từng mẫu thử vào giấy quỳ tím.
+ Quỳ tím hóa xanh: KOH, Ba(OH)2 (1)
+ Quỳ hóa đỏ: HCl, HNO3 (2)
- Cho mẫu thử nhóm (1) pư với K2SO4
+ Có tủa trắng: \(K_2SO_4+Ba\left(OH\right)_2+2KOH+BaSO_4\)
+ Không hiện tượng: KOH
- Cho mẫu thử nhóm (2) pư với dd AgNO3.
+ Có tủa trắng: HCl
PT: \(HCl+AgNO_3\rightarrow HNO_3+AgCl\)
+ Không hiện tượng: HNO3
- Dán nhãn.
4. - Trích mẫu thử.
- Nhỏ từng mẫu thử vào giấy quỳ tím.
+ Quỳ hóa đỏ: HCl, H2SO4 (1)
+ Quỳ hóa xanh: NaOH
+ Quỳ không đổi màu: NaCl
- Cho mẫu thử nhóm (1) pư với dd BaCl2
+ Có tủa trắng: H2SO4
PT: \(H_2SO_4+BaCl_2\rightarrow2HCl+BaSO_4\)
+ Không hiện tượng: HCl
- Dán nhãn.
Thực hiện các thí nghiệm sau:
(a) Cho dung dịch HCl vào dung dịch Fe(NO3)3;
(b) Cho FeS vào dung dịch HCl;
(c) Cho dung dịch AgNO3 vào dung dịch Fe(NO3)2;
(d) Cho Al vào dung dịch NaOH;
(e) Cho dung dịch NaOH vào dung dịch NaHCO3
(f) Cho kim loại Cu vào dung dịch FeCl3.
Số thí nghiệm có xảy ra phản ứng là
A. 6
B. 4
C. 5
D. 3
Đáp án C
(a) Không xảy ra.
(b) FeS + HCl ® FeCl2 + H2S
(c) AgNO3 + Fe(NO3)2 ® Fe(NO3)3 + Ag
(d) 2Al + 2NaOH + 2H2O ® 2NaAlO2 + 3H2
(e) NaOH + NaHCO3 ® Na2CO3 + H2O
(f) Cu + 2FeCl3 ® CuCl2 + 2FeCl2
Thực hiện các thí nghiệm sau:
(a) Cho dung dịch HCl vào dung dịch Fe(NO3)3; (b) Cho FeS vào dung dịch HCl;
(c) Cho dung dịch AgNO3 vào dung dịch Fe(NO3)2; (d) Cho Al vào dung dịch NaOH;
(e) Cho dung dịch NaOH vào dung dịch NaHCO3; (f) Cho kim loại Cu vào dung dịch FeCl3.
Số thí nghiệm có xảy ra phản ứng là
A. 6.
B. 4.
C. 5.
D. 3.
Chọn C.
(a) Không xảy ra.
(b) FeS + HCl ® FeCl2 + H2S
(c) AgNO3 + Fe(NO3)2 ® Fe(NO3)3 + Ag
(d) 2Al + 2NaOH + 2H2O ® 2NaAlO2 + 3H2
(e) NaOH + NaHCO3 ® Na2CO3 + H2O
(f) Cu + 2FeCl3 ® CuCl2 + 2FeCl2
Cho các nhận xét sau:
(1) Al và Cr đều tác dụng được với dung dịch HCl và dung dịch NaOH.
(2) Dẫn khí CO2 đến dư vào dung dịch Ca(OH)2 thì cuối cùng thu được kết tủa.
(3) Kim loại dẫn điện tốt nhất là Au.
(4) Thêm NaOH vào dung dịch FeCl2 thì thu được kết tủa màu trắng xanh.
(5) Để phân biệt Al và Al2O3 ta có thể dùng dung dịch NaOH.
Số nhận xét không đúng là
![]()
![]()
![]()
![]()
Cho các nhận xét sau:
(1) Al và Cr đều tác dụng được với dung dịch HCl và dung dịch NaOH.
(2) Dẫn khí CO2 đến dư vào dung dịch Ca(OH)2 thì cuối cùng thu được kết tủa.
(3) Kim loại dẫn điện tốt nhất là Au.
(4) Thêm NaOH vào dung dịch FeCl2 thì thu được kết tủa màu trắng xanh.
(5) Để phân biệt Al và Al2O3 ta có thể dùng dung dịch NaOH.
Số nhận xét không đúng là
A. 3.
B. 2.
C. 5.
D. 4.
Đáp án A
(1) Sai vì Cr không tác dụng được với dung dịch NaOH.
(2) Sai vì CO2 dư thì Ca(OH)2 + 2CO2 → Ca(HCO3)2 ⇒ không thu được ↓.
(3) Sai vì kim loại dẫn điện tốt nhất là Ag.
(4) Đúng vì: FeCl2 + 2NaOH → 2NaCl + Fe(OH)2↓ (trắng xanh).
(5) Đúng vì: 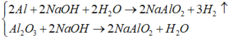
⇒ sủi bọt khí không màu là Al, còn lại là Al2O3.
||⇒ (1), (2) và (3) sai ⇒ chọn A.
Cho các nhận xét sau:
(1) Al và Cr đều tác dụng được với dung dịch HCl và dung dịch NaOH.
(2) Dẫn khí C O 2 đến dư vào dung dịch C a ( O H ) 2 thì cuối cùng thu được kết tủa.
(3) Kim loại dẫn điện tốt nhất là Au.
(4) Thêm NaOH vào dung dịch F e C l 2 thì thu được kết tủa màu trắng xanh.
(5) Để phân biệt Al và A l 2 O 3 ta có thể dùng dung dịch NaOH.
Số nhận xét không đúng là
A. 3.
B. 2.
C. 5.
D. 4.
Cho các nhận xét sau:
(1) Al và Cr đều tác dụng được với dung dịch HCl và dung dịch NaOH.
(2) Dẫn khí CO2 đến dư vào dung dịch Ca(OH)2 thì cuối cùng thu được kết tủa.
(3) Kim loại dẫn điện tốt nhất là Au.
(4) Thêm NaOH vào dung dịch FeCl2 thì thu được kết tủa màu trắng xanh.
(5) Để phân biệt Al và Al2O3 ta có thể dùng dung dịch NaOH.
Số nhận xét không đúng là
A.3
B.2
C.5
D.4