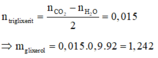giữa NaHCO3, NH4H2PO4, Mg(HCO3)2 cùng ở một điều kiện 90 độ C, áp suất 1 atm, và số khối lượng bằng nhau thì chất nào kết thúc phản ứng nhiệt phân nhanh nhất? Chất nào sinh ra khối lượng H2O nhiều nhất?

Những câu hỏi liên quan
Biết ở điều kiện tiêu chuẩn, khối lượng riêng của ôxi là
1
,
43
k
g
/
m
3
+
. Khối lượng khí ôxi đựng trong một bình kín có thể tích 15 lít dưới áp suất 150 atm ở nhiệt độ
0
o
C
bằng A. 3,22 kg B. 214,5 kg. C. 7,5 kg D. 2,25 kg
Đọc tiếp
Biết ở điều kiện tiêu chuẩn, khối lượng riêng của ôxi là 1 , 43 k g / m 3 + . Khối lượng khí ôxi đựng trong một bình kín có thể tích 15 lít dưới áp suất 150 atm ở nhiệt độ 0 o C bằng
A. 3,22 kg
B. 214,5 kg.
C. 7,5 kg
D. 2,25 kg
Chọn A.

Ở điều kiện tiêu chuẩn (1 atm, 0 o C ), khối lượng riêng của ôxi là: p 0 = m / V 0
Ở điều kiện 150 atm, 0 o C , khối lượng riêng của ôxi là: ρ = m/V.
Do đó: m = p 0 . V 0 = ρ.V (1)
Do nhiệt độ không đổi, theo định luật Bôi-lơ – Ma-ri-ốt: p 0 . V 0 = pV (2)
Từ (1) và (2) suy ra:
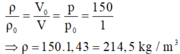
Và m = ρ . V = 214,5.15.10 − 3 ≈ 3,22 k g
Đúng 0
Bình luận (0)
Biết ở điều kiện tiêu chuẩn, khối lượng riêng của ôxi là 1,43 kg/
m
3
+
. Khối lượng khí ôxi đựng trong một bình kín có thể tích 15 lít dưới áp suất 150 atm ở nhiệt độ
0
o
C
bằng A. 3,22 kg B. 214,5 kg C. 7,5 kg D. 2,25 kg.
Đọc tiếp
Biết ở điều kiện tiêu chuẩn, khối lượng riêng của ôxi là 1,43 kg/ m 3 + . Khối lượng khí ôxi đựng trong một bình kín có thể tích 15 lít dưới áp suất 150 atm ở nhiệt độ 0 o C bằng
A. 3,22 kg
B. 214,5 kg
C. 7,5 kg
D. 2,25 kg.
Chọn A.

Ở điều kiện tiêu chuẩn (1 atm, 0 o C ), khối lượng riêng của ôxi là: p 0 = m/ V 0 .
Ở điều kiện 150 atm, 0 o C , khối lượng riêng của ôxi là: ρ = m/V.
Do đó: m = p 0 V 0 = ρ.V (1)
Do nhiệt độ không đổi, theo định luật Bôi-lơ – Ma-ri-ốt: p 0 V 0 = pV (2)
Từ (1) và (2) suy ra:
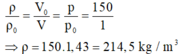
Và m = ρ . V = 214,5.15.10 − 3 ≈ 3,22 k g
Đúng 0
Bình luận (0)
Biết ở điều kiện tiêu chuẩn, khối lượng riêng của ôxi là
1
,
43
k
g
/
m
3
. Khối lượng khí ôxi đựng trong một bình kín có thể tích 15 lít dưới áp suất 150 atm ở nhiệt độ 0 bằng A. 3,23 kg. B. 214,5 kg. C. 7,5 kg. D. 2,25 kg.
Đọc tiếp
Biết ở điều kiện tiêu chuẩn, khối lượng riêng của ôxi là 1 , 43 k g / m 3 . Khối lượng khí ôxi đựng trong một bình kín có thể tích 15 lít dưới áp suất 150 atm ở nhiệt độ 0 bằng
A. 3,23 kg.
B. 214,5 kg.
C. 7,5 kg.
D. 2,25 kg.
Chọn A.
Ở điều kiện tiêu chuẩn (1 atm, 0 oC), khối lượng riêng của ôxi là: ρ0 = m/V0.
Ở điều kiện 150 atm, 0 oC, khối lượng riêng của ôxi là: ρ = m/V.
Do đó: m = ρ0.V0 = ρ.V (1)
Do nhiệt độ không đổi, theo định luật Bôi-lơ – Ma-ri-ốt: p0V0 = pV (2)
Từ (1) và (2) suy ra:
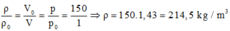
Và m = ρ.V = 214,5.15-3 ≈ 3,23 kg.
Đúng 0
Bình luận (0)
Trong cùng điều kiện nhiệt độ và áp suất, 1 lít hơi anđehit A có khối lượng bằng khối lượng 1 lít CO2. A là
A. anđehit fomic
B. anđehit benzoic
C. anđehit axetic
D. anđehit acrylic.
Giải thích: Đáp án C
![]() Công thức của anđehit là R(CHO)n → n < 2.
Công thức của anđehit là R(CHO)n → n < 2.
n = 1 → R = 15 → R là CH3. A là anđehit axetic.
Đúng 0
Bình luận (0)
Trong cùng điều kiện nhiệt độ và áp suất, 1 lít hơi anđehit A có khối lượng bằng khối lượng 1 lít CO2. A là A. anđehit fomic B. anđehit benzoic C. anđehit axetic D. anđehit acrylic
Đọc tiếp
Trong cùng điều kiện nhiệt độ và áp suất, 1 lít hơi anđehit A có khối lượng bằng khối lượng 1 lít CO2. A là
A. anđehit fomic
B. anđehit benzoic
C. anđehit axetic
D. anđehit acrylic
Đáp án C
m A = m C O 2 ; n A = n C O 2 ⇒ M A = M C O 2 = 44 . Công thức của anđehit là R(CHO)n → n < 2.
n = 1 → R = 15 → R là CH3. A là anđehit axetic
Đúng 0
Bình luận (0)
Một bình chứa một lượng khí ở nhiệt độ 27 và áp suất 30 atm. Nếu giảm nhiệt độ xuống còn 10 và để một nửa lượng khí thoát ra ngoài thì áp suất khí còn lại trong bình bằng A. 2 atm. B. 14,15 atm. C. 15 atm. D. 1,8 atm.
Đọc tiếp
Một bình chứa một lượng khí ở nhiệt độ 27 và áp suất 30 atm. Nếu giảm nhiệt độ xuống còn 10 và để một nửa lượng khí thoát ra ngoài thì áp suất khí còn lại trong bình bằng
A. 2 atm.
B. 14,15 atm.
C. 15 atm.
D. 1,8 atm.
Chọn B.
Xét lượng khí còn lại trong bình:
Trạng thái 1: V1 = V/2; T1 = 300 K; p1 = 30 atm.
Trạng thái 2: V2 = V; T2 = 283 K; p2 = ?
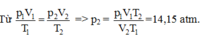
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn m gam chất béo X (chứa axit stearic, axit panmitic và các triglixerit của các axit này). Sau phản ứng thu được 20,16 lít CO2 (điều kiện tiêu chuẩn) và 15,66 gam nước. Xà phòng hóa m gam X (hiệu suất phản ứng bằng 90%) thì thu được khối lượng glixerol là A. 2,484 gam B. 1,242 gam C. 1,380 gam D. 2,760 gam
Đọc tiếp
Đốt cháy hoàn toàn m gam chất béo X (chứa axit stearic, axit panmitic và các triglixerit của các axit này). Sau phản ứng thu được 20,16 lít CO2 (điều kiện tiêu chuẩn) và 15,66 gam nước. Xà phòng hóa m gam X (hiệu suất phản ứng bằng 90%) thì thu được khối lượng glixerol là
A. 2,484 gam
B. 1,242 gam
C. 1,380 gam
D. 2,760 gam
Một khí khi đặt ở điều kiện nhiệt độ không đổi thì có sự biến thiên của thể tích theo áp suất như hình V.2. Khi áp suất có giá trị
500
N
/
m
2
thì thể tích khối khí bằng A.
3
,
6
m
3
B.
4
,
8
m
3
C.
1...
Đọc tiếp
Một khí khi đặt ở điều kiện nhiệt độ không đổi thì có sự biến thiên của thể tích theo áp suất như hình V.2. Khi áp suất có giá trị 500 N / m 2 thì thể tích khối khí bằng
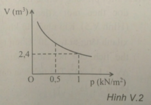
A. 3 , 6 m 3
B. 4 , 8 m 3
C. 1 , 2 m 3
D. 20 m 3
Chọn B.
Áp dụng phương trình trạng thái ta được:
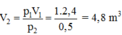
Đúng 0
Bình luận (0)
Một khí khi đặt ở điều kiện nhiệt độ không đổi thì có sự biến thiên của thể tích theo áp suất như hình V.2. Khi áp suất có giá trị 500 N/
m
2
thì thể tích khối khí bằng A. 3,6
m
3
. B. 4,8
m
3
C. 1,2
m
3
. D. 20
m
3
Đọc tiếp
Một khí khi đặt ở điều kiện nhiệt độ không đổi thì có sự biến thiên của thể tích theo áp suất như hình V.2. Khi áp suất có giá trị 500 N/ m 2 thì thể tích khối khí bằng
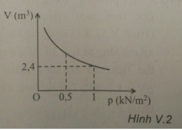
A. 3,6 m 3 .
B. 4,8 m 3
C. 1,2 m 3 .
D. 20 m 3
Chọn B.
Áp dụng phương trình trạng thái ta được:
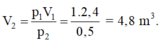
Đúng 0
Bình luận (0)