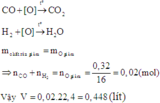Dẫn từ từ V (1) hỗn hợp X (đktc) gồm (CO và H2) qua ống nghiệm 16,8 g hỗn hợp (CuO,Fe3O4,Fe2O3) nung nóng . phản ứng hòan tòan thu được hỗn hợp khí nặng hơn hỗn hợp ban đầu 0,32g .Tính V ? (O = 16)

Những câu hỏi liên quan
dẫn từ từ V liít hỗn họp X (đktc) gồm CO và H2 qua ống dẫn chứa hỗn hợp gồm CuO,Fe2O3, Fe3O4 nung nóng. Phản ứng hoàn toàn thu được hỗn hợp khí và hơi có khối lượng nặng hơn hỗn hợp khí ban đầu là 0,32gam. viết PTHH xảy ra và tính V
m(tăng) = mO = 0,32 (g)
nO = 0,32/16 = 0,02 (mol)
=> nhh khí = 0,02 (mol)
=> Vhh khí = 0,02 . 22,4 = 0,448 (l)
Đúng 1
Bình luận (2)
Cho từ từ V lít hỗn hợp khí CO, H2 đi qua ống sứ đựng 16,8 gam hỗn hợp 3 oxit CuO, Fe2O3, Al2O3. Sau phản ứng hoàn toàn thu được hỗn hợp khí và hơi nặng hơn hỗn hợp CO, H2 ban đầu 0,32g. Giá trị của V và khối lượng chất rắn còn lại trong ống sứ sau khi nung nóng lần lượt là A. 4,48 lít và 13,6g. B. 0,448 lít và 16,48g. C. 0,336 lít và 16,56g. D. 0,112 lít và 16g.
Đọc tiếp
Cho từ từ V lít hỗn hợp khí CO, H2 đi qua ống sứ đựng 16,8 gam hỗn hợp 3 oxit CuO, Fe2O3, Al2O3. Sau phản ứng hoàn toàn thu được hỗn hợp khí và hơi nặng hơn hỗn hợp CO, H2 ban đầu 0,32g. Giá trị của V và khối lượng chất rắn còn lại trong ống sứ sau khi nung nóng lần lượt là
A. 4,48 lít và 13,6g.
B. 0,448 lít và 16,48g.
C. 0,336 lít và 16,56g.
D. 0,112 lít và 16g.
Ta có thể tổng quát các phản ứng như sau:
![]()
Quan sát 2 phản ứng trên, ta nhận thấy: khối lượng hỗn hợp khí và hơi thu được sau phản ứng nặng hơn hỗn hợp CO, H2 ban đầu là do H2, CO đã "chiếm lấy" những nguyên tử O trong oxit.
Khi đó khối lượng hỗn hợp khí tăng lên chính là khối lượng mà chất rắn đã giảm đi sau phản ứng hay khối lượng này chính là khối lượng của những nguyên tử oxi trong oxit bị "chiếm mất".
Suy ra m c h ấ t r ắ n p h ả n ứ n g - m o x i b a n đ ầ u - 0 , 32 = 16 , 48 ( g a m )
Cũng quan sát các phản ứng hoặc sử dụng định luật BTNT đối với C, H, có:
![]()
Đáp án B.
Đúng 0
Bình luận (0)
Thổi từ từ V lít hỗn hợp khí (đktc) gồm CO và H2 đi qua ống đựng 16,8 gam hỗn hợp 3 oxit CuO, Fe3O4, Al2O3 nung nóng, phản ứng hoàn toàn. Sau phản ứng thu được m gam chất rắn và một hỗn hợp khí nặng hơn khối lượng của hỗn hợp V là 0,32 gam. Tính V và m A. 0,224 lít và 14,48 gam B. 0,672 lít và 18,46 gam C. 0,112 lít và 12,28 gam D. 0,448 lít và 16,48 gam
Đọc tiếp
Thổi từ từ V lít hỗn hợp khí (đktc) gồm CO và H2 đi qua ống đựng 16,8 gam hỗn hợp 3 oxit CuO, Fe3O4, Al2O3 nung nóng, phản ứng hoàn toàn. Sau phản ứng thu được m gam chất rắn và một hỗn hợp khí nặng hơn khối lượng của hỗn hợp V là 0,32 gam. Tính V và m
A. 0,224 lít và 14,48 gam
B. 0,672 lít và 18,46 gam
C. 0,112 lít và 12,28 gam
D. 0,448 lít và 16,48 gam
Đáp án D.
Ta có: mO = 0,32 (g) ⟹ nO = 0 , 32 16 = 0,02 (mol) nên số mol của hỗn hợp CO, H2 cũng bằng 0,02 (mol) ⟹ V = 0,02.22,4 = 0,448 (l).
Theo định luật bảo toàn khối lượng, m = 16,8 – 0,02.16 = 16,48 (g).
Đúng 0
Bình luận (0)
Dẫn từ từ V lít hỗn hợp X (đktc) gồm CO và H2 qua ống chứa hỗn hợp gồm CuO, Fe2O3,Fe3O4 nung nóng. Phản ứng hoàn toàn thu được hỗn hợp khí và hơi có khối lượng nặng hơn hỗn hợp khí ban đầu là 0,32g. Viết các phương trình phản ứng xảy ra và tính V.
bài 1: Hỗn hợp X gồm: CuO, FeO, và Fe3O4. Dẫn V lít khí CO dư (đktc) đi qua ống đựng m gam hỗn hợp X nung nóng. Sau khi kết thúc thí nghiệm, thu được 54 gam chất rắn Y trong ống sứ và 11,2 lít hỗn hợp khí A (đktc) có tỉ khối hơi so với H2 là 20,4.a/Viết PTHH.b/ Tính khối lượng mỗi khí trong hỗn hợp A.c/ Tính V, m.bài 2: Đốt cháy hoàn toàn 44,8 gam hỗn hợp gồm FeS và FeS2 trong V lít không khí (đktc) vừa đủ (không khí có 20% thể tích là O2, 80% thể tích là N2), thu được m gam Fe2O3 và V’ lít hỗn...
Đọc tiếp
bài 1: Hỗn hợp X gồm: CuO, FeO, và Fe3O4. Dẫn V lít khí CO dư (đktc) đi qua ống đựng m gam hỗn hợp X nung nóng. Sau khi kết thúc thí nghiệm, thu được 54 gam chất rắn Y trong ống sứ và 11,2 lít hỗn hợp khí A (đktc) có tỉ khối hơi so với H2 là 20,4.
a/Viết PTHH.
b/ Tính khối lượng mỗi khí trong hỗn hợp A.
c/ Tính V, m.
bài 2: Đốt cháy hoàn toàn 44,8 gam hỗn hợp gồm FeS và FeS2 trong V lít không khí (đktc) vừa đủ (không khí có 20% thể tích là O2, 80% thể tích là N2), thu được m gam Fe2O3 và V’ lít hỗn hợp khí (đktc) gồm N2 và SO2, trong đó SO2 chiếm 14,89% về thể tích.
a/ Viết PTHH.
b/ Tìm V.
c/ Tính khối lượng từng chất trong hỗn hợp đầu.
d/ Tìm m.
bài 3: Cacnalit là một loại muối có công thức là KCl.MgCl2.xH2O. Nung 33,3 gam muối đó tới khối lượng không đổi thì thu được 20,34 g muối khan.
a/ Tìm x.
b/ Tính số nguyên tử clo có trong 33,3 gam cacnalit.
Dẫn 11,2 lít (đktc) hỗn hợp X gồm CO và
C
O
2
(có tỉ khối so với
H
2
bằng 15,6) qua ống đựng hỗn hợp chất rắn gồm CuO,
F
e
2
O
3
nung nóng, thu được hỗn hợp khí Y (có tỉ khối so với H2 bằng 18). Khối lượng chất rắn còn lại sau phản ứng đã giảm đi so với ban đầu là A. 1,6 gam B. 3,2 gam C. 2,4 gam D. 4,8 gam
Đọc tiếp
Dẫn 11,2 lít (đktc) hỗn hợp X gồm CO và C O 2 (có tỉ khối so với H 2 bằng 15,6) qua ống đựng hỗn hợp chất rắn gồm CuO, F e 2 O 3 nung nóng, thu được hỗn hợp khí Y (có tỉ khối so với H2 bằng 18). Khối lượng chất rắn còn lại sau phản ứng đã giảm đi so với ban đầu là
A. 1,6 gam
B. 3,2 gam
C. 2,4 gam
D. 4,8 gam
Thổi từ từ V lít hỗn hợp CO và H2 đi qua ống sứ nung nóng đựng hỗn hợp CuO, ZnO, Fe2O3, Al2O3. Sau phản ứng thu được V lít (đktc) hỗn hợp khí và hơi nặng hơn hỗn hợp khí ban đầu là 0,64 gam. Giá trị của V là
Xem chi tiết
- Đề không nói rằng hỗn hợp khí ban đầu có dư hay là không nên mình cho rằng hỗn hợp khi sau phản ứng chỉ có thể gồm CO2 và H2O (tức là CO và H2 hết )( chỉ như vậy mới tính được thôi)
- Nhắc lại kiến thức : Phương pháp nhiệt luyện: Dùng chất khử như CO, H2, C hoặc kim loại (Al) có thể khử ion kim loại trong oxit ở nhiệt độ cao... Bằng phương pháp này, người ta có thể điều chế được những kim loại có tính khử yếu và trung bình" (Kim loại đứng sau Al)
- Khối lượng tăng lên do H2 và CO đã lấy mất O2− trong hỗn hợp ( nói chính xác hơn O2− trong CuO và Fe2O3)
- Lời giải :
PTHH:
H2 + O2− \(\rightarrow\) H2O
CO + O2− \(\rightarrow\) CO2
\(\rightarrow\) nhỗnhợpkhí = nO2− =\(\frac{0,64}{16}\) = 0,04 mol
\(\rightarrow\) V = 22,4 . 0,04 = 0,896 l
Thổi từ từ V lít hỗn hợp khí (đktc) gồm CO và H2 đi qua một ống đựng 16,8 gam hỗn hợp 3 oxit: CuO, Fe3O4, Al2O3 nung nóng, phản ứng hoàn toàn. Sau phản ứng thu được m gam chất rắn và một hỗn hợp khí và hơi nặng hơn khối lượng của hỗn hợp V là 0,32 gam. Tính V và m.
[VIết phương trình hóa học ra]
(Al2O3 không bị khử bởi CO và H2 ở nhiệt độ cao)
Ta thấy, trong quá trình phản ứng thì hai oxit bị khử mất đi ngyên tử oxi trong công thức phân tử tạo thành kim loại.
Và khí sinh ra sau phản ứng theo đề cho nặng hơn khối lượng hỗn hợp khí ban đầu là 0,32 gam.
=> 0,32 gam này là khối lượng của nguyên tử oxi có trong 2 oxit bị khử là CuO và Fe3O4
=> Khối lượng chất rắn thu được sau phản ứng là:
\(m chất rắn = 16,8 - 0,32 = 16,48(g)\)
Vậy \(m = 16,48 (g)\)
Ta có: \(n_{hh}=n_O=\dfrac{0,32}{16}=0,02\left(mol\right)\)
\(\Rightarrow V\left(đktc\right)=0,448\left(l\right)\)
Đúng 0
Bình luận (0)
Cho V lít hỗn hợp khí (đktc) gồm CO và H2 phản ứng với một lượng dư hỗn hợp rắn gồm CuO và Fe3O4 nung nóng, Sau khi các phản ứng xảy ra hoàn toàn, khối lượng hỗn hợp rắn giảm 0,32g. Giá trị của V là: A. 0,224. B. 0,448. C. 0,112 D. 0,560.
Đọc tiếp
Cho V lít hỗn hợp khí (đktc) gồm CO và H2 phản ứng với một lượng dư hỗn hợp rắn gồm CuO và Fe3O4 nung nóng, Sau khi các phản ứng xảy ra hoàn toàn, khối lượng hỗn hợp rắn giảm 0,32g. Giá trị của V là:
A. 0,224.
B. 0,448.
C. 0,112
D. 0,560.