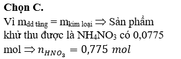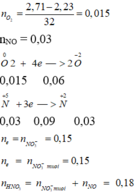x gồm 0.1 mol Mg, 0.04 mol Al, 0.15 mol Zn, X+ Hno3 loãn dư, sau pư m tăng 13,23g. tinh số mol hno3

Những câu hỏi liên quan
Hỗn hợp X gồm Mg ( 0,10 mol); Al ( 0,04 mol) và Zn ( 0,15 mol). Cho X tác dụng với dung dịch HNO3 loãng ( dư), sau phản ứng khối lượng dung dịch tăng 13,23 gam. Số mol HNO3 tham gia phản ứng là
A. 0,7750 mol.
B. 0,6975 mol.
C. 0,6200 mol.
D. 1,2400 mol.
Đáp án A
mKL = 0,1.24 + 0,04.27 + 0,15.65 = 13,23 (g) đúng bằng khối lượng dung dịch tăng
=> KL + HNO3 chỉ tạo muối NH4+
=> nNH4+ = 1/8 ne(KL nhường) = 1/ 8 . ( 0,1.2 + 0,04.3 + 0,15.2) = 0,0775 (mol)
=> nHNO3 PƯ = 10nNH4+ = 0,775 (mol)
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Mg (0,10 mol), Al (0,04 mol) và Zn (0,15 mol). Cho X tác dụng với dung dịch HNO3 loãng (dư), sau phản ứng khối lượng dung dịch tăng 13,23 gam. Số mol HNO3 tham gia phản ứng là: A. 0,6200 mol. B. 1,2400 mol. C. 0,6975 mol. D. 0,7750 mol.
Đọc tiếp
Hỗn hợp X gồm Mg (0,10 mol), Al (0,04 mol) và Zn (0,15 mol). Cho X tác dụng với dung dịch HNO3 loãng (dư), sau phản ứng khối lượng dung dịch tăng 13,23 gam. Số mol HNO3 tham gia phản ứng là:
A. 0,6200 mol.
B. 1,2400 mol.
C. 0,6975 mol.
D. 0,7750 mol.
Hỗn hợp X gồm Mg ( 0,10 mol); Al ( 0,04 mol) và Zn ( 0,15 mol). Cho X tác dụng với dung dịch HNO3 loãng (dư), sau phản ứng khối lượng dung dịch tăng 13,23 gam. Số mol HNO3 tham gia phản ứng là A. 0,7750 mol. B. 0,6975 mol. C. 0,6200 mol. D. 1,2400 mol.
Đọc tiếp
Hỗn hợp X gồm Mg ( 0,10 mol); Al ( 0,04 mol) và Zn ( 0,15 mol). Cho X tác dụng với dung dịch HNO3 loãng (dư), sau phản ứng khối lượng dung dịch tăng 13,23 gam. Số mol HNO3 tham gia phản ứng là
A. 0,7750 mol.
B. 0,6975 mol.
C. 0,6200 mol.
D. 1,2400 mol.
Giải thích: Đáp án A
mKL = 0,1.24 + 0,04.27 + 0,15.65 = 13,23 (g) đúng bằng khối lượng dung dịch tăng
=> KL + HNO3 chỉ tạo muối NH4+
=> nNH4+ = 1/8 ne(KL nhường) = 1/ 8 . ( 0,1.2 + 0,04.3 + 0,15.2) = 0,0775 (mol)
=> nHNO3 PƯ = 10nNH4+ = 0,775 (mol)
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Mg ( 0,10 mol); Al ( 0,04 mol) và Zn ( 0,15 mol). Cho X tác dụng với dung dịch HNO3 loãng ( dư), sau phản ứng khối lượng dung dịch tăng 13,23 gam. Số mol HNO3 tham gia phản ứng là A. 0,7750 mol B. 0,6975 mol C. 0,6200 mol D. 1,2400 mol
Đọc tiếp
Hỗn hợp X gồm Mg ( 0,10 mol); Al ( 0,04 mol) và Zn ( 0,15 mol). Cho X tác dụng với dung dịch HNO3 loãng ( dư), sau phản ứng khối lượng dung dịch tăng 13,23 gam. Số mol HNO3 tham gia phản ứng là
A. 0,7750 mol
B. 0,6975 mol
C. 0,6200 mol
D. 1,2400 mol
Đáp án A
mKL = 0,1.24 + 0,04.27 + 0,15.65 = 13,23 (g)
đúng bằng khối lượng dung dịch tăng
=> KL + HNO3 chỉ tạo muối NH4+
=> nNH4+ = 1/8 ne(KL nhường)
= 1/ 8 . ( 0,1.2 + 0,04.3 + 0,15.2) = 0,0775 (mol)
=> nHNO3 PƯ = 10nNH4+ = 0,775 (mol)
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Mg ( 0,10 mol); Al ( 0,04 mol) và Zn ( 0,15 mol). Cho X tác dụng với dung dịch HNO3 loãng ( dư), sau phản ứng khối lượng dung dịch tăng 13,23 gam. Số mol HNO3 tham gia phản ứng là A. 0,7750 mol B. 0,6975 mol C. 0,6200 mol D. 1,2400 mol.
Đọc tiếp
Hỗn hợp X gồm Mg ( 0,10 mol); Al ( 0,04 mol) và Zn ( 0,15 mol). Cho X tác dụng với dung dịch HNO3 loãng ( dư), sau phản ứng khối lượng dung dịch tăng 13,23 gam. Số mol HNO3 tham gia phản ứng là
A. 0,7750 mol
B. 0,6975 mol
C. 0,6200 mol
D. 1,2400 mol.
Chọn A
mKL = 0,1.24 + 0,04.27 + 0,15.65 = 13,23 (g) đúng bằng khối lượng dung dịch tăng
=> KL + HNO3 chỉ tạo muối NH4+
=> nNH4+ = 1/8 ne(KL nhường) = 1/ 8 . ( 0,1.2 + 0,04.3 + 0,15.2) = 0,0775 (mol)
=> nHNO3 PƯ = 10nNH4+ = 0,775 (mol)
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Mg (0,10 mol), Al (0,04 mol) và Zn (0,15 mol). Cho X tác dụng với dung dịch HNO3 loãng (dư), sau phản ứng khối lượng dung dịch tăng 13,23 gam. Số mol HNO3 tham gia phản ứng là A. 0,6200 mol B. 0,6975 mol C. 0,7750 mol D. 1,2400 mol
Đọc tiếp
Hỗn hợp X gồm Mg (0,10 mol), Al (0,04 mol) và Zn (0,15 mol). Cho X tác dụng với dung dịch HNO3 loãng (dư), sau phản ứng khối lượng dung dịch tăng 13,23 gam. Số mol HNO3 tham gia phản ứng là
A. 0,6200 mol
B. 0,6975 mol
C. 0,7750 mol
D. 1,2400 mol
Cho hỗn hợp A gồm Mg (0,1 mol), Al (0,04 mol) và Zn (0,15 mol). Cho A tác dụng với dung dịch HNO3 loãng dư, sau phản ứng khối lượng dung dịch tăng 13,23 gam. Xác định HNO3 tham gia phản ứng
Nung 2,23g hh X gồm các kim loại Fe, Al, Zn, Mg trong oxi, sau một thời gian thu được 2,71g hhY. Hoà tan hoàn toàn Y vào dd HNO3 (dư), thu được 0,672 lít khí NO (sản phẩm khử duy nhất, ở đktc). Số mol HNO3 đã pư là A. 0,12. B. 0,14. C. 0,16. D. 0,18.
Đọc tiếp
Nung 2,23g hh X gồm các kim loại Fe, Al, Zn, Mg trong oxi, sau một thời gian thu được 2,71g hhY. Hoà tan hoàn toàn Y vào dd HNO3 (dư), thu được 0,672 lít khí NO (sản phẩm khử duy nhất, ở đktc). Số mol HNO3 đã pư là
A. 0,12.
B. 0,14.
C. 0,16.
D. 0,18.
Hòa tan hoàn toàn m gam hỗn hợp X gồm Al; Mg (tỉ lệ mol là 1:1) vào dung dịch HNO3 dư, thấy thoát ra hỗn hợp gồm 0,4 mol NO và 0,1 mol N2O
a, Xác định số mol HNO3 đã bị khử
b, Xác định số mol HNO3 đã tham gia phản ứng
c, Tính m
a, BTNT N, có: nHNO3 (bị khử) = nNO + 2NN2O = 0,4 + 2.0,1 = 0,6 (mol)
b, Giả sử: nAl = mMg = x (mol)
Các quá trình:
\(Al^0\rightarrow Al^{+3}+3e\)
x___________ 3x (mol)
\(Mg^0\rightarrow Mg^{+2}+2e\)
x_____________ 2x (mol)
\(N^{+5}+3e\rightarrow N^{+2}\)
_____ 1,2 __ 0,4 (mol)
\(2N^{+5}+8e\rightarrow N_2^{+1}\)
_______0,8__0,1 (mol)
Theo ĐLBT mol e, có: 3x + 2x = 1,2 + 0,8 ⇒ x = 0,4 (mol)
⇒ nAl = nMg = 0,4 (mol)
BTNT Al, có: nAl(NO3)3 = nAl = 0,4 (mol)
BTNT Mg, có: nMg(NO3)2 = nMg = 0,4 (mol)
BTNT N, có: nHNO3 (pư) = 3nAl(NO3)3 + 2nMg(NO3)2 + nNO + 2nN2O
= 3.0,4 + 2.0,4 + 0,4 + 2.0,1 = 2,6 (mol)
c, m = mAl + mMg = 0,4.27 + 0,4.24 = 20,4 (g)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)