3 mol khí oxy được chứa trong bình kín ở nhiệt độ 300k, áp suất 6atm sẽ có thể tích ?

Những câu hỏi liên quan
Một khối khí lí tưởng được đựng trong một bình kín có thể tích không đổi.khi nhiệt độ khí là 300k thì áp suất khí là 10⁵pa.để áp suất khí là 1,2.10⁵ pa thì nhiệt độ khí khi này là
Trạng thái 1: \(\left\{{}\begin{matrix}p_1=10^5Pa\\T_1=300K\end{matrix}\right.\)
Trạng thái 2: \(\left\{{}\begin{matrix}p_2=1,2\cdot10^5Pa\\T_2=???\end{matrix}\right.\)
Quá trình đẳng tích:
\(\dfrac{p_1}{T_1}=\dfrac{p_2}{T_2}\Rightarrow\dfrac{10^5}{300}=\dfrac{1,2\cdot10^5}{T_2}\)
\(\Rightarrow T_2=360K\)
Đúng 5
Bình luận (0)
Trong một bình kín dung tích 20 lít có chứa 4,4 kg khí cacbonic ở nhiệt độ 27 ° C. Tính áp suất của khí trong bình. Biết thể tích của một mol khí ở điều kiện chuẩn là V 0 = 22,4 lít.
Gọi n là số mol khí cacbonic chứa trong bình: n = m/ μ , trong đó M là khối lượng khí cacbonic có trong bình, μ là khối lượng mol của khí cacbonic.
Ta có n = 100 mol
Nếu gọi V 0 là thể tích của lượng khí cacbonic ở điều kiện chuẩn ( p 0 = 1,013. 10 5 Pa; T 0 = 273 K) thì V 0 = n v 0
Áp dụng phương trình trạng thái của khí lí tưởng cho lượng khí cacbonic:
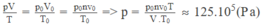
Đúng 0
Bình luận (0)
Một lượng khí lí tưởng trong xilanh kín được giữ ở nhiệt độ không đổi. Ban đầu lượng khí có thể tích 4m3 và áp suất 3atm. Người ta nén khí tới áp suất 6atm. Tính thể tích khí khi bị nén và vẽ đường biểu diễn quá trình biến đổi trạng thái khí trên trong hệ tọa độ (p,V).
Một xylanh có thể tích ban đầu 2 m3 chứa khí CO ở nhiệt độ 300K và áp suất ban đầu 500 kPa. Sau đó được nén đẳng nhiệt đến khi thể tích còn 0,1 m3, công nén sẽ là:
Một bình kín có thể tích không đổi chứa khí lí tưởng ở áp suất 1,5.
10
5
Pa và nhiệt độ 20
°
C
. Tính áp suất trong bình khi nhiệt độ trong bình tăng lên tới 40
°
C
. A.
p
2
1
,
6
.
10
6
P
a
.
B.
p
2
1
,
6...
Đọc tiếp
Một bình kín có thể tích không đổi chứa khí lí tưởng ở áp suất 1,5. 10 5 Pa và nhiệt độ 20 ° C . Tính áp suất trong bình khi nhiệt độ trong bình tăng lên tới 40 ° C .
A. p 2 = 1 , 6 . 10 6 P a .
B. p 2 = 1 , 6 . 10 5 P a .
C. p 2 = 1 , 6 . 10 7 P a
D. p 2 = 1 , 6 . 10 4 P a .
Đáp án: B
Vì thể tích của bóng đèn không đổi nên ta có:
p 1 T 1 = p 2 T 2 → p 2 = T 2 T 1 p 1 = 40 + 273 20 + 273 .1,5.10 5 = 1,6.10 5 (pa)
Đúng 0
Bình luận (0)
Một bình kín chứa 1 mol khí Nito, áp suất 10 5 Pa, ở nhiệt độ 27 ° C . Do có một lượng khí thoát ra ngoài nên áp suất của khí trong bình chỉ còn 0,8. 10 5 Pa, nhiệt độ vẫn được giữ không đổi. Lượng khí đã thoát ra ngoài bằng:
A. 0,4mol
B. 0,8mol
C. 0,2mol
D. 0,1mol
Đáp án: C
Ban đầu, khí Nito có khối lượng mm, thể tích V, áp suất p, nhiệt độ T
PT: p 1 V = m M R T 1
- Sau một thời gian, khí Heli có khối lượng m′, thể tích V, áp suất p2, nhiệt độ T
PT: p 2 V = m ' M R T 2
Lấy 2 1 ta được:
p 2 p 1 = m ' m ↔ 0,8 1 = m ' m → m ' = 0,8 m
=> Lượng khí Nito đã thoát ra:
Δ m = m − m ' = m − 0,8 m = 0,2 m = 0,2.1.28 = 5,6 g
Số mol khí Nito thoát ra ngoài là: n = m M = 5,6 28 = 0,2 m o l
Vậy lượng khí đã thoát ra ngoài bằng: 0,2mol
Đúng 0
Bình luận (0)
Một bình chứa kín một chất khí ở nhiệt độ
57
°
C
và áp suất 30atm. Người ta cho 2/3 lượng khí thoát ra khỏi bình và hạ nhiệt độ xuống còn
41
°
C
. Tính áp suất của khí còn lại trong bình. Coi thể tích của bình chứa không thay đổi khi hạ nhiệt độ. Chọn đáp án đúng. A. 6,98 atm B. 10,1 atm C. 7,66 atm D. 5,96 atm
Đọc tiếp
Một bình chứa kín một chất khí ở nhiệt độ 57 ° C và áp suất 30atm. Người ta cho 2/3 lượng khí thoát ra khỏi bình và hạ nhiệt độ xuống còn 41 ° C . Tính áp suất của khí còn lại trong bình. Coi thể tích của bình chứa không thay đổi khi hạ nhiệt độ. Chọn đáp án đúng.
A. 6,98 atm
B. 10,1 atm
C. 7,66 atm
D. 5,96 atm
Chọn B.
Ban đầu, lúc chưa làm thoát khí ta có:
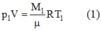
Khi làm thoát khí, lượng khí còn lại trong bình là
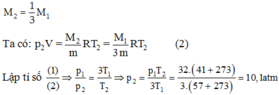
Đúng 0
Bình luận (0)
Một bình chứa kín một chất khí ở nhiệt độ 57°C và áp suất 30atm. Người ta cho 2/3 lượng khí thoát ra khỏi bình và hạ nhiệt độ xuống còn
41
o
C
. Tính áp suất của khí còn lại trong bình. Coi thể tích của bình chứa không thay đổi khi hạ nhiệt độ. Chọn đáp án đúng. A. 6,98 atm B. 10,1 atm C. 7,66 atm D. 5,96 atm
Đọc tiếp
Một bình chứa kín một chất khí ở nhiệt độ 57°C và áp suất 30atm. Người ta cho 2/3 lượng khí thoát ra khỏi bình và hạ nhiệt độ xuống còn 41 o C . Tính áp suất của khí còn lại trong bình. Coi thể tích của bình chứa không thay đổi khi hạ nhiệt độ. Chọn đáp án đúng.
A. 6,98 atm
B. 10,1 atm
C. 7,66 atm
D. 5,96 atm
Một bình kín chứa khí oxi ở nhiệt độ 200C và áp suất 105Pa. Nếu đem bình phơi nắng ở nhiệt độ 400C thì áp suất trong bình sẽ là bao nhiêu ? A. 2.105Pa B.0,15.105Pa C. 1,068.105Pa D. 0,936.105Pa
Đọc tiếp
Một bình kín chứa khí oxi ở nhiệt độ 200C và áp suất 105Pa. Nếu đem bình phơi nắng ở nhiệt độ 400C thì áp suất trong bình sẽ là bao nhiêu ?
A. 2.105Pa
B.0,15.105Pa
C. 1,068.105Pa
D. 0,936.105Pa