Nguyên tố R có cấu hình electron lớp ngoài cùng là ns2np4. Công thức hợp chất của R với H và công thức oxit tương ứng với hóa trị cao nhất của R lần lượt là
A. RH2 và RO
B. RH2 và RO2
C. RH4 và RO2
D. RH2 và RO3
Nguyên tố R có cấu hình electron lớp ngoài cùng là ns2np4. Công thức hợp chất của R với H và công thức oxit tương ứng với hóa trị cao nhất của R lần lượt là
A. RH2 và RO
B. RH2 và RO2
C. RH4 và RO2
D. RH2 và RO3
Đáp án D
R có 6e lớp ngoài cùng, hóa trị cao nhất với oxi = 6, hidro = 2.
Nguyên tố R có cấu hình electron lớp ngoài cùng là n s 2 n p 4 . Công thức hợp chất của R với H và công thức oxit tương ứng với hóa trị cao nhất của R lần lượt là
A. R H 2 và RO
B. R H 2 và R O 2
C. R H 4 và R O 2
D. R H 2 và R O 3
Chọn D
Nguyên tố R có cấu hình electron lớp ngoài cùng là ns2np4 → R thuộc nhóm VIA.
→ Công thức oxit cao nhất của R là RO3; công thức hợp chất khí với H của R là RH2.
Mọi người giúp với. Nguyên tố r có cấu hình electron ngoài cùng là ns²np⁴. Hãy tìm công thức hợp chất của K với H và công thức oxit tương ứng với hóa trị cao nhất của R
1. Một nguyên tố R tạo với hidro hợp chất chứa 12,5% hidro về khối lượng. Oxit tạo cao nhất của nó trong hợp chất với oxi là RO2. Tìm nguyên tố R . Viết công thức electron và công thức cấu tạo của hợp chất khí với hidro và oxit cao nhất, xác định cộng hóa trị của các nguyên tử trong các hợp chất.
Oxit cao nhất của một nguyên tố R thuộc nhóm A có dạng RO3. Cho các nhận định về R:
(1) R có hóa trị cao nhất với oxi là 6.
(2) Công thức hợp chất khí của R với H có dạng RH2.
(3) R là một phi kim.
(4) Axit tương ứng với oxit cao nhất của R là H2RO3
Số nhận định đúng là:
A. 1.
B. 2.
C. 3.
D. 4.
Oxit cao nhất của một nguyên tố R thuộc nhóm A có dạng RO3
=>Hóa trị cao nhất của R với oxi là 6 R có công thức electron lớp ngoài cùng
=>R là một phi kim.
Hóa trị với hidro là: 8 – 6 = 2
=>Công thức hợp chất khí với hidro hóa là RH2
Axit tương ứng của RO3 là H2SO4.
Các nhận định đúng là (1),(2),(3).
Đáp án C.
Phần trăm khối lượng của nguyên tố R trong hợp chất khí với hiđro (R có số oxi hóa thấp nhất) và trong oxit cao nhất tương ứng là a% và b%, với a : b = 15 : 8, biết R có cấu hình electron ở lớp ngoài cùng là n s 2 n p 2 . Giá trị a là
A. 75,00%.
B. 87,50%.
C. 82,35%.
D. 94,12%.
Chọn B
R có 4 electron lớp ngoài cùng, e cuối cùng điền vào phân lớp np → R thuộc nhóm IVA
→ Hợp chất khí với hiđro và oxit cao nhất của R lần lượt là R O 2 , R H 4 .
Ta có:
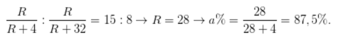
Nguyên tử R có cấu hình electron lớp ngoài cùng là ns 2 np 4 . Trong công thức hợp chất với H của nó có chứa 5,88% H về khối lượng. Nguyên tố R là
A. O.
B. Se.
C. Te.
D. S.
: Oxit cao nhất của một nguyên tố R ứng với công thức RO2. Trong hợp chất của R với Hidro có 75% R về khối lượng. Xác định nguyên tố R; công thức hợp chất khí với Hidro; hợp chất với oxi.
Nguyên tố R có cấu hình electron nguyên tử 1s22s22p63s23p3. Công thức hợp chất với hidro và công thức oxit cao nhất của R là
A. RH2 và RO3
B. RH3 và R2O5
C. RH và R2O7
D. RH4 và RO2
Nguyên tố R có cấu hình electron nguyên tử ls22s22p63s23p3. Công thức hợp chất với hiđro và công thức oxit cao nhất của R là
A. RH2 và RO3
B. RH3 và R2O5
C. RH và R2O7
D. RH4 và RO2.