Cho 26,0 gam Zn tác dụng hoàn toàn với một lượng dư dung dịch cu( No↓3)↓2 thủ được m gam kim loại cu. Giá trị của m là

Những câu hỏi liên quan
Cho m gam bột Zn tác dụng hoàn toàn với dung dịch CuSO 4 dư, thu được 9,6 gam kim loại Cu. Giá trị của m là
A. 6,50
B. 3,25
C. 9,75
D. 13,00
Cho m gam kim loại gồm Mg và Al vào 500 ml dung dịch chứa Cu(NO3)2 0,5M và AgNO31M, sau phản ứng hoàn toàn thu được (m + 57,8) gam 2 kim loại. Cho lượng kim loại vừa thu được tác dụng với HNO3 dư thu được 6,72 lít NO (đktc). Giá trị của m gần nhất với A. 15 B. 8 C. 9 D. 11
Đọc tiếp
Cho m gam kim loại gồm Mg và Al vào 500 ml dung dịch chứa Cu(NO3)2 0,5M và AgNO31M, sau phản ứng hoàn toàn thu được (m + 57,8) gam 2 kim loại. Cho lượng kim loại vừa thu được tác dụng với HNO3 dư thu được 6,72 lít NO (đktc). Giá trị của m gần nhất với
A. 15
B. 8
C. 9
D. 11
Đáp án C
Cho m gam kim loại Mg, Al tác dụng với 0,25 mol Cu(NO3)2 và 0,5 mol Ag sau phản ứng thu được (m+57,8) gam 2 kim loại chắc chắn là Cu và Ag
Do sinh ra Cu nên Ag hết do vậy thu được 0,5 mol Ag và x mol Cu.
Cho lượng kim loại tác dụng với HNO33 dư thu được 0,3 mol NO
Bảo toàn e:
x = 0 , 3 . 3 - 0 , 25 2 = 0 , 2 → m + 57 , 8 = 0 , 5 . 108 + 0 , 2 . 64 → m = 9 g a m
Đúng 0
Bình luận (0)
Cho m gam kim loại gồm Mg và Al vào 500 ml dung dịch chứa Cu(NO3)2 0,5M và AgNO31M, sau phản ứng hoàn toàn thu được (m + 57,8) gam 2 kim loại. Cho lượng kim loại vừa thu được tác dụng với HNO3 dư thu được 6,72 lít NO (đktc). Giá trị của m gần nhất với A. 15 B. 8 C. 9 D. 11
Đọc tiếp
Cho m gam kim loại gồm Mg và Al vào 500 ml dung dịch chứa Cu(NO3)2 0,5M và AgNO31M, sau phản ứng hoàn toàn thu được (m + 57,8) gam 2 kim loại. Cho lượng kim loại vừa thu được tác dụng với HNO3 dư thu được 6,72 lít NO (đktc). Giá trị của m gần nhất với
A. 15
B. 8
C. 9
D. 11
Đáp án C
Cho m gam kim loại Mg, Al tác dụng với 0,25 mol Cu(NO3)2
và 0,5 mol Ag sau phản ứng thu được (m+57,8) gam 2 kim loại chắc chắn là Cu và Ag
Do sinh ra Cu nên Ag hết do vậy thu được 0,5 mol Ag và x mol Cu.
Cho lượng kim loại tác dụng với HNO33 dư thu được 0,3 mol NO
Bảo toàn e: x = 0 , 3 . 3 - 0 , 5 2 = 0 , 2
→ m + 57 , 8 = 0 , 5 . 108 + 0 , 2 . 64
→ m = 9 g a m
Đúng 0
Bình luận (0)
Cho m gam kim loại gồm Mg và Al vào 500 ml dung dịch chứa Cu(NO3)2 0,5M và AgNO3 1M, sau phản ứng hoàn toàn thu được (m + 57,8) gam 2 kim loại. Cho lượng kim loại vừa thu được tác dụng với HNO3 dư thu được 6,72 lít NO (đktc). Giá trị của m gần nhất với: A.9 B. 11 C. 8 D. 15
Đọc tiếp
Cho m gam kim loại gồm Mg và Al vào 500 ml dung dịch chứa Cu(NO3)2 0,5M và AgNO3 1M, sau phản ứng hoàn toàn thu được (m + 57,8) gam 2 kim loại. Cho lượng kim loại vừa thu được tác dụng với HNO3 dư thu được 6,72 lít NO (đktc). Giá trị của m gần nhất với:
A.9
B. 11
C. 8
D. 15
Cho m gam kim loại gồm Mg và Al vào 500 ml dung dịch chứa Cu(NO3)2 0,5M và AgNO3 1M, sau phản ứng hoàn toàn thu được (m + 57,8) gam 2 kim loại. Cho lượng kim loại vừa thu được tác dụng với HNO3 dư thu được 6,72 lít NO (đktc). Giá trị của m gần nhất với: A.9. B. 11. C. 8. D. 15.
Đọc tiếp
Cho m gam kim loại gồm Mg và Al vào 500 ml dung dịch chứa Cu(NO3)2 0,5M và AgNO3 1M, sau phản ứng hoàn toàn thu được (m + 57,8) gam 2 kim loại. Cho lượng kim loại vừa thu được tác dụng với HNO3 dư thu được 6,72 lít NO (đktc). Giá trị của m gần nhất với:
A.9.
B. 11.
C. 8.
D. 15.
Sau phản ứng thu được 2 kim loại là Ag và Cu => Mg và Al phản ứng hết.
Đặt số mol Cu2+ phản ứng là x
=> m + 57,8 = 108.0,5 + 64x
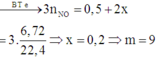
=> Chọn đáp án A
Đúng 0
Bình luận (0)
Chia m gam hỗn hợp X gồm hai kim loại Cu, Fe thành hai phần bằng nhau.Phần 1: Tác dụng hoàn toàn với
HNO
3
đặc, nguội thu được 2,24 khí
NO
2
(đktc).Phần 2: Tác dụng hoàn toàn với dung dịch
H
2
SO
4
loãng, dư thu được 4,48 lít khí (đktc) Giá trị của m là (Cho Cu 64; Fe 56) A. 4,96. B. 28,8. C. 4,16. D. 17,6.
Đọc tiếp
Chia m gam hỗn hợp X gồm hai kim loại Cu, Fe thành hai phần bằng nhau.
Phần 1: Tác dụng hoàn toàn với HNO 3 đặc, nguội thu được 2,24 khí NO 2 (đktc).
Phần 2: Tác dụng hoàn toàn với dung dịch H 2 SO 4 loãng, dư thu được 4,48 lít khí (đktc) Giá trị của m là (Cho Cu = 64; Fe = 56)
A. 4,96.
B. 28,8.
C. 4,16.
D. 17,6.
Chọn B
Phần I. Cho X tác dụng với HNO 3 đặc, nguội chỉ có Cu phản ứng.
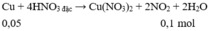
Phần II. Cho X tác dụng với H 2 SO 4 loãng, dư chỉ có Fe phản ứng
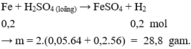
Đúng 0
Bình luận (0)
Cho 10.8 gam hỗn hợp A gồm Cu và kim loại M (khối lượng của M lớn hơn khối lượng của Cu) tác dụng với dung dịch HCl dư, thu dược 2,912 lít khí (đktc). Nếu cho hỗn hợp A này tác dụng hết với dung dịch H2SO4 đặc, đun nóng thì thu được 5,6 lít khí SO2 (sản phẩm khử duy nhất, đktc). Mặt khác, nếu cho 5,4 gam hỗn hợp A tác dụng với 160 ml AgNO3 1M thu được m gam chắt rắn. Biết các phản ứng xảy ra hoàn toàn, kim loại M không có hóa trị (I) trong các hợp chất. Xác định giá trị m
Đọc tiếp
Cho 10.8 gam hỗn hợp A gồm Cu và kim loại M (khối lượng của M lớn hơn khối lượng của Cu) tác dụng với dung dịch HCl dư, thu dược 2,912 lít khí (đktc). Nếu cho hỗn hợp A này tác dụng hết với dung dịch H2SO4 đặc, đun nóng thì thu được 5,6 lít khí SO2 (sản phẩm khử duy nhất, đktc). Mặt khác, nếu cho 5,4 gam hỗn hợp A tác dụng với 160 ml AgNO3 1M thu được m gam chắt rắn. Biết các phản ứng xảy ra hoàn toàn, kim loại M không có hóa trị (I) trong các hợp chất. Xác định giá trị m
nH2 = 0,13 mol; nSO2 = 0,25 mol
Ta có
2H+ + 2e → H2 Cu → Cu2+ + 2e
0,26 ←0,13 0,12 0,24
S+6 + 2e → S+4
0,5 ← 0,25
TH1: M là kim loại có hóa trị không đổi
=> nCu = (0,5 – 0,26) : 2 = 0,12 mol => mCu = 7,68g
=> mM = 3,12g (loại vì khối lượng của M lớn hơn của Cu)
TH2: M là kim loại có hóa trị thay đổi
Do M không có hóa trị I do đó khi phản ứng với HCl thì M thể hiện hóa trị II
M + 2HCl → MCl2 + H2
0,13 ← 0,13
Do M có hóa trị thay đổi => khi phản ứng với H2SO4 đặc nóng thì M thể hiện hóa trị III
2M + 6H2SO4 → M2(SO4)3 + 3SO2 + 6H2O
0,13 → 0,195
Cu + 2H2SO4 → CuSO4+ SO2 + 2H2O
0,055 ← 0,055
=> mM = 10,8 – 0,055 . 64 = 7,28g
=> MM = 56 => Fe
Ta có số mol của Cu và Fe trong 10,8 g lần lượt là 0,055 và 0,13 mol
=> Trong 5,4g có số mol Cu và Fe lần lượt là 0,0275 và 0,065 mol
nAgNO3 = 0,16mol
Fe + 2AgNO3 → Fe(NO3)2 +2Ag
0,065 0,13 0,065 0,13
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
0,015 0,03 0,03
=> nCu dư = 0,0275 – 0,015 = 0,0125mol
m = mCu dư + mAg = 0,0125 . 64 + 0,16 . 108 = 18,08g
Đúng 1
Bình luận (0)
Cho m gam hỗn hợp kim loại Zn, Cu vào dung dịch HCl (dư). Sau khi các phản ứng xảy ra hoàn toàn, thu được 4,48 lít H2 (đktc) và 2,0 gam kim loại không tan. Giá trị của m là A. 8,5. B. 18,0. C. 15,0. D. 16,0.
Đọc tiếp
Cho m gam hỗn hợp kim loại Zn, Cu vào dung dịch HCl (dư). Sau khi các phản ứng xảy ra hoàn toàn, thu được 4,48 lít H2 (đktc) và 2,0 gam kim loại không tan. Giá trị của m là
A. 8,5.
B. 18,0.
C. 15,0.
D. 16,0.
Cho m gam hỗn hợp kim loại Zn, Cu vào dung dịch HCl dư. Sau khi phản ứng xảy ra hoàn toàn, thu được 4,48 lít khí H2 (đktc) và 2,0 gam kim loại không tan. Giá trị của m là
A. 18,0
B. 15,0
C. 8,5
D. 16,0
Đáp án B
Chỉ có Zn phản ứng với HCl, Cu không phản ứng nên mCu = 2 gam
nH2 = 0,2 mol
Zn + 2HCl → ZnCl2 + H2
0,2 0,2
=> mZn = 0,2.65 = 13 gam
=> m = 13+2 = 15 gam
Đúng 0
Bình luận (0)





