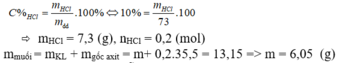cho m(g) fe tác dụng vừa đủ với 200g dd HCl 14,6% . tìm m

Những câu hỏi liên quan
Câu 2:Có một hỗn hợp m gam gồm kim loại Al và Fe, hai dd NaOH và HCl chưa rõ nồng độ biết rằng: - 100ml dd HCl tác dụng vừa đủ với 3,71 gam Na2CO3 và 20 gam dd NaOH thu được 5,85g muối khan. - Cho m gam hỗn hợp Al, Fe tác dụng vừa đủ với 66,67 g dd NaOH hoặc 700ml dd HCl. a. Tính CM dd HCl và nồng độ % dd NaOH. b. Tính khối lượng mỗi kim loại trong hỗn hợp.
Cho 12,1 g hỗn hợp Zn, Fe tác dụng với vừa đủ với m g dd HCl 10%. Cô cạn dd thu được 19,2 g muối. Giá trị m là:
A. 73 g
B. 53 g
C. 43 g
D. 63 g
Đáp án A
mmuối = mKL + mgốc axit => 19,2 = 12,1 + mCl-
![]() = nHCl
= nHCl
![]() .100%
.100%
=> m = 73 g
Đúng 0
Bình luận (0)
1.cho 4 8g mg tác dụng vừa đủ với m gam dd hcl 14,6%
a. tính giá trị m và thể tích hidro
b C% muối thu đc
2. cho 13g zn tác dụng vừa đủ vs 200g dd H2SO4
a tính C% đ h2so4 đã dùng
b tính c% dd muối thu đc
mik đg cần gấp mai nộp ai nhanh nhất mik đánh dấu cho nha mãi iuu
M là kim loại nhóm A có 2 electron lớp ngoài cùng , cho 16g M tác dụng vừa đủ với 200g dd HCl 14,6% thu được dd X .Tìm kim loại M?
M có 2 e lớp ngoài cùng => M hóa trị II
M + 2HCl --> MCl2 + H2
0,4 <- 0,8
mHCl = (200.14,6)/100 = 29,2 g
=> nHCl = 29,2/36,5 = 0,8 mol
=> MM = 16/0,4 = 40 đvC
vậy M là Canxi : Ca (M = 40)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
bài 1:Cho 6,5g Zn tác dụng vừa đủ với 200g dd HCl tạo thành dd ZnCl2 và khí H2.a/Tính khối lượng HCl đã phản ứng?b/ Tính thể tích khí H2 thoát ra(đktc)?c/Tính khối lượng dd sau phản ứng?Bài 2:Cho 4,8g Mg tác dụng vừa đủ với 100g dd HCl tạo thành dd MgCl2 và khí H2.a/Tính khối lượng HCl đã phản ứng?b/Tính thể tích khí H2 thoát ra(đktc)?c/Tính nồng độ phần trăm của dd sau phản ứng?MỌI NGƯỜI ƠI GIÚP VỚI Ạ!!! làm ơn SOS
Đọc tiếp
bài 1:Cho 6,5g Zn tác dụng vừa đủ với 200g dd HCl tạo thành dd ZnCl2 và khí H2.
a/Tính khối lượng HCl đã phản ứng?
b/ Tính thể tích khí H2 thoát ra(đktc)?
c/Tính khối lượng dd sau phản ứng?
Bài 2:Cho 4,8g Mg tác dụng vừa đủ với 100g dd HCl tạo thành dd MgCl2 và khí H2.
a/Tính khối lượng HCl đã phản ứng?
b/Tính thể tích khí H2 thoát ra(đktc)?
c/Tính nồng độ phần trăm của dd sau phản ứng?
MỌI NGƯỜI ƠI GIÚP VỚI Ạ!!! làm ơn SOS
\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\
pthh:Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1 0,1
\(m_{HCl}=0,2.36,5=7,3\left(g\right)\\
V_{H_2}=0,1.22,4=2,24l\\
m_{\text{dd}}=6,5+200-\left(0,1.2\right)=206,3g\)
bài 2 :
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\
pthh:Mg+2HCl\rightarrow MgCl_2+H_2\)
0,2 0,4 0,2 0,2
\(m_{HCl}=0,4.36,5=14,6g\\
V_{H_2}=0,2.22,4=4,48l\\
m\text{dd}=4,8+200-0,4=204,4g\\
C\%=\dfrac{0,2.136}{204,4}.100\%=13,3\%\)
Đúng 2
Bình luận (0)
Cho 200ml dd CuCl₂ 1,5M tác dụng vừa đủ với 200g dd KOH a% a) Tính a b) Tính khối lượng kết tủa thu được c) Lọc lấy kết tủa cho tác dụng với dd HCl 7,3% vừa đủ. Tính khối lượng dd HCl đã dùng ?
Cho m gam hỗn hợp gồm Ca và CaCO3 tác dụng hoàn toàn với một lượng vừa đủ dd HCL 14,6 % thu được 6,72 lít khí hỗn hợp có tỉ lệ mol 1 :1. Tìm m và nồng độ mol của muối sau pư
Xem chi tiết
\(n_{hhk}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Gọi x là số mol Ca
y là số mol CaCO3
\(Ca+2HCl\rightarrow CaCl_2+H_2\)
x..........2x...........x.............x
\(CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\)
y...................2y............y........................y
Ta có x+y =0,3
Mặt khác ta lại có x:y=1:1
=> x=y=0,15
=>m=0,15.40+0,15.100=21(g)
\(m_{ddHCl}=\dfrac{\left(0,3+0,3\right).36,5}{14,6\%}=150\left(g\right)\)
mdd sau phản ứng = m + mddHCl-mkhí = 21 +150 - (0,15.2 + 0,15.44) = 164,1 (g)
=> \(C\%_{CaCl_2}=\dfrac{\left(0,15+0,15\right).111}{164,1}.100=20,29\%\)
Đúng 2
Bình luận (0)
Cho m gam hỗn hợp Zn, Fe tác dụng với vừa đủ với 73g dd HCl 10%. Cô cạn dd thu được 13,15g muối. Giá trị m là: A. 7,05 g B. 5,3 g C. 4,3 g D. 6,05 g
Đọc tiếp
Cho m gam hỗn hợp Zn, Fe tác dụng với vừa đủ với 73g dd HCl 10%. Cô cạn dd thu được 13,15g muối. Giá trị m là:
A. 7,05 g
B. 5,3 g
C. 4,3 g
D. 6,05 g
Cho hh (A) gồm K2O và K2SO3 tác dụng hoàn toàn với 200g dd HCl 14,6% (vừa đủ), kết thúc phản ứng thu được thu được 6,72 l khí (đktc)
a. Tính thành phần % về khối lượng mỗi chất rắn trong hh đầu.
b. Tính C% của muối trong dd thu được.
PTHH: \(K_2O+2HCl\rightarrow2KCl+H_2O\)
\(K_2SO_3+2HCl\rightarrow2KCl+SO_2\uparrow+H_2O\)
a) Ta có: \(\left\{{}\begin{matrix}n_{HCl}=\dfrac{200\cdot14,6\%}{36,5}=0,8\left(mol\right)\\n_{SO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{K_2SO_3}=0,3\left(mol\right)\\n_{K_2O}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{K_2O}=\dfrac{0,1\cdot94}{0,1\cdot94+0,3\cdot158}\cdot100\%\approx16,55\%\\\%m_{K_2SO_3}=83,45\%\end{matrix}\right.\)
b) Theo các PTHH: \(n_{KCl}=0,8\left(mol\right)\) \(\Rightarrow m_{KCl}=74,5\cdot0,8=59,6\left(g\right)\)
Mặt khác: \(\left\{{}\begin{matrix}m_{hh}=56,8\left(g\right)\\m_{SO_2}=0,3\cdot64=19,2\left(g\right)\end{matrix}\right.\)
\(\Rightarrow m_{dd}=m_{hh}+m_{ddHCl}-m_{SO_2}=237,6\left(g\right)\)
\(\Rightarrow C\%_{KCl}=\dfrac{59,6}{237,6}\cdot100\%\approx25,1\%\)
Đúng 2
Bình luận (2)
cho 4 8g mg tác dụng vừa đủ với m gam dd hcl 14,6%
a. tính giá trị m và thể tích hidro
b C% muối thu đc
cho 13g zn tác dụng vừa đủ vs 200g dd H2SO4
a tính C% đ h2so4 đã dùng
b tính c% dd muối thu đc
cho 4 8g mg tác dụng vừa đủ với m gam dd hcl 14,6%
a. tính giá trị m và thể tích hidro
b C% muối thu đc
----------------------------------------------Giải-------------------------------------------------
a) \(n_{Mg}=\frac{48}{24}=2\left(mol\right)\)
PTHH: Mg + 2HCl -------> MgCl2 + H2
Theo PT : n HCl =2 n Mg =4(mol)
=> \(m_{ddHCl}=\frac{4.36,5}{14,6\%}=1000\left(g\right)\)
Theo PT : n H2 =n Mg =2 (mol)
=> V H2 =2 .22,4 =44,8 (l)
b) m dd sau phản ứng = 48 + 1000 - 2.2 = 1044 (g)
Theo PT : n MgCl2 =n Mg =2 (mol)
=> \(C\%_{MgCl_2}=\frac{2.95}{1044}.100=18,2\%\)
cho 13g zn tác dụng vừa đủ vs 200g dd H2SO4
a tính C% đ h2so4 đã dùng
b tính c% dd muối thu đc
----------------------------------------------Giải-------------------------------------------------
a) \(n_{Zn}=\frac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + H2SO4 ---------> ZnSO4 + H2
Theo PT : n H2SO4 = n Zn = 0,2 (mol )
=> \(C\%_{H_2SO_4}=\frac{0,2.98}{200}.100=9,8\%\)
b) Theo PT : n H2 = n Zn = 0,2 (mol )
m dd sau phản ứng = 13 + 200 - 0,2.2 = 212,6 (g)
Theo PT : n ZnSO4 = n Zn = 0,2 (mol )
=> \(C\%_{ZnSO_4}=\frac{0,2.161}{212,6}.100=15,15\%\)
Đúng 0
Bình luận (0)