Nếu tăng hoặc giảm nhiệt độ dung dịch so với nhiệt độ ban đầu thì dung môi có thay đổi khối lượng không?

Những câu hỏi liên quan
Cho 6g kẽm hạt vào một cốc đựng dung dịch H2SO4 4M (dư) ở nhiệt độ thường. Nếu giữ nguyên các điều kiện khác, chỉ biến đổi một trong các điều kiện sau đây thì tốc độ phản ứng biến đổi như thế nào (tăng lên, giảm xuống hay không đổi)? a) Thay 6g kẽm hạt bằng 6g kẽm bột. b) Thay dung dịch H2SO4 4M bằng dung dịch H2SO4 2M. c) Thực hiện phản ứng ở nhiệt độ phản ứng là 50oC. d) Dùng thể tích dung dịch H2SO4 4M lên gấp đôi ban đầu.
Đọc tiếp
Cho 6g kẽm hạt vào một cốc đựng dung dịch H2SO4 4M (dư) ở nhiệt độ thường.
Nếu giữ nguyên các điều kiện khác, chỉ biến đổi một trong các điều kiện sau đây thì tốc độ phản ứng biến đổi như thế nào (tăng lên, giảm xuống hay không đổi)?
a) Thay 6g kẽm hạt bằng 6g kẽm bột.
b) Thay dung dịch H2SO4 4M bằng dung dịch H2SO4 2M.
c) Thực hiện phản ứng ở nhiệt độ phản ứng là 50oC.
d) Dùng thể tích dung dịch H2SO4 4M lên gấp đôi ban đầu.
a) Tốc độ phản ứng tăng lên (tăng diện tích bề mặt).
b) Tốc độ phản ứng giảm xuống (giảm nồng độ chất phản ứng).
c) Tốc độ phản ứng tăng.
d) Tốc độ phản ứng không thay đổi.
Đúng 0
Bình luận (0)
1.Khi làm lạnh một khối khí oxi thì thể tích của khối khí giảm đi 3 lần?Khối lượng và khối lượng riêng của chất khí đó có thay đổi không, nếu có thì tăng hay giảm bao nhiêu lần?2.Khối lượng của 1 khối chất tăng hay giảm khi : a) Nhiệt độ khối chất tăng b) Nhiệt độ khối chất giảm3.Cho biết khí oxi, hi-đơ-rô, các-bô-níc ban đầu đều có thể tích là 1000cm khối. Khi nhiệt độ của 3 chất cùng tăng 50 độ C thì thể tích khí oxi là 1183 cm khối. Hỏi thể tích của khí hi-đơ-rô à khí các- bô-níc tă...
Đọc tiếp
1.Khi làm lạnh một khối khí oxi thì thể tích của khối khí giảm đi 3 lần?Khối lượng và khối lượng riêng của chất khí đó có thay đổi không, nếu có thì tăng hay giảm bao nhiêu lần?
2.Khối lượng của 1 khối chất tăng hay giảm khi : a) Nhiệt độ khối chất tăng b) Nhiệt độ khối chất giảm
3.Cho biết khí oxi, hi-đơ-rô, các-bô-níc ban đầu đều có thể tích là 1000cm khối. Khi nhiệt độ của 3 chất cùng tăng 50 độ C thì thể tích khí oxi là 1183 cm khối. Hỏi thể tích của khí hi-đơ-rô à khí các- bô-níc tăng thêm bao nhiêu?
Giúp mình với! Chiều nay mình khiểm tra rồi
Đúng 0
Bình luận (0)
vậy thì tớ và cậu cùng tra google cho vui đi
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Nếu áp suất của một lượng khí tăng 2.105 Pa thì thể tích của nó giảm 3 lít, nếu áp suất tăng 5.105Pa thì thể tích giảm đi 5 lít. Coi rằng nhiệt độ của khối khí là không thay đổi, áp suất và thể tích ban đầu của khí. A. B. C. D.
Đọc tiếp
Nếu áp suất của một lượng khí tăng 2.105 Pa thì thể tích của nó giảm 3 lít, nếu áp suất tăng 5.105Pa thì thể tích giảm đi 5 lít. Coi rằng nhiệt độ của khối khí là không thay đổi, áp suất và thể tích ban đầu của khí.
A. ![]()
B. ![]()
C. ![]()
D. ![]()
Đáp án A
Gọi P0 và V0 là áp suất và thể tích ban đầu của khối khí. Gọi P1 và V1 là áp suất và thể tích của khối khí áp suất của nó tăng lên 3.105Pa
P1 =P0 + 2.105Pa; V1 = V0 - 3 lít
Vì nhiệt độ là không đổi, do đó áp dụng định luật Bôi-lơ-ma-ri-ốt, ta có:P0V0 = (P0 + 2.105)(V0 - 3)
⟹ P0V0 = P0V0 + 2.105V0 - 3V0 - 6.105
⟹ 3P0 = 2.105(V0 - 3)
Gọi P2 và V2 là áp suất và thể tích của khối khí khi áp suất của nó tăng lên 5.105Pa
⟹P1=P0+5.105Pa; V1=V0-5
Tương tự như trên, ta suy ra được:
5P0 = 5.105(V0 - 5)
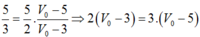 (2)
(2)
Từ (1) và (2) ta có:
⟹V0 = 15-6 = 9 lít
Thay V0=9 lít và phương trình (1), ta tìm được P0 = 4.105Pa
Đúng 0
Bình luận (0)
Một khối sắt có khối lượng m1 nhiệt dung riêng C1 nhiệt độ ban đầu T1 100 độ C khi thả vào một bình nước có khối lượng m2 nhiệt dung riêng c2 thì làm nhiệt độ trung bình tăng từ thêm 2 20 độ C đến t 25 độ C Hỏi nếu thả khối sắt thứ hai có khối lượng m2 có khối lượng 2 M1 nhiệt độ ban đầu 100 độ C vào nước có khối lượng m2 nhiệt dung riêng C2 nhiệt độ T2 20 độ C thì nhiệt độ cân bằng hệ thống là bao nhiêu giải giải bài tập trong hai trường hợp bỏ qua sự hấp thụ nhiệt của bình chứa và sự trao...
Đọc tiếp
Một khối sắt có khối lượng m1 nhiệt dung riêng C1 nhiệt độ ban đầu T1 = 100 độ C khi thả vào một bình nước có khối lượng m2 nhiệt dung riêng c2 thì làm nhiệt độ trung bình tăng từ thêm 2 = 20 độ C đến t = 25 độ C Hỏi nếu thả khối sắt thứ hai có khối lượng m2 có khối lượng 2 M1 nhiệt độ ban đầu 100 độ C vào nước có khối lượng m2 = nhiệt dung riêng C2 nhiệt độ T2 = 20 độ C thì nhiệt độ cân bằng hệ thống là bao nhiêu giải giải bài tập trong hai trường hợp bỏ qua sự hấp thụ nhiệt của bình chứa và sự trao đổi nhiệt với bên ngoài bình chứa khối lượng m3 có nhiệt dung riêng C3 bỏ qua tác dụng nhiệt trong đổi nhiệt với môi trường
Đổ một chất lỏng có khối lượng
m
1
, nhiệt dung riêng
c
1
và nhiệt độ
t
1
vào một chất lỏng có khối lượng
m
2
2
m
1
, nhiệt dung riêng ...
Đọc tiếp
Đổ một chất lỏng có khối lượng m 1 , nhiệt dung riêng c 1 và nhiệt độ t 1 vào một chất lỏng có khối lượng m 2 = 2 m 1 , nhiệt dung riêng c 2 = 1 / 2 c 1 nhiệt độ t 2 > t 1 . Nếu không bỏ qua sự trao đổi nhiệt giữa hai chất lỏng và môi trường (cốc đựng, không khí...) thì khi có cân bằng nhiệt, nhiệt độ t của hai chất lỏng trên có giá trị là
A. t > t 2 + t 1 2
B. t < t 2 + t 1 2
C. t = t 2 + t 1 2
D. t = t 2 + t 1
B
Nếu bỏ qua sự trao đổi nhiệt giữa hai chất lỏng và môi trường (cốc không khí...) thì khi có cân bằng nhiệt, nhiệt độ t theo phương trình cân bằng nhiệt ta có.
Nhiệt lượng thu vào và toả ra bằng nhau nên: Q = m 1 c 1 ∆ t 1 = m 2 c 2 ∆ t 2
Vì m 2 = 2 m 1 , nhiệt dung riêng
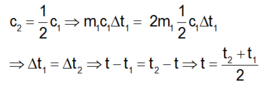
Nếu không bỏ qua sự trao đổi nhiệt giữa hai chất lỏng và môi trường thì t < t 2 + t 1 2
Đúng 0
Bình luận (0)
Dung dịch X được pha từ NaCl và CuSO4 với tỉ lệ mol là 1: 2. Tiến hành điện phân dung dịch X bằng điện cực trơ có màng ngăn xốp đến khi khối lượng dung dịch giảm 10,5 gam thì dừng lại. Sau khi kết thúc quá trình điện phân, tháo điện cực thu được V lít hỗn hợp khí (đktc) và dung dịch Y. Cho lượng dư Ba(OH)2 vào Y thì thấy xuất hiện kết tủa Z. Đem lượng Z này nung nóng ở nhiệt độ cao đến khối lượng không đổi thì thấy khối lượng rắn khan giảm 2,7 gam so với ban đầu. Giá trị của V là A. 1,68 B. 2,2...
Đọc tiếp
Dung dịch X được pha từ NaCl và CuSO4 với tỉ lệ mol là 1: 2. Tiến hành điện phân dung dịch X bằng điện cực trơ có màng ngăn xốp đến khi khối lượng dung dịch giảm 10,5 gam thì dừng lại. Sau khi kết thúc quá trình điện phân, tháo điện cực thu được V lít hỗn hợp khí (đktc) và dung dịch Y. Cho lượng dư Ba(OH)2 vào Y thì thấy xuất hiện kết tủa Z. Đem lượng Z này nung nóng ở nhiệt độ cao đến khối lượng không đổi thì thấy khối lượng rắn khan giảm 2,7 gam so với ban đầu. Giá trị của V là
A. 1,68
B. 2,24
C. 2,80
D. 1,12
Chọn đáp án A
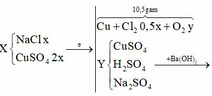
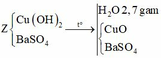
Cho Ba(OH)2 vào dung dịch X thu được kết tủa, lấy kết tủa này nung nóng thì khối lượng giảm chứng tỏ trong kết tủa có Cu(OH)2 Þ nCu2+ trong Y = nH2O bay ra = 2,7/18 = 0,15 mol
Cu2+ dư, mà có hỗn hợp khí thoát ra Þ Hỗn hợp khí này gồm Cl2 và O2 (do Cl- đã hết)
Gọi x là số mol NaCl Þ 2x là số mol CuSO4, gọi y là số mol O2 sinh ra
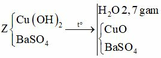
Vậy V=(0,12/2+0,015)x22,4=1,68
Đúng 0
Bình luận (0)
Dung dịch X được pha từ NaCl và CuSO4 với tỉ lệ mol là 1: 2. Tiến hành điện phân dung dịch X bằng điện cực trơ có màng ngăn xốp đến khi khối lượng dung dịch giảm 10,5 gam thì dừng lại. Sau khi kết thúc quá trình điện phân, tháo điện cực thu được V lít hỗn hợp khí (đktc) và dung dịch Y. Cho lượng dư Ba(OH)2 vào Y thì thấy xuất hiện kết tủa Z. Đem lượng Z này nung nóng ở nhiệt độ cao đến khối lượng không đổi thì thấy khối lượng rắn khan giảm 2,7 gam so với ban đầu. Giá trị của V là A. 1,12 B. 1,6...
Đọc tiếp
Dung dịch X được pha từ NaCl và CuSO4 với tỉ lệ mol là 1: 2. Tiến hành điện phân dung dịch X bằng điện cực trơ có màng ngăn xốp đến khi khối lượng dung dịch giảm 10,5 gam thì dừng lại. Sau khi kết thúc quá trình điện phân, tháo điện cực thu được V lít hỗn hợp khí (đktc) và dung dịch Y. Cho lượng dư Ba(OH)2 vào Y thì thấy xuất hiện kết tủa Z. Đem lượng Z này nung nóng ở nhiệt độ cao đến khối lượng không đổi thì thấy khối lượng rắn khan giảm 2,7 gam so với ban đầu. Giá trị của V là
A. 1,12
B. 1,68
C. 2,24
D. 2,80
Chọn đáp án B
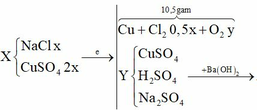
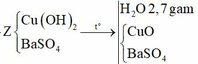
Cho Ba(OH)2 vào dung dịch X thu được kết tủa, lấy kết tủa này nung nóng thì khối lượng giảm chứng tỏ trong kết tủa có Cu(OH)2 Þ nCu2+ trong Y = nH2O bay ra = 2,7/18 = 0,15 mol
Cu2+ dư, mà có hỗn hợp khí thoát ra Þ Hỗn hợp khí này gồm Cl2 và O2 (do Cl- đã hết)
Gọi x là số mol NaCl Þ 2x là số mol CuSO4, gọi y là số mol O2 sinh ra
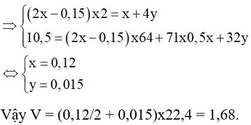
Đúng 0
Bình luận (0)
Đổ một chất lỏng có khối lượng
m
1
, nhiệt dung riêng
c
1
và nhiệt độ
t
1
vào một chất lỏng có khối lượng
m
2
2
m
1
, nhiệt dung riêng
c
2
1...
Đọc tiếp
Đổ một chất lỏng có khối lượng m 1 , nhiệt dung riêng c 1 và nhiệt độ t 1 vào một chất lỏng có khối lượng m 2 = 2 m 1 , nhiệt dung riêng c 2 = 1 2 c 1 và nhiệt độ t 2 > t 1 . Nếu bỏ qua sự trao đổi nhiệt giữa hai chất lỏng và môi trường (cốc đựng, không khí…) thì khi có cân bằng nhiệt, nhiệt độ t của hai chất lỏng trên có giá trị là
A. t = t 2 - t 1 t
B. t = t 1 + t 2 t
C. t < t 1 < t 2
D. t > t 2 > t 1
Nếu bỏ qua sự trao đổi nhiệt giữa hai chất lỏng và môi trường (cốc đựng, không khí…) thì khi có cân bằng nhiệt, nhiệt độ t theo phương trình cân bằng nhiệt ta có: Nhiệt lượng thu vào và tỏa ra bằng nhau nên
Vì m 2 = 2 m 1 nhiệt dung riêng c 2 = 1 2 c 1
⇒ m 1 c 1 c ∆ t 1 = 1 c . 2 m 1 c 1 Q = m 1 c 1 ∆ t 1 = m 2 c 2 ∆ t 2 ∆ t 2
⇒ ∆ t 1 = ∆ t t = 2 ⇒ t - t 1 = t 2 ⇒ t = t 1 + t 2 t
⇒ Đáp án B
Đúng 0
Bình luận (0)
Đổ một chất lỏng có khối lượng m1 , nhiệt dung riêng c1 và nhiệt độ t1 vào một chất lỏng có khối lượng m2 2m1, nhiệt dung riêng c1 1/2c2 và nhiệt độ t1 t2. Nếu bỏ qua sự trao đổi nhiệt giữa hai chất lỏng và môi trường (cốc đựng, không khí...) thì khi có cân bằng nhiệt, nhiệt độ t của hai chất lỏng trên có giá trị là A.
t
t
2
-
t
1...
Đọc tiếp
Đổ một chất lỏng có khối lượng m1 , nhiệt dung riêng c1 và nhiệt độ t1 vào một chất lỏng có khối lượng m2 = 2m1, nhiệt dung riêng c1 = 1/2c2 và nhiệt độ t1 > t2. Nếu bỏ qua sự trao đổi nhiệt giữa hai chất lỏng và môi trường (cốc đựng, không khí...) thì khi có cân bằng nhiệt, nhiệt độ t của hai chất lỏng trên có giá trị là
A. t = t 2 - t 1 2
B. t = t 2 + t 1 2
C. t < t 1 < t 2
D. t > t 2 > t 1
B
Nếu bỏ qua sự trao đổi nhiệt giữa hai chất lỏng và môi trường (cốc không khí...) thì khi có cân bằng nhiệt, nhiệt độ t theo phương trình cân bằng nhiệt ta có.
Nhiệt lượng thu vào và toả ra bằng nhau nên: Q = m 1 c 1 ∆ t 1 = m 2 c 2 ∆ t 2
Vì m 2 = 2 m 1 , nhiệt dung riêng
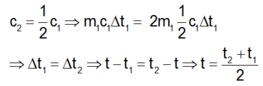
Nếu không bỏ qua sự trao đổi nhiệt giữa hai chất lỏng và môi trường thì t < t 2 + t 1 2
Đúng 0
Bình luận (0)








