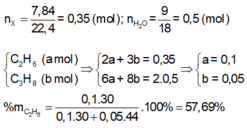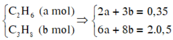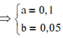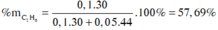Những câu hỏi liên quan
Cho 0,2 mol hỗn hợp X gồm etan, propan và propen qua dung dịch brom dư, thấy khối lượng bình brom tăng 4,2g. Lượng khí còn lại đem đốt cháy hoàn toàn thu được 6,48g nước. Vậy % thể tích etan, propan và propen lần lượt là A. 30%, 20%, 50%. B. 20%, 50%, 30%. C. 50%, 20%, 30%. D. 20%, 30%, 50%.
Đọc tiếp
Cho 0,2 mol hỗn hợp X gồm etan, propan và propen qua dung dịch brom dư, thấy khối lượng bình brom tăng 4,2g. Lượng khí còn lại đem đốt cháy hoàn toàn thu được 6,48g nước. Vậy % thể tích etan, propan và propen lần lượt là
A. 30%, 20%, 50%.
B. 20%, 50%, 30%.
C. 50%, 20%, 30%.
D. 20%, 30%, 50%.
khối lượng bình brom tăng 4,2g ⇒ mC3H6 = 4,2g ⇒ nC3H6 = 0,1
⇒ nAnkan = 0,2 – 0,1 = 0,1
Đặt nC2H6 = a ; nC3H8 = b
Có a+ b = nAnkan = 0,1 (1)
3a + 4b = nH2O = 6,48 : 18 = 0,36 (2)
Từ (1) và (2) ⇒ a = 0,04 ; b = 0,06
⇒ %VC2H6 = 0,04 : 0,2 = 20%
%VC3H8 = 30%
%VC3H6 = 50%
Đáp án D.
Đúng 0
Bình luận (0)
Câu 6: Cho 21,4 gam hỗn hợp gồm propan và propilen lội qua dung dịch brom dư, thấy khối lượng bình brom tăng 12,6 gam.
a) Tính thành phần phần trăm thể tích mỗi khí trong hỗn hợp đầu.
b) Nếu đốt cháy hỗn hợp trên, rồi cho toàn bộ sản phẩm cháy vào nước vôi trong dư thì khối lượng kết tủa thu được là bao nhiêu gam?
Cho hỗn hợp khí A gồm 0,1 mol axetilen, 0,2 mol etilen, 0,1 mol etan và 0,36 mol hidro đi qua ống sứ đựng Ni làm xúc tác, đun nóng, thu được hỗn hợp khí B. Dẫn hỗn hợp khí B qua bình đựng nước brom dư, khối lượng bình tăng 1,64 gam và có hỗn hợp khí C thoát ra khỏi bình brom. Khối lượng của hỗn hợp khí C bằng bao nhiêu? A. 13,26 gam B. 10,28 gam C. 9,58 gam D. 8,2 gam
Đọc tiếp
Cho hỗn hợp khí A gồm 0,1 mol axetilen, 0,2 mol etilen, 0,1 mol etan và 0,36 mol hidro đi qua ống sứ đựng Ni làm xúc tác, đun nóng, thu được hỗn hợp khí B. Dẫn hỗn hợp khí B qua bình đựng nước brom dư, khối lượng bình tăng 1,64 gam và có hỗn hợp khí C thoát ra khỏi bình brom. Khối lượng của hỗn hợp khí C bằng bao nhiêu?
A. 13,26 gam
B. 10,28 gam
C. 9,58 gam
D. 8,2 gam
Bài toán trên có thể tóm tắt theo sơ đồ sau:
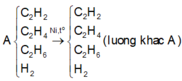
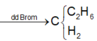
Yêu cầu cần tính khối lượng khí thoát ra trong khi biết khối lượng đầu và khối lượng bị giữ lại, vì thế đơn giản là áp dụng bảo toàn khối lượng ta được:
![]()
![]()
![]()
Đúng 0
Bình luận (0)
Hỗn hợp X gồm axetilen, etilen và hiđrocacbon A cháy hoàn toàn thu được CO2 và H2O theo tỉ lệ mol 1:1. Dẫn X đi qua bình đựng dung dịch brom dư thấy khối lượng bình tăng lên 0,82 gam, khí thoát ra khỏi bình đem đốt cháy hoàn toàn thu được 1,32 gam CO2 và 0,72 gam H2O. Phần trăm thể tích của A trong hỗn hợp X là A. 25% B. 66,66% C. 33,33% D. 75%
Đọc tiếp
Hỗn hợp X gồm axetilen, etilen và hiđrocacbon A cháy hoàn toàn thu được CO2 và H2O theo tỉ lệ mol 1:1. Dẫn X đi qua bình đựng dung dịch brom dư thấy khối lượng bình tăng lên 0,82 gam, khí thoát ra khỏi bình đem đốt cháy hoàn toàn thu được 1,32 gam CO2 và 0,72 gam H2O. Phần trăm thể tích của A trong hỗn hợp X là
A. 25%
B. 66,66%
C. 33,33%
D. 75%
Đáp án A
Hỗn hợp chứa axetilen, etilen và chất A khi đốt thu được CO2 và H2O tỉ lệ 1:1 thì chất A chắc chắn phải là ankan (do axetilen đốt thu được nCO2 > nH2O, etilen đốt thu được nCO2=nH2O, cần phải có 1 chất đốt thu được nCO2< nH2O để đảm bảo tỉ lệ)
Hơn nữa, nC2H2=nA
Khí thoát ra khỏi bình là ankan:
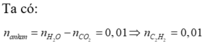
Khối lượng bình tăng lên là khối lượng của axetilen và etilen.

Đúng 0
Bình luận (0)
Hỗn hợp khí X gồm etan và propan. Đốt cháy hoàn toàn X, thu được 7,84 lít CO2 (đktc) và 9 gam H2O. thành phần phần trăm theo khối lượng của etan trong X là :
A. 66,67%
B. 57,69
C. 25,42%
D. 40,54%
Hỗn hợp khí X gồm etan và propan. Đốt cháy hoàn toàn X, thu được 7,84 lít
CO
2
(đktc) và 9 gam
H
2
O
. Thành phần phần trăm theo khối lượng của etan trong X là A. 66,67% B. 57,69 % C. 25,42% D. 40,54%.
Đọc tiếp
Hỗn hợp khí X gồm etan và propan. Đốt cháy hoàn toàn X, thu được 7,84 lít CO 2 (đktc) và 9 gam H 2 O . Thành phần phần trăm theo khối lượng của etan trong X là
A. 66,67%
B. 57,69 %
C. 25,42%
D. 40,54%.
Thực hiện phản ứng crakinh butan thu được một hỗn hợp X gồm các ankan và các anken. Cho toàn bộ hỗn hợp X vào dd brom dư thấy có khí thoát ra bằng 60% thể tích X và khối lượng dd brom tăng thêm 5,6 gam và có 25,6 gam brom đã tham gia phản ứng. Đốt cháy hoàn toàn khí bay ra thu được a mol CO2 và b mol H2O. Vậy a, b có giá trị là A. a 0,9 và b 1,5 B. a 0,56 và b 0,8 C. a 1,2 và b 1,6 D. a 1,2 và b 2
Đọc tiếp
Thực hiện phản ứng crakinh butan thu được một hỗn hợp X gồm các ankan và các anken. Cho toàn bộ hỗn hợp X vào dd brom dư thấy có khí thoát ra bằng 60% thể tích X và khối lượng dd brom tăng thêm 5,6 gam và có 25,6 gam brom đã tham gia phản ứng. Đốt cháy hoàn toàn khí bay ra thu được a mol CO2 và b mol H2O. Vậy a, b có giá trị là
A. a = 0,9 và b = 1,5
B. a = 0,56 và b = 0,8
C. a = 1,2 và b = 1,6
D. a = 1,2 và b = 2
Đáp án B
Khi crakinh butan ta có các quá trình sau:
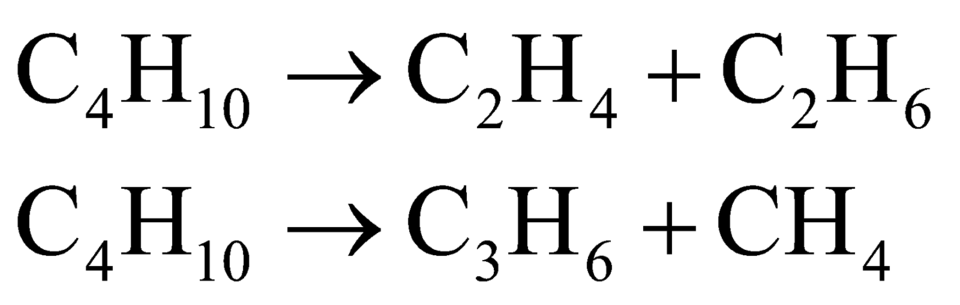
Nhìn vào các phản ứng dễ thấy nanken = nankan mói
Khi đi qua nước brom dư có 60% thể tích X thoát ra, suy ra có 40% X là anken đã phản ứng với brom
=> Có 40% ankan mới tạo thành và 20% butan dư.
Dễ tính được
nBr2=0,16 mol=> n anken=n Br2=0,16
=> nC4H10 du= n anken/2=0,08 mol
Tới đây đề bài đã cho khối lượng hỗn hợp anken, số mol hỗn hợp anken nên có thể tính được số mol mỗi anken trong hỗn hợp
Gọi số mol C3H6 và C2H4 lần lượt là x và y ta có hệ
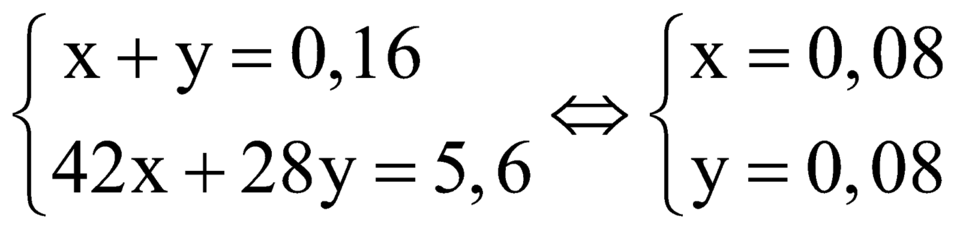 .
.
Khi đó khí bay ra gồm có

Đốt hỗn hợp này ta thu được
![]()
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn hỗn hợp X gồm axetilen, etilen và hiđrocacbon A thu được CO2 và H2O theo tỉ lệ mol 1 : 1. Dẫn X đi qua bình đựng dung dịch brom dư thấy khối lượng bình tăng 0,82 gam, đốt cháy hoàn toàn khí thoát ra khỏi bình brom thu được 1,32 gam CO2 và 0,72 gam H2O. Phần trăm thể tích của A trong X là A. 50%. B. 75%. C. 25%. D. 33,33%.
Đọc tiếp
Đốt cháy hoàn toàn hỗn hợp X gồm axetilen, etilen và hiđrocacbon A thu được CO2 và H2O theo tỉ lệ mol 1 : 1. Dẫn X đi qua bình đựng dung dịch brom dư thấy khối lượng bình tăng 0,82 gam, đốt cháy hoàn toàn khí thoát ra khỏi bình brom thu được 1,32 gam CO2 và 0,72 gam H2O. Phần trăm thể tích của A trong X là
A. 50%.
B. 75%.
C. 25%.
D. 33,33%.
Bài 1/ Dẫn 15,68 lít hỗn hợp X gồm 2 anken liên tiếp trong dãy đồng đẳng và propan qua bình đựng dung dịch brom thấy khối lượng bình brom tăng 16,8g. Mặt khác nếu đốt cháy hoàn toàn X thu được 40,32 lít CO2 (đktc) a. Viết PTHH b. Xác định CTPT 2 anken và tính % V mỗi chất trong hỗn hợp XBài 2/ Đốt cháy hoàn toàn hỗn hợp X gồm 2 ankin A, B thu được 13,44 lít CO2 ( đktc) và 6,48g H2O.a. Xác định CTPT và viết CTCT của A, B ( biết A, B hơn kém nhau 2 nguyên tử cacbon)b. Xác định CTCT đúng của...
Đọc tiếp
Bài 1/ Dẫn 15,68 lít hỗn hợp X gồm 2 anken liên tiếp trong dãy đồng đẳng và propan qua bình đựng dung dịch brom thấy khối lượng bình brom tăng 16,8g. Mặt khác nếu đốt cháy hoàn toàn X thu được 40,32 lít CO2 (đktc)
a. Viết PTHH
b. Xác định CTPT 2 anken và tính % V mỗi chất trong hỗn hợp X
Bài 2/ Đốt cháy hoàn toàn hỗn hợp X gồm 2 ankin A, B thu được 13,44 lít CO2 ( đktc) và 6,48g H2O.
a. Xác định CTPT và viết CTCT của A, B ( biết A, B hơn kém nhau 2 nguyên tử cacbon)
b. Xác định CTCT đúng của A, B. Biết rằng khi cho hỗn hợp X tác dụng với dung dịch AgNO3 trong NH3 dư thu được 43,2 gam kết tủa.
HELP ME .... thank you
Bài 1:
a, \(C_nH_{2n}+Br_2\rightarrow C_nH_{2n}Br_2\)
\(C_nH_{2n}+\dfrac{3n}{2}O_2\underrightarrow{t^o}nCO_2+nH_2O\)
\(C_3H_8+5O_2\underrightarrow{t^o}3CO_2+4H_2O\)
b, Gọi: \(\left\{{}\begin{matrix}n_{C_nH_{2n}}=x\left(mol\right)\\n_{C_3H_8}=y\left(mol\right)\end{matrix}\right.\) \(\Rightarrow x+y=\dfrac{15,68}{22,4}=0,7\left(1\right)\)
Có: \(n_{CO_2}=n.n_{C_nH_{2n}}+3n_{C_3H_8}=nx+3y=\dfrac{40,32}{22,4}=1,8\left(2\right)\)
Mà: m bình tăng = 16,8 (g) = mCnH2n = 14nx (3)
Từ (1), (2) và (3) \(\Rightarrow\left\{{}\begin{matrix}nx=1,2\\x=0,5\left(mol\right)\\y=0,2\left(mol\right)\end{matrix}\right.\)
⇒ n = 1,2:0,5 = 2,4
Mà: 2 anken đồng đẳng kế tiếp.
→ C2H4 và C3H6.
Có: \(\left\{{}\begin{matrix}28n_{C_2H_4}+42n_{C_3H_6}=16,8\\n_{C_2H_4}+n_{C_3H_6}=0,7-0,2\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{C_2H_4}=0,3\left(mol\right)\\n_{C_3H_6}=0,2\left(mol\right)\end{matrix}\right.\)
%n cũng là %V ở cùng điều kiện nhiệt độ, áp suất.
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,3}{0,7}.100\%\approx42,86\%\\\%V_{C_3H_6}=\%V_{C_3H_8}=\dfrac{0,2}{0,7}.100\%\approx28,57\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Bài 2:
a, \(n_{CO_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
\(n_{H_2O}=\dfrac{6,48}{18}=0,36\left(mol\right)\)
\(\Rightarrow n_X=0,6-0,35=0,24\left(mol\right)\)
\(\Rightarrow\overline{C}=\dfrac{0,6}{0,24}=2,5\)
Mà: 2 ankin hơn kém nhau 2 C và số C nhỏ nhất có thể có là 2.
→ C2H2 và C4H6.
CTCT: C2H2: \(CH\equiv CH\)
C4H6: \(CH\equiv C-CH_2-CH_3\) hoặc \(CH_3-C\equiv C-CH_3\)
b, BTNT C, có: \(2n_{C_2H_2}+4n_{C_4H_6}=n_{CO_2}=0,6\left(1\right)\)
BTNT H, có: \(2n_{C_2H_2}+6n_{C_4H_6}=2n_{H_2O}=0,36.2\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{C_2H_2}=0,18\left(mol\right)\\n_{C_4H_6}=0,06\left(mol\right)\end{matrix}\right.\)
C2H2 luôn pư với AgNO3/NH3.
Ta có: \(n_{Ag_2C_2}=n_{C_2H_2}=0,18\left(mol\right)\Rightarrow m_{Ag_2C_2}=0,18.240=43,2\left(g\right)=m_{\downarrow}\)
→ C4H6 không pư.
Vậy: CTCT đúng của 2 chất là: \(CH\equiv CH\) và \(CH_3-C\equiv C-CH_3\)
Đúng 1
Bình luận (0)