Cho m gam hỗn hợp bột X gồm Fe, Cu vào 600 ml dung dịch AgNO3 1M. Sau khi kết thúc phản ứng thu được dung dịch Y chứa 3 muối (không có AgNO3) có khối lượng giảm 50 gam so với ban đầu. Giá trị của m là
A. 64,8
B. 17,6
C. 114,8
D. 14,8
Cho m gam hỗn hợp bột X gồm Fe, Cu vào 600 ml dung dịch AgNO3 1M. Sau khi kết thúc phản ứng thu được dung dịch Y chứa 3 muối (không có AgNO3) có khối lượng giảm 50 gam so với ban đầu. Giá trị của m là
A. 64,8
B. 17,6
C. 114,8
D. 14,8
Chọn đáp án D

Dd sau phản ứng thu được 3 muối và không có AgNO3 => tất cả Ag+ chuyển hết thành Ag
BTNT Ag => nAg = nAgNO3 = 0,6 (mol)
Khối lượng giảm = mAg sinh ra – mFe, Cu
=> 50 = 0,6.108 – m
=> m = 14,8 (g)
Cho m gam hỗn hợp bột X gồm Fe, Cu vào 600 ml dung dịch AgNO3 1M. Sau khi kết thúc phản ứng thu được dung dịch Y chứa 3 muối (không có AgNO3) có khối lượng giảm 50 gam so với ban đầu. Giá trị của m là
A. 64,8
B. 17,6
C. 114,8
D. 14,8
Cho m gam hỗn hợp bột X gồm Fe, Cu vào 600 ml dung dịch AgNO3 1M. Sau khi kết thúc phản ứng thu được dung dịch Y chứa 3 muối (không có AgNO3) có khối lượng giảm 50 gam so với ban đầu. Giá trị của m là
A. 64,8
B. 17,6
C. 114,8
D. 14,8
n(Cu) = 0,1 mol; n(Fe) = 0,1 mol
Các chất có trong cốc sau phản ứng với HCl: Cu (0,1 mol); FeCl2 (0,1 mol); HCl dư
PTHH:
3Cu + 8H+ + 2NO3- → 2Cu2+ + 2NO + 4H2O
3Fe2+ + 4H+ + NO3- → 3Fe3+ + NO + 2H2O
→ n(NaNO3) = 2/3*n(Cu) + 1/3*n(Fe2+) = 0,1 mol → m(NaNO3) = 8,5 gam → Đáp án A
Cho hỗn hợp X gồm CuCl2 và FeCl3. Điện phân dung dịch chứa m gam hỗn hợp X với điện cực trơ, cường độ dòng điện 2,68 A, trong thời gian là 4 giờ. Sau khi kết thúc điện phân thu được dung dịch Y có khối lượng giảm 20,6 gam so với trước khi điện phân. Toàn bộ dung dịch Y tác dụng với lượng dư dung dịch AgNO3 thu được 136,4 gam kết tủa. Mặt khác cho 14,88 gam bột Mg vào dung dịch chứa m gam hỗn hợp X ban đầu. Kết thúc phản ứng thu được m gam kim loại. Giá trị của m là
A. 19,2 gam
B. 26,88 gam
C. 24,48 gam
D. 35,68 gam
Cho hỗn hợp X gồm C u C l 2 và F e C l 3 . Điện phân dung dịch chứa m gam hỗn hợp X với điện cực trơ, cường độ dòng điện 2,68A, trong thời gian là 4 giờ. Sau khi kết thúc điện phân thu được dung dịch Y có khối lượng giảm 20,6 gam so với trước khi điện phân. Toàn bộ dung dịch Y tác dụng với lượng dư dung dịch A g N O 3 thu được 136,4 gam kết tủa. Mặt khác cho 14,88 gam bột Mg vào dung dịch chứa m gam hỗn hợp X ban đầu. Kết thúc phản ứng thu được m' gam kim loại. Giá trị của m' là
A. 26,88 gam
B. 35,68 gam
C. 19,2 gam
D. 24,48 gam
Cho m gam hỗn hợp bột X gồm FexOy, CuO và Cu (x, y nguyên dương) vào 600 ml dung dịch HCl 1M, thu được dung dịch Y (không chứa HCl) và còn lại 6,4 gam kim loại không tan. Cho Y tác dụng với lượng dư dung dịch AgNO3, thu được 102,3 gam kết tủa. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây?
A. 22,7.
B. 34,1.
C. 29,1.
D. 27,5.
Cho m gam hỗn hợp bột X gồm FexOy, CuO và Cu (x, y nguyên dương) vào 600 ml dung dịch HCl 1M, thu được dung dịch Y (không chứa HCl) và còn lại 6,4 gam kim loại không tan. Cho Y tác dụng với lượng dư dung dịch AgNO3, thu được 102,3 gam kết tủa. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây?
A. 22,7.
B. 34,1.
C. 29,1.
D. 27,5.
Do Cu dư sau pư⟶hỗn hợp Y chứa muối Fe2+
nCu trong X = 0,1; nAgCl = 0,6
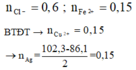
BTKL ⟶ m = 29,2
Đáp án C
Cho m gam hỗn hợp bột X gồm FexOy, CuO và Cu (x, y nguyên dương) vào 600 ml dung dịch HCl 1M, thu được dung dịch Y (không chứa HCl) và còn lại 6,4 gam kim loại không tan. Cho Y tác dụng với lượng dư dung dịch AgNO3, thu được 102,3 gam kết tủa. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây?
A. 22,7
B. 34,1
C. 29,1
D. 27,5
Cho m gam hỗn hợp bột X gồm FexOy, CuO và Cu (x, y nguyên dương) vào 600 ml dung dịch HCl 1M, thu được dung dịch Y (không chứa HCl) và còn lại 6,4 gam kim loại không tan. Cho Y tác dụng với lượng dư dung dịch AgNO3, thu được 102,3 gam kết tủa. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây?
A. 29,1
B. 34,1
C. 27,5
D. 22,7
Đáp án : A
Do Cu dư sau pư => hỗn hợp Y chứa muối Fe2+
n O trong X = 0.1 ; nAgCl = 0.6 => nCl- = 0.6 ; nFe2+ = 0.15
BTĐT => nCu2+ = 0.15 => nAg = (102,3-86,1)/2 = 0.15
BTKL => m = 29.2