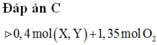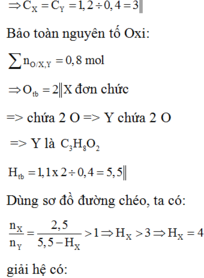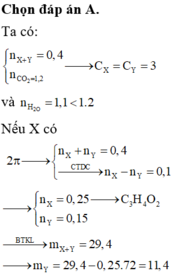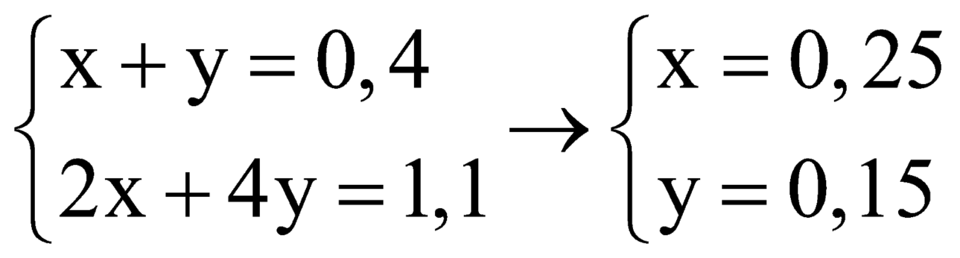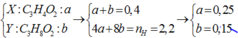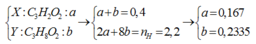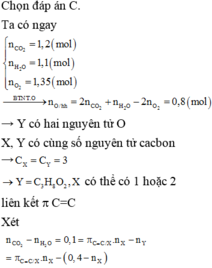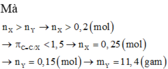Biết X là axit cacboxylic đơn chức, Y là ancol no, cả hai chất đều mạch hở, có cùng số nguyên tử cacbon. Đốt cháy hoàn toàn 0,4 mol hỗn hợp gồm X và Y (trong đó số mol của X lớn hơn số mol của Y) cần vừa đủ 30,24 lít khí O2, thu được 26,88 lít khí CO2 và 19,8 gam H2O. Biết thể tích các khí đo ở điều kiện tiêu chuẩn. Khối lượng của Y trong 0,4 mol hỗn hợp trên là A. 11,4 gam B. 19,0 gam C. 9,0 gam D. 17,7 gam
Đọc tiếp
Biết X là axit cacboxylic đơn chức, Y là ancol no, cả hai chất đều mạch hở, có cùng số nguyên tử cacbon. Đốt cháy hoàn toàn 0,4 mol hỗn hợp gồm X và Y (trong đó số mol của X lớn hơn số mol của Y) cần vừa đủ 30,24 lít khí O2, thu được 26,88 lít khí CO2 và 19,8 gam H2O. Biết thể tích các khí đo ở điều kiện tiêu chuẩn. Khối lượng của Y trong 0,4 mol hỗn hợp trên là
A. 11,4 gam
B. 19,0 gam
C. 9,0 gam
D. 17,7 gam