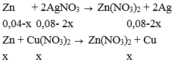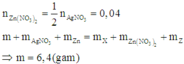Cho m gam bột Cu vào 400 ml dung dịch AgNO3 0,2M, sau một thời gian phản ứng thu được 7,76 gam hỗn hợp chất rắn X và dung dịch Y. Lọc tách X, rồi thêm 5,85 gam bột Zn vào Y, sau khi phản ứng xảy ra hoàn toàn thu được 10,53 gam chất rắn Z. Giá trị của m là :
A. 6,40.
B. 5,76 .
C. 3,84.
D. 5,12.