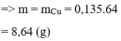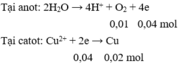Điện phân dung dịch C u S O 4 với cường độ I = 10A trong thời gian t, ta thấy có 224 ml khí (đktc) thoát ra ở anot. Giả thiết rằng điện cực trơ và hiệu suất điện phân bằng 100%. Thời gian điện phân t là
A. 7 phút 20 giây.
B. 3 phút 13 giây.
C. 6 phút 26 giây.
D. 5 phút 12 giây.