X là dung dịch NaOH có pH = 12; Y là dung dịch H2SO4 có pH = 2. Để trung hòa 200 ml dung dịch X cần V ml dung dịch Y. Giá trị của V là:
A. 100
B. 200
C. 400
D. 300
X là dung dịch NaOH có pH = 12; Y là dung dịch H2SO4 có pH = 2. Để trung hòa 200 ml dung dịch X cần V ml dung dịch Y. Giá trị của V là:
A. 100
B. 200
C. 400
D. 300
Trộn 100 ml dung dịch NaOH có pH = 11 với 50 ml dung dịch KOH có pH = 12 thu được dung dịch X. Nồng độ ion OH trong dung dịch X là
A. 7 . 10 - 12 M
B. 4 , 3 . 10 - 11 M
C. 4 . 10 - 3 M
D. 7 , 3 . 10 - 2 M
Chọn C
pH = 11 → [ OH - ] = 10 - 3 (M)
pH = 12 → [ OH - ] = 10 - 2 (M)
Tổng số mol OH - có trong dung dịch X là: n = 0 , 1 . 10 - 3 + 0 , 05 . 10 - 2 = 6 . 10 - 4 (mol)
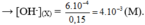
Trộn 100 ml dung dịch H2SO4 xM với 100 ml dung dịch NaOH có pH =12 thu được dung dịch Z có pH = 2. Giá trị x là
A. 0,015 M
B. 0,03M.
C. 0,02 M.
D. 0,04 M.
Đáp án A
pH = 12 => pOH = 2 => [OH-] = 10-2 => n NaOH = 0,01 . 0.1 = 0.001 mol
pH = 2 =>[H+] = 10-2 => dung dịch sau khi trộn dư axit : V dd sau trộn = 0,1+ 0,1 = 0,2 lít
=> n H+ dư = 0,2 . 10-2 = 0,002 mol
H+ + OH-→ H2O
x 0,001
0,002 (dư )
=> n H+ban đầu = 0,003 mol => n H2SO4 = 0,0015 mol
=> CM = 0,015
Chú ý:
Chú ý: tính lại nồng độ khi trộn dung dịch làm nồng độ từng chất bị thay đổi
Trộn V lít dung dịch HCOOH có pH = 2 với V lít dung dịch NaOH có pH = 12 thu được dung dịch X. Dung dịch X có môi trường:
A. trung tính.
B. bazơ.
C. lưỡng tính.
D. axit.
Chọn đáp án D
Chú ý : PH=2 suy ra nồng độ H+ là 0,01.Nhiều bạn sẽ cho môi trường là trung tính ngay.Nhưng các bạn chú ý nhé .HCOOH không điện ly hoàn toàn sau khi H+ đã điện ly phản ứng hết với NaOH nó lại tiếp tục điện ly ra H+ do đó môi trường sẽ là axit
Trộn 240 ml dung dịch HCl có pH =2 với 160 ml dung dịch NaOH có pH = 12, thu được dung dịch có pH là
A. 2,7
B. 3,5
C. 6,0
D. 11,3
Trộn V 1 ml dung dịch NaOH có pH = 13 với V 2 ml dung dịch Ba OH 2 có pH = 11, thu được dung dịch mới có pH = 12. Tỉ số V 1 : V 2 có giá trị là
A. 1/1
B. 2/1
C. 1/10
D. 10/1
Trộn V 1 lít dung dịch H 2 SO 4 có pH = 3 với V 2 lít dung dịch NaOH có pH = 12, thu được dung dịch mới có pH = 4. Tỉ số V 1 : V 2 có giá trị là
A. 8/1
B. 101/9
C. 10/1
D. 4/1
Dung dịch NaOH có pH = 12. Cần pha loãng dung dịch này bao nhiêu lần để thu được dung dịch NaOH mới có pH = 11?
A. 10
B. 100
C. 1000
D. 10000
Đáp án A
Gọi V, V’ lần lượt là thể tích dung dịch NaOH có pH = 12, pH = 11
Do pH = 12 => pOH = 2 => [OH-] = 10-2M => nOH-trước khi pha loãng = 10-2V
pH = 11 => pOH = 3 => [OH-] = 10-3M => nOH-sau khi pha loãng = 10-3V’
Ta có nOH-trước khi pha loãng = nOH-sau khi pha loãng => 10-2V = 10-3V’
![]()
Vậy cần pha loãng dung dịch NaOH 10 lần