Hòa tan 1 mol Fe vào dung dịch chứa 0,5 mol FeCl3 và 1,5 mol HCl, sau khi phản ứng hoàn toàn thu được dung dịch X. Chất tan có trong dung dịch X là
A. FeCl2 và HCl
B. FeCl2.
C. FeCl3 và HCl.
D. FeCl2 và FeCl3.
Hòa tan hoàn toàn x mol Fe vào dung dịch chứa y mol F e C l 3 và z mol HCl, thu được dung dịch chỉ chứa một chất tan duy nhất. Biểu thức liên hệ giữa x, y và z là
A. 2x = y + 2z.
B. x = y – 2z.
C. 2x = y + z.
D. y = 2x.
Hòa tan hoàn toàn x mol Fe vào dung dịch chứa y mol FeCl 3 và z mol HCl, thu được dung dịch chỉ chứa một chất tan duy nhất. Biểu thức liên hệ giữa x, y và z là
A. 2x = y + 2z
B. 2x = y + z
C. x = y – 2z
D. y = 2x
Hòa tan hoàn toàn x mol Fe vào dung dịch chứa y mol FeCl 3 và z mol HCl, thu được dung dịch chỉ chứa một chất tan duy nhất. Biểu thức liên hệ giữa x, y và z là
A. y = 2x
B. 2x = y + z
C. 2x = y + 2z
D. x = y – 2z
Hòa tan hoàn toàn x mol Fe vào dung dịch chứa y mol FeCl3 và z mol HCl, thu được dung dịch chỉ chứa một chất tan duy nhất. Biểu thức liên hệ giữa x, y và z là
A. x = y – 2z.
B. 2x = y + z.
C. 2x = y + 2z.
D. y = 2x.
Đáp án B
Dung dịch sau phản ứng chỉ thu được 1 chất tan duy nhất chính là FeCl2 vì:
Cách 1:Tìm mối liên hệ theo PTHH
Fe + 2HCl → FeCl2 + H2
Fe + 2FeCl3 → 3FeCl2
=> 2 phản ứng trên phải xảy ra hoàn toàn.
=> nFe = ½ nHCl + ½ nFeCl3 => 2x = y + z
Cách 2: Tìm mối liên hệ dựa vào bảo toàn electron
Bảo toàn e ta có: n e nhường = n e nhận => 2nFe = nFe3+ + nH+ => 2x = y + z
Cho a mol Al tan hoàn toàn vào dung dịch chứa b mol HCl thu được dung dịch Y chứa 2 chất tan có cùng nồng độ mol. Thêm từ từ dung dịch NaOH vào dung dịch Y ta có đồ thị sau :
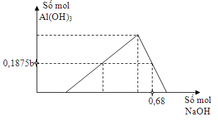
Cho a mol Al tác dụng với dung dịch hỗn hợp chứa 0,15b mol FeCl3 và 0,2b mol CuCl2. Sau khi phản ứng kết thúc thu được m gam chất rắn. Giá trị của m là
A. 11,776
B. 12,896
C. 10,874
D. 9,864
Hòa tan hoàn toàn 7,68 gam bột Cu vào dung dịch chứa FeCl3 và HCl (tỉ lệ số mol 3 : 1), sau phản ứng, thu được dung dịch X chứa 4 chất tan trong đó có 3 chất tan có cùng nồng độ mol. Tiến hành điện phân dung dịch X bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện là 9,65A đến khi khối lượng dung dịch giảm 23,38 gam thì dừng lại. Thời gian điện phân là
A. 4200 giây
B. 4400 giây
C. 4500 giây
D. 4600 giây
Chọn đáp án B
Trong X có CuCl2, FeCl2, FeCl3 và HCl với nCuCl2 = 7,68/64 = 0,12 (BTNT.Cu)
Theo phương trình phản ứng: Cu + 2FeCl3 → CuCl2 + 2FeCl2 ⇒ nFeCl2
= 0,12 . 2 = 0,24
Trường hợp 1: Trong X có nFeCl3 = nHCl = nCuCl2 = 0,12 và nFeCl2 = 0,24
⇒ nFeCl3 ban đầu 12 + 0,24 = 0,36 = 3nHCl ⇒ Thỏa đề bài

Trường hợp 2: Trong X có nFeCl3 = nHCl = nFeCl2 = 0,24 và nCuCl2 = 0,12
⇒ nFeCl3 ban đầu = 0,24 + 0,24 = 0,48 = 2nHCl ⇒ Không thỏa đề bài ⇒ Loại.
Hòa tan hết 35,52 gam hỗn hợp X gồm Mg, Al, FeCl2 và Fe(NO3)2 vào dung dịch chứa 0,816 mol HCl thu được dung dịch Y và 0,144 mol khí NO. Cho từ từ dung dịch AgNO3 vào dung dịch Y đến khi phản ứng xảy ra hoàn toàn thì lượng AgNO3 đã phản ứng là 1,176 mol, thu được 164,496 gam kết tủa, 0,896 lít khí NO2 (đktc) và dung dịch Z chứa m gam muối. Giá trị của m gần nhất với giá trị nào sau đây?
A. 86.
B. 88.
C. 82
D. 84
Cho các phát biểu sau
(1). Hỗn hợp Fe3O4 + Cu (tỉ lệ mol 1:1) có thể tan hết trong dung dịch HCl dư.
(2). Cho dung dịch FeCl2 tác dụng với dung dịch AgNO3 dư, chất rắn thu được gồm AgCl và Ag.
(3). Hỗn hợp kim loại Al, Fe tan hoàn toàn trong dung dịch H2SO4 đặc, nguội.
(4). Hỗn hợp Na và Al2O3 (có tỉ lệ mol 2:1) có thể tan hoàn toàn trong nước.
(5). Cho kim loại Mg dư vào dung dịch FeCl3 sau phản ứng thu được dung dịch chứa 2 muối tan.
(6). Hỗn hợp kim loại Cu và Ag có thể tan hoàn toàn trong dung dịch gồm KNO3 + H2SO4 loãng.
(7). Kim loại cứng nhất là W, kim loại có nhiệt độ nóng chảy thấp nhất là Hg.
Số phát biểu đúng là
A. 4
B. 5
C. 2
D. 3
Chọn B.
(1) Đúng, Fe3O4 + 8HCl ® FeCl2 + 2FeCl3 + 4H2O và Cu + 2FeCl3 ® FeCl2 + CuCl2.
(2) Đúng, FeCl2 + AgNO3 ® Fe(NO3)3 + AgCl + Ag.
(3) Sai, Al, Fe bị thụ động hoá bởi dung dịch H2SO4 đặc nguội.
(4) Đúng, 2Na + 2H2O ® 2NaOH + H2 và Al2O3 + 2NaOH ® 2NaAlO2 + H2O.
(5) Đúng, Mg + 2FeCl3 ® MgCl2 + 2FeCl2 sau đó Mg + FeCl2 ® MgCl2 + Fe.
(6) Đúng, Cu và Ag có thể hoà tan được dung dịch chứa ion H+ và NO3–.
(7) Sai, Kim loại cứng nhất là Cr, kim loại có nhiệt độ nóng chảy thấp nhất là Hg.
hòa tan 9,6g Mg vao 400 ml dung dịch FeCl3 0,5 mol/l người ta thu được dung dịch A và hỗn hợp rắn B.
a)Tính nồng độ mol/l của chất tan trong dung dich A.(Biết thễ tích dung dịch không thay đổi và các phản ứng hoàn toàn)
b)Hỗn hợp B tan hoàn tàn trong dung dịch HCl 30%(d=1,123 g/ml). Tính thể tích dung dịch HCl đã dùng.
Do sau phản ứng là hh chất rắn nên Mg dư, FeCl3 hết
PTHH
Mg + 2FeCl3 --> MgCl2 + 2FeCl2
x 2x 2x
Mg + FeCl2 --> MgCl2 + Fe
2x 2x 2x
3Mg + 2FeCl3 --> 3MgCl2 + 2Fe
y 2/3y 2/3y
Theo PTHH ta có: nFeCl3 = nFe = 0.2
2nMg = 3nFe = 0.3
nMg = nMgCl2 = 0.3
Nồng độ mol của các chất trong hh:
CmFeCl2 = 0.2/0.4 = 0.5M
CmMgCl2 = 0.3/0.4 = 0.75M
PTHH
Fe + 2HCl --> FeCl2 + H2
0.2 0.4
Mg + 2HCl --> MgCl2 + H2
0.3 0.6
Khối lượng HCl cần dùng: m = 1*36.5 = 36.5g
với lại bài này có cho Mg tác dụng với FeCl2 hay là chỉ cho tác dụng với FeCl3 với lại cho mình bik vì sao khi làm nhớ giải thích giùm mình nhé thank you