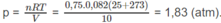Một bình kín chứa 1 mol khí nitơ ở áp suất 10 5 N / m 2 ở 27 ° C
Thể tích của bình xấp xỉ bằng bao nhiêu?
A. 2,5l
B. 2,8 l
C. 25 l
D. 27,7 l
Một bình kín chứa 1 mol khí nitơ ở áp suất 10 5 N / m 2 ở 27°C. Nung bình đến khi áp suất khí là 5. 10 5 N/m:. Nhiệt độ khí bây giở là?
A. 127 ° C
B. 60 ° C
C. 135 ° C
D. 1227 ° C
Một bình kín chứa 1 mol khí nitơ ở áp suất 10 5 N / m 2 ở 27 ° C
Nung bình đến khi áp suất khí là 5 . 10 5 N / m 2 .Nhiệt độ khí bây giờ là?
A. 127 ° C
B. 60 ° C
C. 135 ° C
D. 1227 ° C
Đáp án D.
Ta có: p 1 T 1 = p 2 T 2 ⇒ T 2 = p 2 p 1 . T 1 = 1500 K = 1227 0 C
Một bình kín chứa 1 mol khí nitơ ở áp suất 10 5 N / m 2 ở 27 ° C. Khi đó van điều áp mở ra và 1 lượng khí thoát ra ngoài, nhiệt độ vẫn giữ không đổi. Sau đó áp suất giảm còn 4. 10 4 N / m 2 lượng khí đã thoát ra là bao nhiêu?
A. 0,8 mol
B. 0,2mol
C. 0,4 mol
D. 0,1 mol
Chọn đáp án B
? Lời giải:
+ Do V, T không đổi nên ta có:
v 3 = p 3 p 2 . v 1 = 0 , 8 mol
khí thoát ra 0,2 mol.
Một bình kín chứa 1 mol khí nitơ ở áp suất 10 5 N / m 2 ở 27 ° C
Khi đó van điều áp mở ra và 1 lượng khí thoát ra ngoài , nhiệt độ vẫn giữ không đổi. Sau đó áp suất giảm còn 4 . 10 4 N / m 2 lượng khí đã thoát ra là bao nhiêu?
A. 0,8 mol
B. 0,2mol
C. 0,4 mol
D. 0,1 mol
Một bình kín chứa 1 moi khí nitơ ở áp suất 10 5 N / m 2 ở 27 ° C. Thể tích của bình xấp xỉ bằng bao nhiêu?
A. 2,5ℓ
B. 2,8 ℓ
C. 25 ℓ
D. 27,7 ℓ
Nén hỗn hợp gồm 4 mol nitơ, 16 mol hiđro vào một bình kín có thể tích 4 lít (chỉ chứa xúc tác với thể tích không đáng kể) và giữ ở nhiệt độ không đổi. Khi phản ứng trong bình đạt cân bằng, áp suất trong bình bằng 0,8 lần áp suất ban đầu. Tính hằng số cân bằng của phản ứng.
Một bình kín chứa một lượng khí Nito xác định ở áp suất 105 N/m , nhiệt độ 27 độ C . Nung bình đến khi áp suất khí là 5.105 N/m2 . Nhiệt độ khí sau khi nung nóng là
Trạng thái 1: \(\left\{{}\begin{matrix}p_1=10^5Pa\\T_1=27^oC=300K\end{matrix}\right.\)
Trạng thái 2: \(\left\{{}\begin{matrix}p_2=5\cdot10^5Pa\\T_2=???\end{matrix}\right.\)
Quá trình đẳng tích:
\(\dfrac{p_1}{T_1}=\dfrac{p_2}{T_2}\Rightarrow\dfrac{10^5}{300}=\dfrac{5\cdot10^5}{T_2}\)
\(\Rightarrow T_2=1500K=1227^oC\)
Một bình kín chứa 1 mol khí Nito, áp suất 10 5 Pa, ở nhiệt độ 27 ° C . Do có một lượng khí thoát ra ngoài nên áp suất của khí trong bình chỉ còn 0,8. 10 5 Pa, nhiệt độ vẫn được giữ không đổi. Lượng khí đã thoát ra ngoài bằng:
A. 0,4mol
B. 0,8mol
C. 0,2mol
D. 0,1mol
Đáp án: C
Ban đầu, khí Nito có khối lượng mm, thể tích V, áp suất p, nhiệt độ T
PT: p 1 V = m M R T 1
- Sau một thời gian, khí Heli có khối lượng m′, thể tích V, áp suất p2, nhiệt độ T
PT: p 2 V = m ' M R T 2
Lấy 2 1 ta được:
p 2 p 1 = m ' m ↔ 0,8 1 = m ' m → m ' = 0,8 m
=> Lượng khí Nito đã thoát ra:
Δ m = m − m ' = m − 0,8 m = 0,2 m = 0,2.1.28 = 5,6 g
Số mol khí Nito thoát ra ngoài là: n = m M = 5,6 28 = 0,2 m o l
Vậy lượng khí đã thoát ra ngoài bằng: 0,2mol
Trong một bình kín dung tích 10,0 lít chứa 21,0 g nitơ. Tính áp suất của khí trong bình, biết nhiệt độ của khí bằng 25 ° C .
Cần áp dụng phương trình trạng thái khí pV = nRT, trong đó p là áp suất của khí trong bình kín (atm) ; V là thể tích của khí (lít), n là số mol khí trong thể tích V ; T là nhiệt độ tuyệt đối (K) với T = t( ° C ) + 273 ; R là hằng số lý tưởng, với trị số
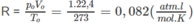
Số mol khí
N
2
: 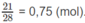
Áp suất của khí N 2 :