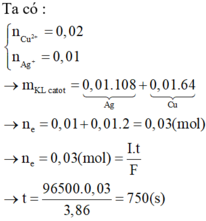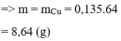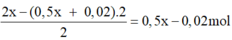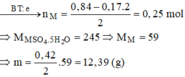Cho 61,25 gam tinh thể MSO4.5H2O vào 300 ml dung dịch NaCl 0,6M thu được dung dịch X. Tiến hành điện phân (điện cực trơ, màng ngăn xốp, hiệu suất điện phân 100%, bỏ qua sự hòa tan của khí trong nước và sự bay hơi của nước) dung dịch X với cường độ dòng điện không đổi, trong thời gian t giây, thấy khối lượng catot tăng m gam, đồng thời ở anot thu được 0,15 mol khí. Nếu thời gian điện phân là 2t giây, tổng số mol khí thoát ra ở hai cực là 0,425 mol. Giá trị của m là A. 13,44 B. 11,80 C. 12,80 D...
Đọc tiếp
Cho 61,25 gam tinh thể MSO4.5H2O vào 300 ml dung dịch NaCl 0,6M thu được dung dịch X. Tiến hành điện phân (điện cực trơ, màng ngăn xốp, hiệu suất điện phân 100%, bỏ qua sự hòa tan của khí trong nước và sự bay hơi của nước) dung dịch X với cường độ dòng điện không đổi, trong thời gian t giây, thấy khối lượng catot tăng m gam, đồng thời ở anot thu được 0,15 mol khí. Nếu thời gian điện phân là 2t giây, tổng số mol khí thoát ra ở hai cực là 0,425 mol. Giá trị của m là
A. 13,44
B. 11,80
C. 12,80
D. 12,39