Trong bảng tuần hoàn các nguyên tố hóa học, nguyên tố X ở nhóm IA, nguyên tố Y ở nhóm VIA. Công thức của hợp chất tạo thành từ 2 nguyên tố trên có dạng là
A. X2Y3
B. X2Y
C. XY
D. X5Y2
Trong bảng tuần hoàn các nguyên tố hóa học, nguyên tố X ở nhóm IA, nguyên tố Y ở nhóm VIA. Công thức của hợp chất tạo thành từ 2 nguyên tố trên có dạng là
A. X2Y3
B. X2Y
C. XY
D. X5Y2
Đáp án B
Do X dễ nhường 1 electron để đạt cấu hình bền vững → X có số oxi hóa +1
Y dễ nhận 2 electron để đạt cấu hình bền vững → Y có số oxi hóa -2
→ Công thức phù hợp là X2Y
Cho 2 nguyên tố X và Y thuộc hai chu kì liên tiếp ( Z X < Z Y ) và cùng số thứ tự của nhóm trong bảng tuần hoàn (nhóm A và nhóm B).
- Nguyên tố X tạo thành hợp chất ion với clo ứng với công thức XC1.
- Nguyên tố Y cũng tạo thành hợp chất với clo hợp chất YC1 trong đó khối lượng của clo chiếm 24,7%.
Xác định các nguyên tố X và Y.
X tạo bởi chất ion với clo có công thức là XC1, vậy X là kim loại có hoá trị I.
Y cùng số nhóm với X vậy cũng có hoá trị I, công thức clorua của nó là YC1.
Ta có:
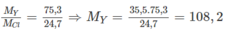
( M Y và M Cl lần lượt là NTK của nguyên tố Y và nguyên tố clo). Đó là Ag. Nguyên tố X cùng chu kì, cùng số thứ tự nhóm với Ag là kali (K))
Cho nguyên tố X thuộc chu kì 3 , nhóm IA , nguyên tố Y số e ở phân lớp P là 2 , Nguyên tố Z thuộc nhóm VIA có tổng số hạt cơ bản (p,e,n) là 24
a. Xác định nguyên tố X Y Z
b. viết phương trình tạo thành Ion từ X,Y,Z
c.Giải thích sự tạo thành liên kết giữa X và Z
a/ntố X ở chu kì 3 \(\Rightarrow\)có 3 lớp e.nhóm IA \(\Rightarrow\)CHe kết thúc ở 3s\(^1\)\(\Rightarrow\)CHe là .\(\Rightarrow\) z=......
ntố Y có số e phân lớp P là 2\(\Rightarrow\) CHe kết thúc ở 2p\(^2\) \(\Rightarrow\) CHe là .....
ntố Z có 2Z+N=24.áp dụng công thức Z\(\le\) N\(\le\) 1,5Z.công vào mỗi vế 2Z đẻ có 2z+n=24\(\Rightarrow\) z=.....(có vài trường hợp bạn tự loại nha)
b/ từ phần a là tự suy ra đc mà!GOOD LUCK!
Các nguyên tố thuộc nhóm VIIA gồm những nguyên tố nào ?
Nguyên tử của các nguyên tố thuộc nhóm này có bao nhiêu electron hoá trị ?
Khi hai nguyên tử của cùng một nguyên tố thuộc nhóm này liên kết với nhau tạo thành phân tử thì mỗi nguyên tử phải góp bao nhiêu electron, tạo thành mấy liên kết, tại sao ? Cho thí dụ.
Các nguyên tố thuộc nhóm VIIA gồm các nguyên tố : flo (F), clo (Cl), brom (Br), iot (I), atatin (At). Nguyên tử của chúng có 7 electron hoá trị.
Khi hai nguyên tử của cùng một nguyên tố thuộc nhóm này liên kết với nhau tạo thành phân tử thì mỗi nguyên tử góp 1 electron, tạo thành một cặp electron chung tức là một liên kết, vì mỗi nguyên tử chỉ thiếu electron để đạt được cấu hình 8 electron vững bền (giống như của khí hiếm đứng sau nó).
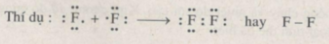
Cho 3 nguyên tố X, Y, M thuộc nhóm A của bảng tuần hoàn. X, Y cùng một chu kì và thuộc hai nhóm liên tiếp. M, X thuộc cùng một nhóm và ở hai chu kì liên tiếp. Tính kim loại: M > X > Y. Nguyên tử của nguyên tố X có 2 electron lớp ngoài cùng thuộc phân lớp 3s.
a. Viết cấu hình electron nguyên tử của X, Y, M.
b. Viết công thức hiđroxit ứng với oxit bậc cao nhất của Y.
Trong bảng tuần hoàn các nguyên tố hóa học, các nguyên tố thuộc nhóm nào sau đây có hoá trị cao nhất với oxi bằng 5?
A. Nhóm VIIA. B. Nhóm VA. C. Nhóm VIA. D. Nhóm IIA.
Nguyên tố X và Y thuộc nhóm A;nguyên tử nguyên tố X có 7 electron trên các phân lớp s, nguyên tử nguyên tố Y có 17 electron trên các phân lớp p.Công thức hợp chất tạo bởi X và Y; liên kết hóa học trong hợp chất đó là:
A. XY; liên kết ion.
B. Y2X; liên kết ion.
C. X5Y; liên kết cộng hoá trị.
D. X7Y; liên kết cộng hoá trị.
Đáp án A
Nguyên tử nguyên tố X có 7 electron trên các phân lớp s
⇒ X: 1s22s23s24s25s1
Vì thuộc nhóm A nên X thuộc nhóm IA
nguyên tử nguyên tố Y có 17 electron trên các phân lớp p
⇒ Y: 2p63p64p5 ⇒ 4s24p5
Vì Y thuộc nhóm A ⇒ X thuộc nhóm VIIA
⇒ Hợp chất XY: liên kết ion
X thuộc chu kì 3, nhóm IA, Y thuộc chu kì 3, nhóm VIIA. Công thức phân tử và bản chất liên kết của hợp chất giữa X và Y là
A. X 2 Y ; liên kết ion B. XY ; liên kết ion.
C. XY 2 ; liên kết cộng hoá trị. D. X 2 Y 2 ; liên kết cộng hoá trị.
Một hợp chất ion có công thức XY. Hai nguyên tố X,Y thuộc 2 chu kì kế cận nhau trong bảng tuần hoàn. X thuộc nhóm IA hoặc IIA, còn Y thuộc VIA hoặc VIIA. Biết tổng số electron trong XY bằng 20. XY là hợp chất nào sau đây
A. NaCl
B. NaF
C. MgO
D. B và C đúng
Đáp án D
Hướng dẫn X thuộc nhóm IA,IIA nên có điện hóa trị +1,+2
Y thuộc cùng nhóm VIA,VIIA nên Y có điện hóa trị -2 và -1
Ngoài ra ZX + ZY = 20. Vì X, Y thuộc hai chu kì kế cận nên nghiệm thích hợp là
ZX = 11 thì ZY = 9 ; X là Na , Y là F và XY là NaF
ZX = 12 thì ZY = 8 ; X là Mg , Y là O và XY là MgO
Câu 6: X và Y là 2 nguyên tố ở cùng 1 nhóm A và thuộc 2 chu kì liên tiếp trong bảng hệ thống
tuần hoàn. Tổng số proton trong 2 hạt nhân nguyên tử X và Y bằng 30. Hãy viết cấu hình
electron của X, Y và của các ion mà X và Y có thể tạo thành.