Ion M - có cấu hình electron phân lớp ngoài cùng là 3 p 6 . Số proton trong hạt nhân của nguyên tử M là
A. 19
B. 18
C. 17
D. 16
Tổng số hạt proton, nơtron, electron của ion M 2 + là 34, biết rằng số hạt mang điện nhiều hơn số hạt không mang điện là 10. Cấu hình electron phân lớp ngoài cùng của nguyên tử M là
A. 2 p 4
B. 2 p 6
C. 3 s 2
D. 3 p 2
Trong hạt nhận nguyên tử X có số hạt nơtron bằng số hạt proton. Cấu hình electron của X có phân lớp ngoài cùng là 3s2. Số khối của X là
A. 36
B. 24.
C. 12.
D. 18.
Đáp án B
Cấu hình electron của X có phân lớp ngoài cùng là 3s2 => Cấu hình electron của X là 1 s 2 2 s 2 2 p 6 3 s 2
=>X có 12 proton
Trong hạt nhân nguyên tử X có số hạt nơtron bằng số hạt proton => X có 12 nơtron
A = Z + N = l2 + 12 = 24
Ion X + có cấu hình electron phân lớp ngoài cùng là 4 p 6 . Số khối của ion này là 87. Số hạt nơtron trong nguyên tử X là
A. 48
B. 49
C. 50
D. 51
Hợp chất H có công thức MX2 trong đó M chiếm 140/3% về khối lượng, X là phi kim ở chu kỳ 3, trong hạt nhân của M có số proton ít hơn số nơtron là 4; trong hạt nhân của X có số proton bằng số nơtron. Tổng số proton trong 1 phân tử A là 58.
Cấu hình electron ngoài cùng của M là.
A. 3d104s1.
B. 3s23p4.
C. 3d64s2.
D. 2s22p4.
Đáp án C
Tổng số proton trong MX2 là 58 hạt
→ ZM + 2.ZX = 58
Trong hạt nhân M có số notron nhiều hơn số hạt proton là 4 hạt
→ -ZM + NM = 4
Trong hạt nhân X, số notron bằng số proton → ZX = NX
MA =ZM + NM + 2.ZX + 2.NX
= (ZM + 2.ZX ) + NM + 2NX
= 58 + NM + 58 - ZM = 116 + NM- ZM
M chiếm 46,67% về khối lượng
![]()
![]()
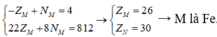
![]()
Cấu hình electron của M là [Ar]3d64s2.
Hợp chất H có công thức M X 2 trong đó M chiếm 140 3 % về khối lượng, X là phi kim ở chu kỳ 3, trong hạt nhân của M có số proton ít hơn số nơtron là 4; trong hạt nhân của X có số proton bằng số nơtron. Tổng số proton trong 1 phân tử H là 58. Cấu hình electron ngoài cùng của M là
A. 3 d 10 4 s 1
B. 3 s 2 3 p 4
C. 3 d 6 4 s 2
D. 2 s 2 2 p 4
Chọn C
Tổng số proton trong MX2 là 58 hạt → ZM + 2.ZX = 58
Trong hạt nhân M có số nơtron nhiều hơn số hạt proton là 4 hạt → -ZM + NM = 4
Trong hạt nhân X, số nơtron bằng số proton → ZX = NX
MH =ZM + NM + 2.ZX + 2.NX = (ZM + 2.ZX ) + NM + 2NX = 58 + NM + 58 - ZM = 116 + NM - ZM

Hợp chất H có công thức MX2 trong đó M chiếm 140 3 % về khối lượng, X là phi kim ở chu kỳ 3, trong hạt nhân của M có số proton ít hơn số nơtron là 4; trong hạt nhân của X có số proton bằng số nơtron. Tổng số proton trong 1 phân tử H là 58. Cấu hình electron ngoài cùng của M là.
A. 3 d 10 4 s 1
B. 3 s 2 3 p 4
C. 3 d 6 4 s 2
D. 2 s 2 2 p 4
Nguyên tử của nguyên tố Y nhận thêm 1 electron thì tạo thành ion Y - có cấu hình electron lớp ngoài cùng là 2 p 6 . Trong hạt nhân của Y có 10 nơtron. Số khối của Y là
A. 19
B. 20
C. 16
D. 9
Nguyên tử nguyên tố X có tổng số hạt (proton, nơtron, electron) là 115, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 25 hạt. Cấu hình electron lớp ngoài cùng của X là
A. 4 s 2
B. 4 s 2 4 p 5
C. 3 s 2 3 p 5
D. 3 d 10 4 s 1
B
Gọi số proton, nơtron và electron của X là p, n và e (trong đó p = e)
Theo bài ra ta có hệ phương trình:
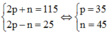
=> Cấu hình nguyên tử của X là
![]()
Bài 1. Nguyên tử X có tổng số proton, nơtron, electron là 116 trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 24. Xác định X, viết cấu hình electron của X.
Bài 2 a.Nguyên tử của nguyên tố X có cấu hình electron lớp ngoài cùng là 4s24p4 . Hãy viết cấu hình electron của nguyên tử X.
b.Nguyên tử của nguyên tố Y có tổng số electron ở các phân lớp p là 11. Hãy viết cấu hình electron của nguyên tử Y.
Bài 1:
Ta có:p+e+n=116
Tức là :2p+n=116 (pt 1)
Số hạt mang điện trong ng tử là p và nên ta có p+e =2p
Số hạt không mang điện là n
Nên ta có 2p -n=24(pt2)
Từ 1,2 suy ra 2p+n=16
2p -n =24
Giải ra ta được:p=35,n=46
Số khối A=p+n =35+46=81
Ta có kí hiệu ngtu 81x35(xin lỗi mik ko ghi được)