Cho các ion kim loại : Zn2+; Sn2+; Ni2+; Fe2+; Pb2+ . Thứ tự tính oxi hóa giảm dần là
A. Pb2+ > Sn2+ >Ni2+ > Fe2+ > Zn2+
B. Sn2+ >Ni2+ >Zn2+ > Pb2+ > Fe2+
C. Zn2+ > Sn2+ >Ni2+ >Fe2+ >Pb2+
D. Pb2+ > Sn2+> Fe2+ >Ni2+ > Zn2+
Cho các ion kim loại: Zn2+, Sn2+, Ni2+, Fe2+, Pb2+. Thứ tự oxi hóa giảm dần là
A. Pb2+ > Sn2+ > Fe2+ > Ni2+ > Zn2+.
B. Sn2+ > Ni2+ > Zn2+ > Pb2+ > Fe2+.
C. Zn2+ > Sn2+ > Ni2+ > Fe2+ > Pb2+.
D. Pb2+ > Sn2+ > Ni2+ > Fe2+ > Zn2+.
Cho các ion kim loại: Zn2+, Sn2+, Ni2+, Fe2+, Pb2+. Thứ tự oxi hóa giảm dần là
A. Pb2+ > Sn2+ > Fe2+ > Ni2+ > Zn2+.
B. Sn2+ > Ni2+ > Zn2+ > Pb2+ > Fe2+.
C. Zn2+ > Sn2+ > Ni2+ > Fe2+ > Pb2+.
D. Pb2+ > Sn2+ > Ni2+ > Fe2+ > Zn2+.
Đáp án D
D đúng vì thứ tự cặp oxi hóa – khử là:
![]()
→ Thứ tự tính oxi hóa giảm dần:
Pb2+ > Sn2+ > Ni2+ > Fe2+ > Zn2
Cho các ion kim loại: Zn2+, Sn2+, Ni2+, Fe2+, Pb2+. Thứ tự oxi hóa giảm dần là
A. Pb2+ > Sn2+ > Fe2+ > Ni2+ > Zn2+.
B. Sn2+ > Ni2+ > Zn2+ > Pb2+ > Fe2+.
C. Zn2+ > Sn2+ > Ni2+ > Fe2+ > Pb2+.
D. Pb2+ > Sn2+ > Ni2+ > Fe2+ > Zn2+.
thứ tự cặp oxi hóa – khử là:
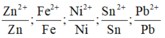
Thứ tự tính oxi hóa giảm dần: Pb2+ > Sn2+ > Ni2+ > Fe2+ > Zn2+
Đáp án D
Có các ion kim loại : Zn2+, Sn2+, Ni2+, Fe2+, Pb2+. Thư tư tinh oxi hoa cua cac ion kim loai giam dân là
A. Pb 2+ > Sn2+ > Fe2+ > Ni2+ > Zn2+
B. Sn2+ > Ni2+ > Zn2+ > Pb2+ > Fe2+
C. Pb2+ > Sn2+ > Ni2+ > Fe2+ > Zn2+
D. Zn2+ > Sn2+ > Ni2+ > Fe2+ > Pb2+
Áp dụng dãy điện hóa, tính oxi hóa giảm dần theo chiều ngược so với tính khử (bình thường thứ tự của dãy điện hóa trong sách là giảm dần của tính khử)
=> Pb2+ > Sn2+ > Ni2+ > Fe2+ > Zn2+
Đáp án C
Cho các ion kim loại: Z n 2 + , S n 2 + , N i 2 + , F e 2 + , P b 2 + . Thứ tự tính oxi hoá giảm dần là
A. P b 2 + , S n 2 + , F e 2 + , N i 2 + , Z n 2 +
B. S n 2 + , N i 2 + , Z n 2 + , P b 2 + , F e 2 +
C. Z n 2 + > S n 2 + > N i 2 + > F e 2 + > P b 2 +
D. P b 2 + > S n 2 + > N i 2 + > F e 2 + > Z n 2 +
Cho các ion kim loại: Z n 2 + , S n 2 + , N i 2 + , F e 2 + , P b 2 + . Thứ tự tăng dần tính oxi hóa là
A. P b 2 + , S n 2 + , F e 2 + , N i 2 + , Z n 2 +
B. Z n 2 + , F e 2 + , N i 2 + , S n 2 + , P b 2 +
C. Z n 2 + , F e 2 + , S n 2 + , N i 2 + , P b 2 +
D. P b 2 + , S n 2 + , N i 2 + , F e 2 + , Z n 2 +
Cho các ion kim loại: Zn2+, Sn2+, Ni2+, Fe2+, Pb2+. Thứ tự tính oxi hoá giảm dần là
A. Pb2+ > Sn2+ > Fe2+ > Ni2+ > Zn2+.
B. Sn2+ > Ni2+ > Zn2+ > Pb2+ > Fe2+.
C. Zn2+ > Sn2+ > Ni2+ > Fe2+ > Pb2+.
D. Pb2+ > Sn2+ > Ni2+ > Fe2+ > Zn2+.
Đáp án D
Thứ tự tính khử tăng dần: Pb < Sn < Ni < Fe < Zn
Nên tính oxi giảm dần: Pb2+ > Sn2+ > Ni2+ >
Fe2+ > Zn2+
Cho các ion kim loại: Zn2+, Sn2+, Ni2+, Fe2+, Pb2+. Thứ tự tính oxi hóa giảm dần là
A. Pb2+ > Sn2+ > Fe2+ > Ni2+> Zn2+
B. Sn2+ > Ni2+ > Zn2+ > Pb2+> Fe2+
C. Zn2+ > Sn2+ > Ni2+ > Fe2+> Pb2+
D. Pb2+ > Sn2+ > Ni2+ > Fe2+> Zn2+
Cho biết thứ tự từ trái sang phải của các cặp oxi hóa – khử trong dãy điện hóa như sau: Zn2+/Zn; Fe2+/Fe; Cu2+/ Cu; Fe3+/Fe2+; Ag+/Ag. Các kim loại và ion đều phản ứng được với ion Fe2+ trong dung dịch là
A. Ag, Fe3+.
B. Zn, Ag+.
C. Ag, Cu2+.
D. Zn, Cu2+.