Khi điều chế Zn từ dung dịch ZnSO4 bằng phương pháp điện phân với điện cực trơ, ở anot xảy ra quá trình
A. Khử ion kẽm
B. Khử nước
C. Oxi hóa nước
D. Oxi hóa kẽm
Sự điện phân là quá trình oxi hóa – khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện ly nóng chảy hoặc dung dịch chất điện ly nhằm thúc đẩy một phản ứng hóa học mà nếu không có dòng điện, phản ứng sẽ không tự xảy ra. Trong thiết bị điện phân: * Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều. * Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều. Cho dãy điện hóa sau:
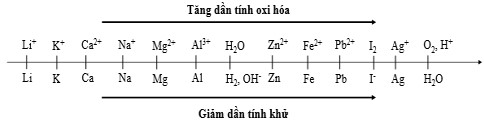
Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời P b N O 3 2 và M g N O 3 2 bằng hệ điện phân sử dụng các điện cực than chì.
Dựa theo dãy điện hóa đã cho ở trên và từ Thí nghiệm, hãy cho biết
Bán phản ứng nào xảy ra ở catot
A. P b 2 + + 2 e → P b
B. M g 2 + + 2 e → M g
C. O 2 + 4 H + + 4 e → 2 H 2 O
D. H 2 O + 2 e → H 2 + 2 O H -
Sự điện phân là quá trình oxi hóa – khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện ly nóng chảy hoặc dung dịch chất điện ly nhằm thúc đẩy một phản ứng hóa học mà nếu không có dòng điện, phản ứng sẽ không tự xảy ra. Trong thiết bị điện phân: * Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều. * Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều. Cho dãy điện hóa sau:
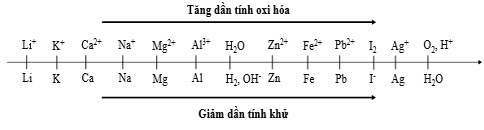
Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời thời P b N O 3 2 và M g N O 3 2 bằng hệ điện phân sử dụng các điện cực than chì.
Bán phản ứng nào xảy ra ở anot
A. P b → P b 2 + + 2 e
B. M g → M g 2 + + 2 e
C. 2 H 2 O → O 2 + 4 H + + 4 e
D. 4 N O 3 - → 2 N 2 O 5 + O 2 + 4 e
Sự ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường xung quanh. Đó là một quá trình hóa học hoặc quá trình điện hóa trong đó kim loại bị oxi hóa thành ion dương.
M → M n + + n e
Có hai dạng ăn mòn kim loại là ăn mòn hóa học và ăn mòn điện hóa học: - Ăn mòn hóa học là quá trình oxi hóa - khử, trong đó các electron của kim loại được chuyển trực tiếp đến các chất trong môi trường.
- Ăn mòn điện hóa học là quá trình oxi hóa - khử, trong đó kim loại bị ăn mòn do tác dụng của dung dịch chất điện li và tạo nên dòng electron chuyển dời từ cực âm đến cực dương.
Thí nghiệm 1: Tiến hành thí nghiệm theo các bước sau: Bước 1: Rót dung dịch H 2 S O 4 loãng vào cốc thủy tinh.
Bước 2: Nhúng thanh kẽm và thanh đồng (không tiếp xúc nhau) vào cốc đựng dung dịch H 2 S O 4 loãng.
Bước 3: Nối thanh kẽm với thanh đồng bằng dây dẫn (có mắc nối tiếp với một điện kế).
Thí nghiệm 2: Để 3 thanh hợp kim: Cu-Fe (1); Fe-C (2); Fe-Zn (3) trong không khí ẩm
Trong Thí nghiệm 1, thanh kẽm và thanh đồng được nối với nhau bằng dây dẫn cùng nhúng trong dung dịch chất điện li tạo thành một cặp pin điện hóa. Quá trình xảy ra tại anot của pin điện này là
A. Z n → Z n 2 + + 2 e
B. C u → C u 2 + + 2 e
C. 2 H + + 2 e → H 2
D. C u 2 + + 2 e → C u
Sự điện phân là quá trình oxi hóa – khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện ly nóng chảy hoặc dung dịch chất điện ly nhằm thúc đẩy một phản ứng hóa học mà nếu không có dòng điện, phản ứng sẽ không tự xảy ra. Trong thiết bị điện phân: * Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều. * Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều. Cho dãy điện hóa sau:
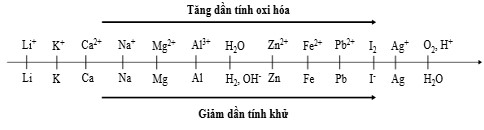
Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời thời P b N O 3 2 và M g N O 3 2 bằng hệ điện phân sử dụng các điện cực than chì.
Dựa theo dãy điện hóa đã cho ở trên và từ Thí nghiệm hãy cho biết
Nếu người sinh viên đổi 2 điện cực than chì bằng 2 điện cực kim loại Pb, phản ứng nào xảy ra ở catot và anot
A. C a t o t : P b 2 + + 2 e → P b ; A n o t : 2 H 2 O → O 2 + 4 H + + 4 e
B. C a t o t : M g 2 + + 2 e → M g ; A n o t : P b → P b 2 + + e
C. C a t o t : 2 H 2 O + 2 e → H 2 + 2 O H - ; A n o t : P b → P b 2 + + e
D. C a t o t : P b 2 + + 2 e → P b ; A n o t : P b → P b 2 + + e
Cho các phát biểu sau:
(a) Ag là kim loại dẫn điện tốt nhất còn Cr là kim loại cứng nhất.
(b) Phản ứng hóa học giữa Hg và S xảy ra ngay ở điều kiện thường.
(c) Ăn mòn hóa học là quá trình oxi hóa khử, trong đó các electron của kim loại được chuyển từ cực âm đến cực dương.
(d) Kim loại Cu chỉ có thể điều chế bằng phương pháp điện phân dung dịch muối của nó.
Số phát biểu đúng là
A. 1
B. 4
C. 3
D. 2
Đáp án : D
(c) Sai vì Ăn mòn hòa học thì electron chuyển trực tiếp từ chất cho sang chất nhận
(d) Sai vì Cu có thể được điều chế bằng phương pháp thủy luyện , nhiệt luyện hoặc điện phân đều được
Cho các phát biểu sau:
(a) Ag là kim loại dẫn điện tốt nhất còn Cr là kim loại cứng nhất.
(b) Phản ứng hóa học giữa Hg và S xảy ra ngay ở điều kiện thường.
(c) Ăn mòn hóa học là quá trình oxi hóa khử, trong đó các electron của kim loại được chuyển từ cực âm đến cực dương.
(d) Kim loại Cu chỉ có thể điều chế bằng phương pháp điện phân dung dịch muối của nó.
Số phát biểu đúng là
A. 1.
B. 4.
C. 3.
D. 2.
Cho các phát biểu sau:
(a) Ag là kim loại dẫn điện tốt nhất còn Cr là kim loại cứng nhất.
(b) Phản ứng hóa học giữa Hg và S xảy ra ngay ở điều kiện thường.
(c) Ăn mòn hóa học là quá trình oxi hóa khử, trong đó các electron của kim loại được chuyển từ cực âm đến cực dương.
(d) Kim loại Cu chỉ có thể điều chế bằng phương pháp điện phân dung dịch muối của nó.
Số phát biểu đúng là
A. 1.
B. 4.
C. 3.
D. 2.
Đáp án D
2 phát biểu đúng là (a) và (b). 2 phát biểu còn lại sai, vì :
Ăn mòn hóa học là quá trình oxi hóa – khử, trong đó electron của kim loại được chuyển trực tiếp từ kim loại sang chất oxi hóa trong môi trường.
Cu có thể được điều chế bằng phương pháp điện phân dung dịch, thủy luyện hay nhiệt luyện.
Sự điện phân là quá trình oxi hóa – khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện ly nóng chảy hoặc dung dịch chất điện ly nhằm thúc đẩy một phản ứng hóa học mà nếu không có dòng điện, phản ứng sẽ không tự xảy ra. Trong thiết bị điện phân: * Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều. * Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều. Cho dãy điện hóa sau:
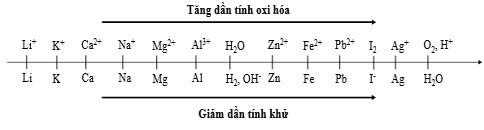
Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời thời P b N O 3 2 và M g N O 3 2 bằng hệ điện phân sử dụng các điện cực than chì.
Dựa theo dãy điện hóa đã cho ở trên và từ Thí nghiệm hãy cho biết Giá trị pH của dung dịch thay đổi như thế nào?
A. pH tăng do OH- sinh ra ở catot
B. pH giảm do H+ sinh ra ở anot
C. pH không đổi do không có H+ và OH- sinh ra
D. pH không đổi do lượng H+ sinh ra ở anot bằng với lượng OH- sinh ra ở catot
Cho các phát biểu sau:
(1) Sắt là kim loại phổ biến thứ 2 trong vỏ trái đất.
(2) Để điều chế kim loại nhôm, người ta có thể dùng phương pháp thủy luyện, nhiệt luyện hoặc điện phân.
(3) Trong công nghiệp, quặng sắt có giá trị để sản xuất gang là hemantit và manhetit.
(4) Sắt tây (sắt tráng thiếc), tôn (sắt tráng kẽm) khi để trong không khí ẩm và bị trày xước sau đến lớp bên trong thì sắt tây bị ăn mòn nhanh hơn tôn.
(5) NaHCO3 có thể dùng làm thuốc chứa bệnh, tạo nước giải khát có ga.
(6) Thứ tự bị khử ở catot khi điện phân bằng điện cực trơ là Ag+, Fe3+, Cu2+, Fe2+, Al3+, H2O.
(7) Fe bị oxi hóa bởi hơi nước ở nhiệt độ cao có thể tạo FeO (trên 570°C) hoặc Fe3O4 (dưới 570°C).
(8) Trong pin Zn-Cu, điện cực Zn là catot, xảy ra quá trình oxi hóa.
Số phát biểu đúng là
A. 6.
B. 7.
C. 5.
D. 4.
Chọn D.
(1) Đúng, Sắt là kim loại phổ biến thứ 2 trong vỏ trái đất (đứng sau kim loại Al).
(2) Sai, Để điều chế kim loại nhôm, người ta có thể dùng phương pháp điện phân nóng chảy Al2O3.
(3) Đúng, Người ta sử dụng quặng giàu sắt để sản xuất gang thép.
(4) Đúng, lúc đó miếng sắt tây bị ăn mòn điện hoá nhanh hơn miếng tôn.
(5) Sai, NaHCO3 có thể dùng làm thuốc chứa bệnh.
(6) Sai, Al3+ không bị điện phân.
(7) Đúng.
(8) Sai, Trong pin Zn-Cu, điện cực Zn là anot và xảy ra quá trình oxi hóa