Cho 28,4 gam P 2 O 5 vào 300 ml dung dịch KOH 1,5M thu được dng dịch X. Cô cạn X thu được hỗn hợp các chất là
A. K 3 PO 4 và KOH
B. K 2 HPO 4 và K 3 PO 4
C. KH 2 PO 4 và K 2 HPO 4
D. KH 2 PO 4 và H3PO4
Cho 28,4 gam P2O5 vào 300 ml dung dịch KOH 1,5M thu được dng dịch X. Cô cạn X thu được hỗn hợp các chất là
A. K3PO4 và KOH
B. K2HPO4 và K3PO4
C. KH2PO4 và K2HPO4
D. KH2PO4 và H3PO4
Đáp án B
nP2O5 = 0,2 mol
nKOH = 0,45 mol
PTHH : P2O5 + 3H2O →2H3PO4
Vì 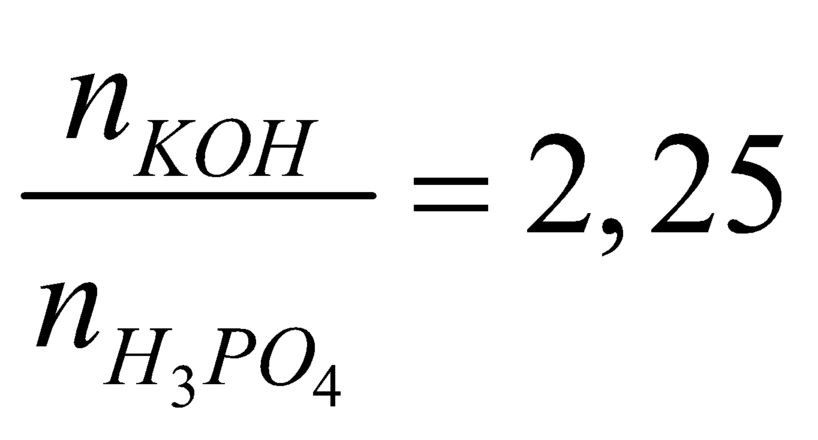 nên phản ứng tạo ra 2 muối K2HPO4 và K3PO4
nên phản ứng tạo ra 2 muối K2HPO4 và K3PO4
Cho 28,4 gam P2O5 vào 300 ml dung dịch KOH 1,5M thu được dng dịch X. Cô cạn X thu được hỗn hợp các chất là
A. K3PO4 và KOH
B. K2HPO4 và K3PO4
C. KH2PO4 và K2HPO4
D. KH2PO4 và H3PO4
Đáp án B
nP2O5 = 0,2 mol
nKOH = 0,45 mol
PTHH : P2O5 + 3H2O →2H3PO4
Vì  nên phản ứng tạo ra 2 muối K2HPO4 và K3PO4
nên phản ứng tạo ra 2 muối K2HPO4 và K3PO4
Cho 28,4 gam P2O5 vào 300 ml dung dịch KOH 1,5M thu được dung dịch X. Cô cạn X thu được hỗn hợp các chất là
A. K3PO4 và KOH
B. K2HPO4 và K3PO4
C. KH2PO4 và K2HPO4
D. KH2PO4 và H3PO4
Đáp án B
nP2O5 = 0,2 mol
nKOH = 0,45 mol
PTHH : P2O5 + 3H2O →2H3PO4
Vì
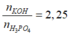
nên phản ứng tạo ra 2 muối K2HPO4 và K3PO4
Cho từ từ 300 ml dung dịch NaHCO3 0,1M, K2CO3 0,2M vào 100 ml dung dịch HCl 0,2M; NaHSO4 0,6M thu được V lít CO2 thoát ra ở đktc và dung dịch X. Thêm vào dung dịch X 100 ml dung dịch KOH 0,6M; BaCl2 1,5M thu được m gam kết tủa. Giá trị của V và m là
A. 1,0752 và 22,254.
B. 1,0752 và 24,224.
C. 0,448 và 25,8.
D. 0,448 và 11,82.
nNaHCO3 = 0,03; nK2CO3 = 0,06
nHCI = 0,02 và nNaHSO4 = 0,06 —> nH+ = 0,08
nHCO3- : nCO32- = 1 : 2 —> Đặt x, 2x là số
mol HCO3- và CO32- phản ứng.
—> nH+ = x + 2.2x = 0,08 => x = 0,016
—> nCO2 = x + 2x = 0,048
—>V=1,0752 lít
Dung dịch X chứa HCO3- dư (0,03 - x = 0,014), CO32- dư (0,06 - 2x = 0,028),
SO42-(0,06) và các ion khác.
nKOH = 0,06 —> Quá đủ để chuyển HCO3- thành CO32-.
nBaCl2 = 0,15 —> BaCO3 (0,014 + 0,028 =0,042) và BaSO4 (0,06)
→ m ↓ = 22 , 254
Đáp án A
Cho từ từ 100 ml dung dịch HCl 0,2M và N a H S O 4 0,6M vào 300 ml dung dịch N a H C O 3 0,1M và K 2 C O 3 0,2M thu được V lit C O 2 (đktc) và dung dịch X. Cho 100ml dung dịch KOH 0,6M và B a C l 2 1,5M vào dung dịch X, thu được m gam kết tủa. Giá trị V và m là
A. 1,0752 lít; 22,254 gam
B. 1,0752 lít; 23,43 gam
C. 0,448 lít ; 25,8 gam
D. 0,448 lít ; 11,82 gam
Đáp án C
n H + =0,02 + 0,06 = 0,08 mol
n H C O 3 - = 0,03 mol
n C O 3 2 - =0,06 mol
Đổ từ từ dung dịch axit vào hỗn hợp muối
CO32- + H+ → HCO3-
0,06 0,06 0,06
HCO3- + H+ →CO2 + H2O
0,02 0,02 mol
=> V = 0,448 l
HCO3- + OH- → CO32- + H2O
0,06 0,06 mol
n S O 4 2 - = 0 , 06 m o l
n B a 2 + = 0,15 mol
⇒ n B a S O 4 = n B a C O 3 = 0,06 mol
=>Vậy m = 0,06.233 + 0,06.197 = 25,8 gam
Cho từ từ 100 ml dung dịch HCl 0,2M và N a H S O 4 0,6M vào 300 ml dung dịch N a H C O 3 0,1M và K 2 C O 3 0,2M thu được V lít C O 2 (đktc) và dung dịch X. Cho 100 ml dung dịch KOH 0,6M và B a C l 2 1,5M vào dung dịch X, thu được m gam kết tủa. Giá trị V và m lần lượt là
A. 1,0752 và 22,254
B. 1,0752 và 23,430
C. 0,4480 và 25,800
D. 0,4480 và 11,820
Cho từ từ 300 ml dung dịch gồm NaHCO3 0,1M và K2CO3 0,2M vào 100 ml dung dịch gồm HCl 0,2M và NaHSO4 0,6M thu được V lít CO2 thoát ra ở đktc và dung dịch X. Thêm vào dung dịch X 100 ml dung dịch gồm KOH 0,6M và BaCl2 1,5M thu được m gam kết tủa. Giá trị của V và m là
A. 1,0752 lít và 8,274 gam.
B. 0,448 lít và 25,8 gam.
C. 1,0752 lít và 22,254 gam.
D. 1,0752 lít và 19,496 gam.
Cho từ từ 300 ml dung dịch gồm NaHCO3 0,1M và K2CO3 0,2M vào 100 ml dung dịch gồm HCl 0,2M và NaHSO4 0,6M thu được V lít CO2 thoát ra ở đktc và dung dịch X. Thêm vào dung dịch X 100 ml dung dịch gồm KOH 0,6M và BaCl2 1,5M thu được m gam kết tủa. Giá trị của V và m là
A. 1,0752 lít và 8,274 gam.
B. 0,448 lít và 25,8 gam.
C. 1,0752 lít và 22,254 gam.
D. 1,0752 lít và 19,496 gam
Cho từ từ, đồng thời khuấy đều 300 ml dung dịch hỗn hợp gồm: NaHCO3 0,1M và K2CO3 0,2M vào 100 ml dung dịch hỗn hợp gồm: HCl 0,2M và NaHSO4 0,6M thu được V lít CO2 (đktc) và dung dịch X. Thêm vào dung dịch X 100 ml dung dịch hỗn hợp gồm: KOH 0,6M và BaCl2 1,5M thu được m gam kết tủa. Giá trị của m là
A. 17,73
B. 31,71
C. 22,254
D. 8,274
Đáp án : C
0 , 03 m o l N a H C O 3 0 , 06 m o l K 2 C O 3 nhỏ từ từ 0 , 02 m o l H C l 0 , 06 m o l K H S O 4
=> 2 muối kiềm sẽ phản ứng theo tỉ lệ mol 1:2
Đặt số mol NaHCO3 phản ứng là x => số mol KCO3 phản ứng là 2x
=> nH+ = 0,02 + 0,06 = x + 2.2x => x = 0,016 mol
=> Sau phản ứng có : 0,014 mol HCO3- ; 0,028 mol CO32- và 0,06 mo SO42-
Khi cho X vào dung dịch chứa : 0,06 mol KOH và 0,15 mol BaCl2
=> nCO3 = 0,014 + 0,028 = 0,042 mol ; nSO4 = 0,06 mol
=> m kết tủa = mBaCO3 + mBaSO4 = 22,254g