Hòa tan hoàn toàn hỗn hợp FeS và FeCO 3 bằng một lượng dung dịch H 2 SO 4 đặc nóng thu được hỗn hợp gồm hai khí X, Y. Công thức hóa học của X, Y lần lượt là:
A. H 2 S và SO 2
B. H 2 S và CO 2
C. SO 2 và CO
D. SO 2 và CO 2
Hòa tan hoàn toàn hỗn hợp FeS và FeCO3 bằng dung dịch HNO3 đặc, nóng, dư thu được hỗn hợp gồm 2 khí CO2 và NO2 (NO2 là sản phẩm khử duy nhất của HNO3) có tỉ khối hơi so với hiđro bằng 22,909. Phần trăm khối lượng của FeS trong hỗn hợp ban đầu là
A. 43,14%.
B. 44,47%.
C. 56,86%.
D. 83,66%.
Hòa tan hoàn toàn m gam hỗn hợp FeO, FeCO3, Fe(OH)2 vào dung dịch H2SO4 đặc, nóng dư thấy thoát ra 5,6 lít hỗn hợp khí SO2 và CO2 (đktc) có tỉ khối so với H2 bằng 28. Tính số mol axit phản ứng ?
ta có hpt : pt1 x+y=0,25 pt 2 64x+44y=28*2*0,25 giải x và y là số mol của CO2 và SO2
bảo toàn e giữa Fe và S ta có nFe=2nSO2 ---> nFe --> nFe2(SO4)3 =1/2nFe --> n gốcSO4 trong muối sau đó cộng mol trong muối và nSO2
cách tính nhanh nH2SO4 phản ứng =2nSO2
mk chưa tính chỉ nêu cách làm chỗ nào sai xót thì mk xin lỗi nha
chúc bạn học tốt
Hòa tan hoàn toàn hỗn hợp gồm 0,002 mol FeS2 và 0,003 mol FeS vào lượng dư dung dịch H2SO4 đặc nóng thu được Fe2(SO4)3, SO2 và H2O. Hấp thụ hết lượng SO2 trên bằng một lượng vừa đủ dung dịch KMnO4 thu được dung dịch có pH = 2. Thể tích dung dịch KMnO4 cần dung là:
A. 2,00 lít
B. 1,5 lít
C. 1,14 lít
D. 2,28 lít
Hòa tan hoàn toàn hỗn hợp gồm 0,002 mol FeS2 và 0,003 mol FeS vào lượng dư dung dịch H2SO4 đặc nóng thu được Fe2(SO4)3, SO2 và H2O. Hấp thụ hết lượng SO2 trên bằng một lượng vừa đủ dung dịch KMnO4 thu được dung dịch có pH = 2. Thể tích dung dịch KMnO4 cần dung là:
A. 2,00 lít
B. 1,5 lít
C. 1,14 lít
D. 2,28 lít
Đáp án D
Áp dụng định luật bảo toàn electron:
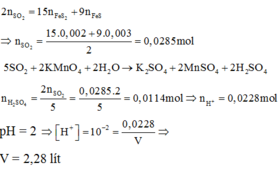
Hòa tan hoàn toàn hỗn hợp FeS và FeCO3 bằng một lượng dung dịch H2SO4 đặc nóng thu được hỗn hợp gồm hai khí X, Y. Công thức hóa học của X, Y lần lượt là
A. H2S và SO2
B. H2S và CO2
C. SO2 và CO
D. SO2 và CO2
Hòa tan hoàn toàn hỗn hợp gồm 0,02 mol FeS2 và 0,03 mol FeS vào dung dịch H2SO4 đặc nóng thu được Fe2(SO4)3, SO2 và H2O. Hấp thụ hết SO2 bằng một lượng vừa đủ dung dịch KMnO4 thu được dung dịch Y trong suốt có pH =2. Thể tích dung dịch Y là
A. 11,4 l
B. 5,7 l
C. 17,1 l
D. 22,8 l
Đáp án D
Ta có :
Fe → Fe3+ + 3e
S → S+6 + 6e
S+6 + 2e → S+4
Do đó số mol SO2 là (0,05 . 3 + 0,07.6 ) / 2= 0,285 mol
5SO2 + 2H2O + 2KMnO4 → K2SO4 + 2 MnSO4 + 2H2SO4
Nên số mol H2SO4 tạo ra là 0,114 mol
=> [H+] = 0,228 : V =0,01 => V =22,8 l
Hòa tan hoàn toàn hỗn hợp gồm 0,02 mol FeS2 và 0,03 mol FeS vào lượng dung dịch H2SO4 đặc nóng thu được Fe2(SO4)3, SO2 và H2O. Hấp thụ hết SO2 bằng một lượng vừa đủ dung dịch KMnO4 thu được dung dịch Y không màu, trong suốt có pH = 2. Thể tích của dung dịch Y là
A. 11,4 lít
B. 5,7 lít
C. 17,1 lít
D. 22,8 lít
Bảo toàn electron: 15nFeS2 + 9nFeS = 2nSO2
⇒ nSO2 = 0,285 mol.
Phản ứng: 5SO2 + 2KMnO4 + 2H2O → K2SO4 + 2MnSO4 + 2H2SO4
∑nH+ = 0,285 × 2 ÷ 5 × 2 = 0,228 mol
⇒ VY = 0,228 ÷ 10 – 2 = 22,8 lít.
Đáp án D
Hòa tan hoàn toàn hỗn hợp gồm 0,02 mol FeS2 và 0,03 mol FeS vào lượng dung dịch H2SO4 đặc nóng thu được Fe2(SO4)3, SO2 và H2O. Hấp thụ hết SO2 bằng một lượng vừa đủ dung dịch KMnO4 thu được dung dịch Y không màu, trong suốt có pH = 2. Thể tích của dung dịch Y là
A. 11,4 lít
B. 5,7 lít
C. 17,1 lít
D. 22,8 lít
Chọn đáp án D
Bảo toàn electron: 15nFeS2 + 9nFeS = 2nSO2 ⇒ nSO2 = 0,285 mol.
Phản ứng: 5SO2 + 2KMnO4 + 2H2O → K2SO4 + 2MnSO4 + 2H2SO4
∑nH+ = 0,285 × 2 ÷ 5 × 2 = 0,228 mol ⇒ VY = 0,228 ÷ 10 – 2 = 22,8 lít
Hòa tan hoàn toàn 14,4g hỗn hợp Fe và Fes bằng 200ml dung dịch Hcl vừa đủ thu được hỗn hợp khí X có tỉ khối so với H2 là 9 .Tính nồng độ mol của Hcl đã dùng
Ta có (sơ đồ đường chéo nha)
H2 : 2 16
18
H2S: 34 16
=>nH2/nH2S=1/1
PTPU Fe + 2HCl -> FeCl2 + H2
FeS + 2HCl -> FeCl2 +H2S
theo ptpu nFe= nH2 , nFeS=nH2S
=> nFe=nFeS=14,4/144=0,1 mol
theo ptpu : nHCl=2nFe +2nFeS=0,4 mol
=> CM(HCl)= 0,4/0,2=2 M