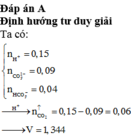Dẫn V lít khí S O 2 ở đktc vào dung dịch chứa 0,15 mol B a ( O H ) 2 thấy tạo ra 21,7 gam kết tủa. Tính giá trị của V.

Những câu hỏi liên quan
Cho rất từ từ từng giọt dung dịch chứa 200 ml dung dịch HCl 2M vào dung dịch X chứa 0,15 mol Na2CO3 và 0,15 mol NaHCO3 . Thể tích khí CO2 thoát ra (ở đktc) là A. 3,36 lít. B. 6,72 lít. C. 2,24 lít. D. 5,6 lít
Nhỏ từ từ dung dịch chứa 0,15 mol HCl vào dung dịch chứa Na2CO3 0,03 mol, NaHCO3 0,04 mol và K2CO3 0,06 mol thu được V lít khí CO2 (đktc). Giá trị của V là: A. 1,344 B. 2,24 C. 1,792 D. 2,688
Đọc tiếp
Nhỏ từ từ dung dịch chứa 0,15 mol HCl vào dung dịch chứa Na2CO3 0,03 mol, NaHCO3 0,04 mol và K2CO3 0,06 mol thu được V lít khí CO2 (đktc). Giá trị của V là:
A. 1,344
B. 2,24
C. 1,792
D. 2,688
Cho từ từ từng giọt của dung dịch chứa b mol HCl vào dung dịch chứa a mol Na2CO3 thu được V lít khí CO2. Ngược lại, cho từ từ từng giọt của dung dịch chứa a mol Na2CO3 vào dung dịch chứa b mol HCl thu được 2V lít khí CO2 (thể tích khí đều đo ở đktc). Mối quan hệ giữa a và b là A. a 0,75b. B. a 0,8b. C. a 0,35b. D. a 0,5b
Đọc tiếp
Cho từ từ từng giọt của dung dịch chứa b mol HCl vào dung dịch chứa a mol Na2CO3 thu được V lít khí CO2. Ngược lại, cho từ từ từng giọt của dung dịch chứa a mol Na2CO3 vào dung dịch chứa b mol HCl thu được 2V lít khí CO2 (thể tích khí đều đo ở đktc). Mối quan hệ giữa a và b là
A. a = 0,75b.
B. a = 0,8b.
C. a = 0,35b.
D. a = 0,5b
Nếu b ≥ 2a thì chắc chắn CO2 sinh ra sẽ như nhau, nhưng đề cho CO2 khác nhau → b < 2a hay a > 0,5b
→ Loại C, D
Thí nghiệm 1: Cho H+ vào CO32-
H+ + CO32- → HCO3-
a a a
H+ + HCO3- → CO2 + H2O
(b – a) → b – a
Thí nghiệm 2: CO32- vào H+
2H+ + CO32- → CO2 + H2O
b → 0,5b
Ta có 0,5b = 2(b – a) → 2a = 1,5b → a = 0,75b
Đáp án A
Đúng 0
Bình luận (0)
Cho từ từ từng giọt của dung dịch chứa b mol HCl vào dung dịch chứa a mol Na2CO3 thu được V lít khí CO2. Ngược lại, cho từ từ từng giọt của dung dịch chứa a mol Na2CO3 vào dung dịch chứa b mol HCl thu được 2V lít khí CO2 (thể tích khí đều đo ở đktc). Mối quan hệ giữa a và b là A. a 0,75b B. a 0,8b C. a 0,35b D. a 0,5b
Đọc tiếp
Cho từ từ từng giọt của dung dịch chứa b mol HCl vào dung dịch chứa a mol Na2CO3 thu được V lít khí CO2. Ngược lại, cho từ từ từng giọt của dung dịch chứa a mol Na2CO3 vào dung dịch chứa b mol HCl thu được 2V lít khí CO2 (thể tích khí đều đo ở đktc). Mối quan hệ giữa a và b là
A. a = 0,75b
B. a = 0,8b
C. a = 0,35b
D. a = 0,5b
Đáp án A
Nếu b ≥ 2a thì chắc chắn CO2 sinh ra sẽ như nhau, nhưng đề cho CO2 khác nhau b < 2a hay a > 0,5b
Loại C, D
Thí nghiệm 1: Cho H+ vào CO32-
H+ + CO32- → HCO3-
a a a
H+ + HCO3- → CO2 + H2O
(b – a) → b – a
Thí nghiệm 2: CO32- vào H+
2H+ + CO32- → CO2 + H2O
b → 0,5b
Ta có 0,5b = 2(b – a) 2a = 1,5b a = 0,75b
Đúng 0
Bình luận (0)
Cho 0,15 mol bột Cu và 0,3 mol Fe(NO3)2 vào dung dịch chứa 0,5 mol H2SO4. Sau khi các phản ứng xảy ra hoàn toàn, thu được V lít khí NO (sản phẩm khử duy nhất, ở đktc). Giá trị của V là
A. 8,96.
B. 4,48.
C. 6,72.
D. 10,08
Có quá trình khử : 4H+ + NO3- + 3e → NO +2H2O
Có nH+ = 1 mol, nNO3- = 0,6 mol ⇒ số e nhận tối đa là 3 × 1 ÷ 4 = 0,75 mol
Quá trình oxi hoá : Cu → Cu2+ + 2e và Fe2+ → Fe3+ + 1e
Số e nhường tối đa là là 2×0,15 + 0,3 = 0,6 mol < ne nhận tối đa
Vậy chứng tỏ NO được tính theo số e nhường ⇒ NO = 0,6 : 3 = 0,2 mol.
⇒ V = 4,48 lít
Đáp án là B
Đúng 0
Bình luận (0)
Cho 0,15 mol bột Cu và 0,3 mol Fe(NO3)2 vào dung dịch chứa 0,5 mol H2SO4. Sau khi các phản ứng xảy ra hoàn toàn, thu được V lít khí NO (sản phẩm khử duy nhất, ở đktc). Giá trị của V là A. 8,96 B. 4,48 C. 6,72. D. 10,08.
Đọc tiếp
Cho 0,15 mol bột Cu và 0,3 mol Fe(NO3)2 vào dung dịch chứa 0,5 mol H2SO4. Sau khi các phản ứng xảy ra hoàn toàn, thu được V lít khí NO (sản phẩm khử duy nhất, ở đktc). Giá trị của V là
A. 8,96
B. 4,48
C. 6,72.
D. 10,08.
Cho 0,15 mol bột Cu và 0,3 mol Fe(NO3)2 vào dung dịch chứa 0,5 mol H2SO4 (loãng). Sau khi các phản ứng xảy ra hoàn toàn, thu được V lít khí NO (sản phẩm khử duy nhất, ở đktc). Giá trị của V là A. 10,08. B. 4,48. C. 6,72. D. 8,96.
Đọc tiếp
Cho 0,15 mol bột Cu và 0,3 mol Fe(NO3)2 vào dung dịch chứa 0,5 mol H2SO4 (loãng). Sau khi các phản ứng xảy ra hoàn toàn, thu được V lít khí NO (sản phẩm khử duy nhất, ở đktc). Giá trị của V là
A. 10,08.
B. 4,48.
C. 6,72.
D. 8,96.
Đáp án B
Có quá trình khử : 4H+ + NO3- + 3e → NO +2H2O
Có nH+ = 1 mol, nNO3- = 0,6 mol ⇒ số e nhận tối đa là 3 × 1 ÷ 4 = 0,75 mol
Quá trình oxi hoá : Cu → Cu2+ + 2e và Fe2+ → Fe3+ + 1e
Số e nhường tối đa là là 2×0,15 + 0,3 = 0,6 mol < ne nhận tối đa
Vậy chứng tỏ NO được tính theo số e nhường ⇒ NO = 0,6 : 3 = 0,2 mol.
⇒ V = 4,48 lít
Đúng 0
Bình luận (0)
Cho 0,15 mol bột Cu và 0,3 mol Fe(NO3)2 vào dung dịch chứa 0,5 mol H2SO4 (loãng). Sau khi các phản ứng xảy ra hoàn toàn, thu được V lít khí NO (sản phẩm khử duy nhất, ở đktc). Giá trị của V là A. 10,08 B. 4,48. C. 6,72 D. 8,96
Đọc tiếp
Cho 0,15 mol bột Cu và 0,3 mol Fe(NO3)2 vào dung dịch chứa 0,5 mol H2SO4 (loãng). Sau khi các phản ứng xảy ra hoàn toàn, thu được V lít khí NO (sản phẩm khử duy nhất, ở đktc). Giá trị của V là
A. 10,08
B. 4,48.
C. 6,72
D. 8,96
Đáp án B
Có quá trình khử : 4H+ + NO3- + 3e → NO +2H2O
Có nH+ = 1 mol, nNO3- = 0,6 mol ⇒ số e nhận tối đa là 3 × 1 ÷ 4 = 0,75 mol
Quá trình oxi hoá : Cu → Cu2+ + 2e và Fe2+ → Fe3+ + 1e
Số e nhường tối đa là là 2×0,15 + 0,3 = 0,6 mol < ne nhận tối đa
Vậy chứng tỏ NO được tính theo số e nhường ⇒ NO = 0,6 : 3 = 0,2 mol.
⇒ V = 4,48 lít
Đúng 0
Bình luận (0)
Cho 0,15 mol bột Cu và 0,3 mol Fe(NO3)2 vào dung dịch chứa 0,5 mol H2SO4 (loãng). Sau khi các phản ứng xảy ra hoàn toàn, thu được V lít khí NO (sản phẩm khử duy nhất, ở đktc). Giá trị của V là A. 10,08. B. 4,48. C. 6,72. D. 8,96.
Đọc tiếp
Cho 0,15 mol bột Cu và 0,3 mol Fe(NO3)2 vào dung dịch chứa 0,5 mol H2SO4 (loãng). Sau khi các phản ứng xảy ra hoàn toàn, thu được V lít khí NO (sản phẩm khử duy nhất, ở đktc). Giá trị của V là
A. 10,08.
B. 4,48.
C. 6,72.
D. 8,96.
Có quá trình khử : 4H+ + NO3- + 3e → NO +2H2O
Có nH+ = 1 mol, nNO3- = 0,6 mol ⇒ số e nhận tối đa là 3 × 1 ÷ 4 = 0,75 mol
Quá trình oxi hoá : Cu → Cu2+ + 2e và Fe2+ → Fe3+ + 1e
Số e nhường tối đa là là 2×0,15 + 0,3 = 0,6 mol < ne nhận tối đa
Vậy chứng tỏ NO được tính theo số e nhường ⇒ NO = 0,6 : 3 = 0,2 mol.
⇒ V = 4,48 lít
Đáp án B
Đúng 0
Bình luận (0)