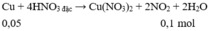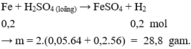Một hỗn hợp bột hai kim loại Mg và R được chia thành 2 phần bằng nhau:
- Phần 1: Cho tác dụng với HNO3 dư thu được 1,68 (l) khí duy nhất(đktc)
- Phần 2: Hoà tan trong 400 ml HNO3 loãng 0,7M thu được V(l) khí không màu, hoá nâu trong không khí (đktc) . Tính giá trị của V.